1 . 下列说法或有关化学用语的表达正确的是( )
| A.在基态多电子原子中,p轨道电子能量一定高于s轨道电子能量 |
B.基态Fe原子的价电子轨道表示式为 |
| C.因硫元素电负性比磷元素大,故硫元素第一电离能比磷元素第一电离能大 |
| D.根据原子核外电子排布的特点,Cu在元素周期表中位于s区 |
您最近一年使用:0次
2020-04-09更新
|
125次组卷
|
3卷引用:第1章 原子结构——C挑战区 模拟高考(鲁科版选修3)
第1章 原子结构——C挑战区 模拟高考(鲁科版选修3)(已下线)第一单元 原子结构(基础过关)-2020-2021学年高二化学单元测试定心卷(鲁科版选修3)新疆维吾尔自治区皮山县高级中学2022-2023学年高二下学期4月期中化学试题
2 . 下列关于电离能和电负性的说法不正确的是( )
| A.第一电离能:Mg>Al |
| B.硅的第一电离能和电负性均大于磷 |
| C.锗的第一电离能和电负性均小于碳 |
| D.F、K、Fe、Ni四种元素中电负性最大的是F |
您最近一年使用:0次
2020-04-09更新
|
1070次组卷
|
7卷引用:第1章 原子结构 易错疑难集训(二)——A学习区 夯实基础(鲁科版选修3)
3 . 在下列横线上,填上适当的元素符号:
(1)在第三周期中,第一电离能最小的元素是_________ ,第一电离能最大的元素是______ 。
(2)在元素周期表中,电负性最大的元素是_______ ,电负性最小的元素是_________ (放射性元素除外)。
(3)最活泼的金属元素是_______ 。
(4)最活泼的非金属元素是______ 。
(5)第二、三、四周期元素中p轨道半充满的原子是_______ 。
(6)电负性相差最大的两种元素是________ (放射性元素除外)。
(1)在第三周期中,第一电离能最小的元素是
(2)在元素周期表中,电负性最大的元素是
(3)最活泼的金属元素是
(4)最活泼的非金属元素是
(5)第二、三、四周期元素中p轨道半充满的原子是
(6)电负性相差最大的两种元素是
您最近一年使用:0次
2020-04-09更新
|
172次组卷
|
5卷引用:第3节 原子结构与元素性质——A学习区 夯实基础(鲁科版选修3)
第3节 原子结构与元素性质——A学习区 夯实基础(鲁科版选修3)(已下线)1.3.2 元素的电负性及其变化规律-2020-2021学年高二化学课时同步练(鲁科2019选择性必修2)(已下线)1.2.2 原子结构与元素周期律(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修2)(已下线)1.2.3 元素的电负性及其变化规律-2021-2022学年高二化学同步课时跟踪训练(人教版2019选择性必修2)1.3.2元素的电离能、电负性及其变化规律(课后)-鲁科版选择性必修2
解题方法
4 . A、B都是短周期元素,原子最外层电子排布式分别为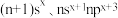 。A与B可形成化合物C和D。D溶于水时有气体逸出,该气体能使带火星的木条复燃。请回答下列问题。
。A与B可形成化合物C和D。D溶于水时有气体逸出,该气体能使带火星的木条复燃。请回答下列问题。
(1)比较电离能:
①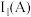
_____ 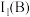 (填“>”或“<”,下同)
(填“>”或“<”,下同)
②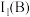
_____  。
。
(2)通常A元素的化合价是_____________ ,对A元素呈现这种价态进行解释:
①用原子结构的观点进行解释:_____________ 。
②用电离能的观点进行解释:______________ 。
(3)写出D跟水反应的离子方程式:_________ 。
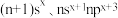 。A与B可形成化合物C和D。D溶于水时有气体逸出,该气体能使带火星的木条复燃。请回答下列问题。
。A与B可形成化合物C和D。D溶于水时有气体逸出,该气体能使带火星的木条复燃。请回答下列问题。(1)比较电离能:
①
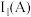
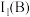 (填“>”或“<”,下同)
(填“>”或“<”,下同)②
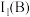
 。
。(2)通常A元素的化合价是
①用原子结构的观点进行解释:
②用电离能的观点进行解释:
(3)写出D跟水反应的离子方程式:
您最近一年使用:0次
名校
解题方法
5 . 氮化钛(Ti3N4)为金黄色晶体,由于具有令人满意的仿金效果,越来越多地成为黄金的代替品。以TiCl4为原料,经过一系列反应可以制得Ti3N4和纳米TiO2(如图1)。
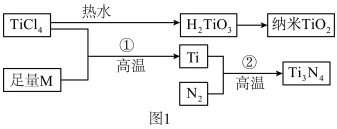
图中的M是短周期金属元素,M的部分电离能如表:
请回答下列问题:
(1)Ti的基态原子外围电子排布式为________________ 。
(2)M是________ (填元素符号),该金属晶体的堆积模型为六方最密堆积,配位数为____ 。
(3)纳米TiO2是一种应用广泛的催化剂,纳米TiO2催化的一个实例如图2所示。化合物甲的分子中采取sp2方式杂化的碳原子有________ 个,化合物乙中采取sp3方式杂化的原子3对应的元素的电负性由大到小的顺序为________________ 。
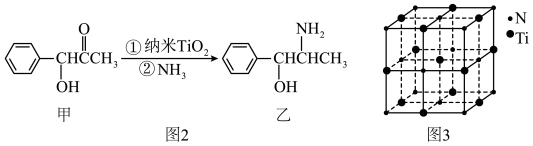
(4)有一种氮化钛晶体的晶胞与NaCl晶胞相似,如图3所示,该晶胞中N、Ti之间的最近距离为a pm,则该氮化钛的密度为________________ g/cm3 (NA为阿伏加 德罗常数的值,只列计算式)。该晶体中与氮原子距离相等且最近的氮原子有________ 个。
(5)科学家通过X-射线探明KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似。且知三种离子晶体的晶格能数据:
KCl、CaO、TiN三种离子晶体熔点由高到低的顺序为__________________ 。

图中的M是短周期金属元素,M的部分电离能如表:
I1 | I2 | I3 | I4 | I5 | |
| 电离能/(kJ/mol) | 738 | 1451 | 7733 | 10540 | 13630 |
请回答下列问题:
(1)Ti的基态原子外围电子排布式为
(2)M是
(3)纳米TiO2是一种应用广泛的催化剂,纳米TiO2催化的一个实例如图2所示。化合物甲的分子中采取sp2方式杂化的碳原子有

(4)有一种氮化钛晶体的晶胞与NaCl晶胞相似,如图3所示,该晶胞中N、Ti之间的最近距离为a pm,则该氮化钛的密度为
(5)科学家通过X-射线探明KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似。且知三种离子晶体的晶格能数据:
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/(kJ/mol) | 786 | 715 | 3401 |
KCl、CaO、TiN三种离子晶体熔点由高到低的顺序为
您最近一年使用:0次
2020-03-30更新
|
296次组卷
|
7卷引用:二轮复习 专题17 物质结构与性质 押题专练
解题方法
6 . A、B、C、D、E代表5种元素。请填空:
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为______
(2)B元素的 价离子和C元素的
价离子和C元素的 价离子的核外电子排布情况均与氩原子相同,则B元素的
价离子的核外电子排布情况均与氩原子相同,则B元素的 价离子的结构示意图为
价离子的结构示意图为______ ,C元素原子有______ 个能层,______ 个能级,______ 个非空原子轨道
(3)D元素的 价离子的3d能级为半充满状态,D的元素符号为
价离子的3d能级为半充满状态,D的元素符号为______ ,其基态原子的核外电子排布式为______
(4)E元素基态原子的M层全充满,N层只有一个电子,E的元素符号为______ ,其基态原子的简化电子排布式为______
(1)A元素基态原子的最外层有3个未成对电子,次外层有2个电子,其元素符号为
(2)B元素的
 价离子和C元素的
价离子和C元素的 价离子的核外电子排布情况均与氩原子相同,则B元素的
价离子的核外电子排布情况均与氩原子相同,则B元素的 价离子的结构示意图为
价离子的结构示意图为(3)D元素的
 价离子的3d能级为半充满状态,D的元素符号为
价离子的3d能级为半充满状态,D的元素符号为(4)E元素基态原子的M层全充满,N层只有一个电子,E的元素符号为
您最近一年使用:0次
2020-03-05更新
|
230次组卷
|
3卷引用:人教化学选修3第一章第一节课时3
名校
解题方法
7 . 大型客机燃油用四乙基铅[Pb(CH2CH3)4])做抗震添加剂,但皮肤长期接触四乙基铅对身体健康有害,可用硫基乙胺(HSCH2CH2NH2)和KMnO4清除四乙基铅。
(1)碳原子核外电子的空间运动状态有______ 种,基态锰原子的外围电子排布式为___ ,该原子能量最高的电子的电子云轮廓图形状为________ 。
(2)N、C和Mn电负性由大到小的顺序为____________ 。
(3)HSCH2CH2NH2中C的杂化方式为_____ ,其中NH2-空间构型为____ ;N和P的价电子相同,但磷酸的组成为H3PO4,而硝酸的组成不是H3NO4,其原因是_______ 。
(4)Pb(CH2CH3)4是一种难电离且易溶于有机溶剂的配合物,其晶体类型属于_____ 晶体。已知Pb(CH2CH3)4晶体的堆积方式如下。
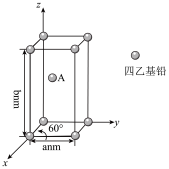
Pb(CH2CH3)4]在xy平面上的二维堆积中的配位数是___ ,A分子的坐标参数为_____ ;设阿伏加 德罗常数为NA/mol,Pb(CH2CH3)4]的摩尔质量为Mg/mol,则Pb(CH2CH3)4]晶体的密度是_____ g/cm3 (列出计算式即可)。
(1)碳原子核外电子的空间运动状态有
(2)N、C和Mn电负性由大到小的顺序为
(3)HSCH2CH2NH2中C的杂化方式为
(4)Pb(CH2CH3)4是一种难电离且易溶于有机溶剂的配合物,其晶体类型属于

Pb(CH2CH3)4]在xy平面上的二维堆积中的配位数是
您最近一年使用:0次
2020-02-24更新
|
654次组卷
|
3卷引用:四川省遂宁市第二中学2020届高三上学期第二次高考模拟理综化学试题
四川省遂宁市第二中学2020届高三上学期第二次高考模拟理综化学试题(已下线)专题6.4 物质结构与性质(选考)(综合提升卷)——巅峰冲刺2020年高考化学二轮专项提升北京专家2020届高三高考模拟试卷(二)化学试题
解题方法
8 . 下列化学用语的表达正确的是
A.二氧化碳的比例模型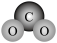 |
B.原子核内有10个中子的原子: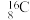 |
C. 的最外层电子排布式为 的最外层电子排布式为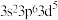 |
D.Cu基态的外围电子排布图: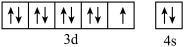 |
您最近一年使用:0次
2020-02-11更新
|
283次组卷
|
2卷引用:2020届高三化学二轮物质结构题型专攻——原子结构与性质【基础专练】
9 . 下列说法中正确的是
| A.基态原子的N层上只有一个电子的元素,一定是ⅠA族元素 | ||||||||||||||
B.原子的价电子排布为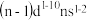 的元素一定是副族元素 的元素一定是副族元素 | ||||||||||||||
C.某主族元素的电离能 数据如下表所示 数据如下表所示 单位: 单位: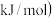 ,可推测该元素位于元素周期表第ⅤA族 ,可推测该元素位于元素周期表第ⅤA族
| ||||||||||||||
D.在①P、S ,②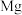 、Ca,③ 、Ca,③ 、F三组元素中,每组中第一电离能较大的元素的原子序数之和为36 、F三组元素中,每组中第一电离能较大的元素的原子序数之和为36 |
您最近一年使用:0次
解题方法
10 . 锗在自然界中非常分散,几乎没有比较集中的锗矿,因此被人们称为“稀散金属”。回答下列问题:
(1)基态锗原子最外层电子排布图为_______ ,Ge原子的电子发生跃迁时会吸收或放出不同的光,可用_______  填仪器名称
填仪器名称 摄取其原子光谱,从而鉴定Ge元素的存在。
摄取其原子光谱,从而鉴定Ge元素的存在。
(2)锗元素能形成无机化合物 如锗酸钠:
如锗酸钠: ;二锗酸钠:
;二锗酸钠: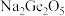 ;四锗酸钠:
;四锗酸钠: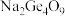 等
等 ,也能形成类似于烷烃的锗烷
,也能形成类似于烷烃的锗烷 。
。
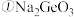 中锗原子的杂化方式为
中锗原子的杂化方式为______________ 。
 锗与碳同族,性质及结构有一定的相似性,据此推测
锗与碳同族,性质及结构有一定的相似性,据此推测 二锗酸钠
二锗酸钠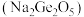 中含有的
中含有的 键的数目为
键的数目为_________ 。
 至今没有发现n大于5的锗烷,根据下表提供的数据分析其中的原因:
至今没有发现n大于5的锗烷,根据下表提供的数据分析其中的原因:___________________ 。
(3)有机多元膦酸锗配合物是由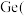 Ⅳ
Ⅳ 与
与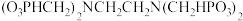 形成的,其结构如下:
形成的,其结构如下:
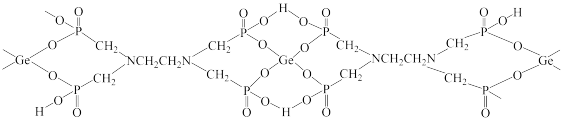
 该配合物中,下列作用力不存在的有
该配合物中,下列作用力不存在的有_________
A.极性键 非极性键
非极性键  金属键
金属键  配位键
配位键  氢键
氢键  键
键
 该配合物中
该配合物中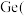 Ⅳ
Ⅳ 的配位数是
的配位数是_______ ;配位原子是_______  填元素符号
填元素符号 。
。
 试解释磷酸
试解释磷酸 酸性为什么与亚硝酸相近?
酸性为什么与亚硝酸相近?______________ 。
(4)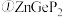 常作为军事上的红外制导材料,其理想晶胞如图所示。测得晶胞参数
常作为军事上的红外制导材料,其理想晶胞如图所示。测得晶胞参数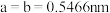 ,
,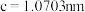 ,该晶体的密度为
,该晶体的密度为_______ 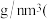 列出算式即可,阿伏加德罗常数用
列出算式即可,阿伏加德罗常数用 表示
表示 。
。
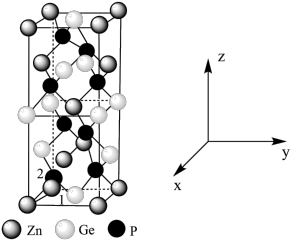
 原子的分数坐标即将晶胞参数a、b、c均看作“1”所得出的三维空间坐标,以1号Zn为坐标原点,则
原子的分数坐标即将晶胞参数a、b、c均看作“1”所得出的三维空间坐标,以1号Zn为坐标原点,则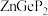 晶胞图中标号为“2”的P原子的分数坐标为
晶胞图中标号为“2”的P原子的分数坐标为_______ 。
(1)基态锗原子最外层电子排布图为
 填仪器名称
填仪器名称 摄取其原子光谱,从而鉴定Ge元素的存在。
摄取其原子光谱,从而鉴定Ge元素的存在。(2)锗元素能形成无机化合物
 如锗酸钠:
如锗酸钠: ;二锗酸钠:
;二锗酸钠: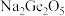 ;四锗酸钠:
;四锗酸钠: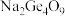 等
等 ,也能形成类似于烷烃的锗烷
,也能形成类似于烷烃的锗烷 。
。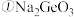 中锗原子的杂化方式为
中锗原子的杂化方式为 锗与碳同族,性质及结构有一定的相似性,据此推测
锗与碳同族,性质及结构有一定的相似性,据此推测 二锗酸钠
二锗酸钠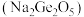 中含有的
中含有的 键的数目为
键的数目为 至今没有发现n大于5的锗烷,根据下表提供的数据分析其中的原因:
至今没有发现n大于5的锗烷,根据下表提供的数据分析其中的原因:| 化学键 |  |  |  |  |
键能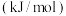 | 346 | 411 | 188 | 288 |
(3)有机多元膦酸锗配合物是由
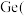 Ⅳ
Ⅳ 与
与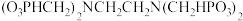 形成的,其结构如下:
形成的,其结构如下:
 该配合物中,下列作用力不存在的有
该配合物中,下列作用力不存在的有A.极性键
 非极性键
非极性键  金属键
金属键  配位键
配位键 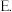 氢键
氢键 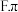 键
键 该配合物中
该配合物中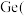 Ⅳ
Ⅳ 的配位数是
的配位数是 填元素符号
填元素符号 。
。 试解释磷酸
试解释磷酸 酸性为什么与亚硝酸相近?
酸性为什么与亚硝酸相近?(4)
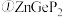 常作为军事上的红外制导材料,其理想晶胞如图所示。测得晶胞参数
常作为军事上的红外制导材料,其理想晶胞如图所示。测得晶胞参数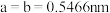 ,
,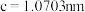 ,该晶体的密度为
,该晶体的密度为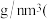 列出算式即可,阿伏加德罗常数用
列出算式即可,阿伏加德罗常数用 表示
表示 。
。
 原子的分数坐标即将晶胞参数a、b、c均看作“1”所得出的三维空间坐标,以1号Zn为坐标原点,则
原子的分数坐标即将晶胞参数a、b、c均看作“1”所得出的三维空间坐标,以1号Zn为坐标原点,则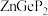 晶胞图中标号为“2”的P原子的分数坐标为
晶胞图中标号为“2”的P原子的分数坐标为
您最近一年使用:0次



