名校
解题方法
1 . 由C、H和与C处于同周期的X、Y四种元素组成的穴醚的键线式如图,该结构中除H外其余原子均满足8电子稳定结构,其空腔直径大约为260~320 pm,可以适配直径与之相近的碱金属离子从而实现离子识别。下列说法正确的是
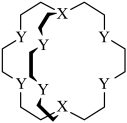
| 离子 | 直径/pm |
 | 204 |
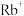 | 304 |
| A.第一电离能:X>Y |
| B.简单氢化物的沸点:X>Y |
| C.键角:C-Y-C>C-X-C |
D.该穴醚可与 通过配位键形成超分子,对 通过配位键形成超分子,对 进行识别 进行识别 |
您最近一年使用:0次
2024-03-05更新
|
689次组卷
|
3卷引用:辽宁省七校协作体2023-2024学年高二下学期5月期中联考化学试题
2 . 下列说法或有关化学用语的表达正确的是
| A.在基态多电子原子中,p轨道电子能量一定高于s轨道电子能量 |
B.基态Fe原子的外围电子排布图为: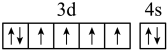 |
| C.因氧元素电负性比氮元素大,故氧原子第一电离能比氮原子第一电离能大 |
| D.根据原子核外电子排布的特点,Cu在周期表中属于s区元素 |
您最近一年使用:0次
2024-02-04更新
|
204次组卷
|
62卷引用:2015-2016学年辽宁省五校协作体高二下学期期中考试化学试卷
2015-2016学年辽宁省五校协作体高二下学期期中考试化学试卷2014-2015学年宁夏宁大附中高二上学期期中考试化学试卷2014-2015吉林省吉林市第五十五中学高二下学期期中考试化学试卷2015-2016学年贵州省思南中学高二下期中化学试卷内蒙古自治区第一机械制造(集团)有限公司第一中学2018-2019学年高二下学期期中考试化学试题辽宁省丹东市2017-2018学年高二下学期期末质量监测化学试题陕西省榆林市第十二中学2019-2020学年高二下学期期中考试化学试题吉林省长春市第二十九中学2019-2020学年高二下学期期中考试化学试题安徽省安庆市太湖县2019-2020学年高二下学期期中质量调研考试化学试题福建省莆田市仙游县第二中学2019-2020学年高二下学期期中考试化学试题四川省南充市阆中中学2020-2021学年高二上学期期中考试化学试题宁夏青铜峡市高级中学2020-2021学年高二下学期期中考试化学试题辽宁省沈阳市辽中区第一高级中学2020-2021学年高二下学期开学考试化学试题天津市实验中学滨海学校2020-2021学年高二下学期期中化学试题甘肃省武威第十八中学2020-2021学年高二下学期期中考试化学试题四川省遂宁市第二中学校2021-2022学年高二上学期期中考试化学试题辽宁省本溪市第二高级中学2021-2022学年高二上学期期末考试化学试题安徽省合肥市肥东县综合高中2021-2022学年高二下学期期中考试化学试题福建省泉州科技中学2021-2022学年高二下学期期中考试化学试题宁夏青铜峡市宁朔中学2022-2023学年高二下学期期中考试化学试题四川省广元中学2022-2023学年高二下学期5月期中考试化学试题安徽省安庆市第二中学2022-2023学年高二下学期期中考试化学试题(已下线)2013-2014宁夏银川一中高二下学期期末考试化学试卷2015-2016学年山西省大同一中高二下3月月考化学试卷2015-2016学年云南省德宏州芒一中高二下学期期末化学试卷山西省大同市第一中学2016-2017学年高二5月月考化学试题新疆呼图壁县第一中学2016-2017学年高二下学期期末考试化学试题贵州省思南中学2016-2017学年高二下学期期末考试化学试题2017-2018学年人教版高中化学选修三 模块综合质量检测吉林省辽源五中2017-2018学年高二下学期第一次月考化学试题四川省广安市第二中学校2017-2018学年高二下学期第二次月考化学试题山西省沁县中学2018-2019学年高二下学期第一次月考化学试题吉林省扶余市第一中学2018-2019学年高二下学期第一次月考化学试题山东省聊城市2019-2020学年高三化学一轮复习《物质结构与性质(》模拟测试四川省广安第二中学校2017-2018学年高二下学期第一次月考化学试题广西靖西市第二中学2019-2020学年高二下学期开学考试化学试题江苏省如东高级中学2019-2020学年高一下学期第二次阶段测试化学试题安徽省蚌埠第三中学2019-2020学年高二下学期期末考试化学试题(已下线)模块同步卷12 综合检测卷(提升卷)-《灯塔金卷系列》2020-2021学年高二化学模块同步卷(人教版选修3)(已下线)专题11 物质结构与性质——备战2021年高考化学纠错笔记山东省济南市济阳区闻韶中学2020-2021学年高三(3班)12月第一次模拟考试化学试题宁夏青铜峡市高级中学2020-2021学年高二下学期第一次月考化学试题(已下线)作业02 原子结构与元素的性质-2021年高二化学暑假作业(人教版2019)新疆昌吉教育共同体2020-2021学年高二下学期期末质量检测化学试题福建省漳州市正兴学校2020-2021学年高二下学期期末考试化学试题宁夏银川市第六中学2020-2021学年高二下学期期末考试化学试题山西省长治市沁源县第一中学等名校2021-2022学年高二下学期5月联考化学试题吉林地区普通高中友好学校联合体2021-2022学年高二下学期期末考试化学试题第一章 本章复习提升1云南省石屏县第一中学2021-2022学年高二下学期3月份考试化学试题福建省莆田市第一中学2021-2022学年高二下学期期末考试化学试题四川省广安市邻水县二中 2022-2023学年高三上学期9月考化学试题甘肃省庆阳市第六中学2021-2022学年高二下学期期末考试化学试题新疆克拉玛依市高级中学2021-2022学年高二下学期期末考试化学试题重庆市荣昌永荣中学校2021-2022学年高二下学期期末考试化学试题山东省新泰市第一中学2022-2023学年高二下学期第一次大单元考试化学试题山东省青岛第十九中学2022-2023学年高二下学期4月月考化学试题河北省唐山市开滦一中2022-2023学年高二下学期期末考试化学试题吉林省普通高中友好学校联合体2023-2024学年高二上学期第三十七届基础年段期末联考化学试题湖南省长郡中学2023-2024学年高二下学期寒假检测(开学考试)化学试题湖北省武汉西藏中学2023-2024学年高二下学期4月月考化学试题(已下线)猜想01 原子结构与性质 【考题猜想】(8大题型)-2023-2024学年高二化学下学期期末考点大串讲(人教版2019)
3 . 在元素周期表中除了同族元素的性质相似外,还有一些处于对角线上的元素的性质也呈现相似性。例如Li和Mg、Be和Al、B和Si,这种相似关系称为对角线关系,也称对角线规则。回答下列问题:
(1)Ge与Si同主族,二者属于周期表中____________ 区元素;Ge能与NaOH溶液反应生成Na2GeO3,其中发生反应的化学方程式为_____________ 。
(2)基态Mg原子和基态A1原子中第一电离能较大的是___________ ,原因为____________ 。
(3)硼氢化钠(NaBH4)是有机合成中常用的还原剂。
①硼氢化钠中存在的化学键为_____________ (填标号)。
a.离子键 c.氢键 b.共价键 d.配位键
②_____________ gNaBH4的还原能力与标准状况下22.4LH2的还原能力相当(还原能力即生成失去电子的量)。
(4)半径:Mg2+____________ Al3+(填“>”或“<”),若某溶液中的金属阳离子只含Mg2+或Al3+,验证金属离子的方法及现象为____________ 。
(1)Ge与Si同主族,二者属于周期表中
(2)基态Mg原子和基态A1原子中第一电离能较大的是
(3)硼氢化钠(NaBH4)是有机合成中常用的还原剂。
①硼氢化钠中存在的化学键为
a.离子键 c.氢键 b.共价键 d.配位键
②
(4)半径:Mg2+
您最近一年使用:0次
解题方法
4 . X、Y、Z、W、R五种前20号主族元素,原子序数依次增大。基态X原子中有3个未成对的电子,Z是元素周期表中电负性最大的元素,Y和W同主族,常温下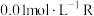 的最高价氧化物对应的水化物溶液的
的最高价氧化物对应的水化物溶液的 。下列说法不正确的是
。下列说法不正确的是
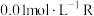 的最高价氧化物对应的水化物溶液的
的最高价氧化物对应的水化物溶液的 。下列说法不正确的是
。下列说法不正确的是A.简单离子半径: | B.简单氢化物的沸点:Y>Z>X |
C.第一电离能: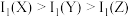 | D.简单氢化物的键角:Y>W |
您最近一年使用:0次
5 . 某研究小组为探究元素周期表中元素性质的递变规律,设计了如下实验:
Ⅰ.验证同周期元素性质的变化规律
(1)将Na、Mg、Al分别投入足量0.05mol/L盐酸中,实验结果:钠与盐酸反应最剧烈;Na、Mg、Al中第一电离能由小到大的顺序是_____ 。
(2)以镁为例,随着反应的进行,化学反应速率是先加快后减慢,分析先加快的主要原因可能是(不考虑固体质量的减少对反应速率的影响,填序号)_____。
(3)将某铝的氯化物加热,180℃时开始升华;500K和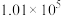 Pa时,它的蒸气密度(换算成标准状况)是
Pa时,它的蒸气密度(换算成标准状况)是 密度的133.5倍。则该铝的氯化物的结构式是
密度的133.5倍。则该铝的氯化物的结构式是_____ 。
Ⅱ.验证同主族元素非金属性的变化规律。
用如图所示装置进行实验(夹持仪器已略去,装置气密性良好),证明卤族元素的非金属性强弱,实验步骤如下:
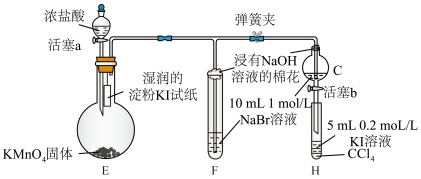
ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸;
ⅱ.当F和G中的溶液都变为黄色时,夹紧弹簧夹;
ⅲ.当F中溶液由黄色变为棕红色时,关闭活塞a;
ⅳ.……
(4)溴的原子结构示意图为_____ 。
(5)A中发生反应生成氯气,请写出该反应的化学反应方程式:_____ 。
(6)为证明非金属性Br>I,过程ⅳ的操作和现象_____ 。
(7)过程G实验的目的是_____ 。
Ⅰ.验证同周期元素性质的变化规律
(1)将Na、Mg、Al分别投入足量0.05mol/L盐酸中,实验结果:钠与盐酸反应最剧烈;Na、Mg、Al中第一电离能由小到大的顺序是
(2)以镁为例,随着反应的进行,化学反应速率是先加快后减慢,分析先加快的主要原因可能是(不考虑固体质量的减少对反应速率的影响,填序号)_____。
| A.该反应是放热反应 |
| B.该反应是吸热反应 |
| C.温度升高对化学反应速率的影响,大于盐酸浓度降低对速率的影响 |
| D.温度升高对化学反应速率的影响,小于盐酸浓度降低对速率的影响 |
(3)将某铝的氯化物加热,180℃时开始升华;500K和
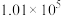 Pa时,它的蒸气密度(换算成标准状况)是
Pa时,它的蒸气密度(换算成标准状况)是 密度的133.5倍。则该铝的氯化物的结构式是
密度的133.5倍。则该铝的氯化物的结构式是Ⅱ.验证同主族元素非金属性的变化规律。
用如图所示装置进行实验(夹持仪器已略去,装置气密性良好),证明卤族元素的非金属性强弱,实验步骤如下:

ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸;
ⅱ.当F和G中的溶液都变为黄色时,夹紧弹簧夹;
ⅲ.当F中溶液由黄色变为棕红色时,关闭活塞a;
ⅳ.……
(4)溴的原子结构示意图为
(5)A中发生反应生成氯气,请写出该反应的化学反应方程式:
(6)为证明非金属性Br>I,过程ⅳ的操作和现象
(7)过程G实验的目的是
您最近一年使用:0次
名校
解题方法
6 . X、Y、Z、Q、W五种元素原子序数依次增大,分布在前四周期,Y、Z、Q是构成地壳的主要元素,Z、Q同周期并相邻,基态W原子的核外电子恰好填满10个原子轨道,由这五种元素构成的某天然结晶水合物的化学式为W[Z2Q3Y10]•3X2Y。下列叙述正确的是
| A.第一电离能:Y>Q>Z>W | B.X与Y形成的粒子中一定不含配位键 |
| C.Q、W单质的晶体类型相同 | D.Z的最高价氧化物对应的水化物是强酸 |
您最近一年使用:0次
7 . 已知X、Y、Z、W、R均是短周期主族元素,X和Z同主族,Y、Z、W、R同周期,W的简单氢化物可用作制冷剂。它们组成的某种化合物的结构如图所示。下列叙述正确的是
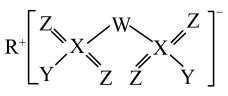

| A.第一电离能:Y>Z>W |
| B.简单离子半径:R<W<Y<Z |
| C.W的简单氢化物的空间结构为三角锥形 |
D. 能使滴有酚酞的氢氧化钠溶液褪色,体现了其漂白性 能使滴有酚酞的氢氧化钠溶液褪色,体现了其漂白性 |
您最近一年使用:0次
名校
8 . X、Y、Z、W、R属于元素周期表中前20号主族元素,且原子序数依次增大。X和Z的基态原子的2p能级上各有两个未成对电子,W与Z同族。R的最外层电子数与最内层电子数相等。下列说法正确的是
| A.简单离子半径:R>W>Z |
| B.简单气态氢化物的热稳定性:W>Z |
| C.元素第一电离能:I1(Y)>I1(Z)>I1(W) |
| D.最高价氧化物对应水化物的酸性:X>W |
您最近一年使用:0次
2023-11-07更新
|
718次组卷
|
4卷引用:辽宁省沈阳市重点高中联合体2023-2024学年高三上学期11月期中化学试题
辽宁省沈阳市重点高中联合体2023-2024学年高三上学期11月期中化学试题(已下线)选择题6-10吉林省通化市梅河口市第五中学2023-2024学年高三上学期11月期中化学试题(已下线)题型01 元素位-构-性推断-2024年高考化学答题技巧与模板构建
名校
9 . 某元素X的一种核素俘获一个氦核后放出氘原子: 下列说法错误的是
下列说法错误的是
 下列说法错误的是
下列说法错误的是| A.X比Y少1个中子 |
| B.第一电离能X小于Y |
| C.X和Y的氢化物中可能既有极性键又有非极性键 |
| D.X的氧化物和其简单氢化物发生反应可以得到X单质 |
您最近一年使用:0次
2023-10-02更新
|
39次组卷
|
2卷引用:辽宁省鞍山市普通高中2022-2023学年高三上学期期中测试化学(A)试题
名校
解题方法
10 . 我国已经形成对全球稀土产业链的统治力,在稀土开采技术方面,我国遥遥领先。同时也是最早研究稀土—钴化合物结构的国家。请回答下列问题:
(1)钴原子的价层电子排布图为___________ ,其M层上有___________ 种不同的空间运动状态,Fe和Co的第四电离能I4(Fe)___________ I4(Co)(填“>”、“<”或“=”)。
(2)为某含钴配合物的组成为CoCl3·5NH3·H2O,是该配合物中钴离子的配位数是6,1mol该配合物可以与足量的硝酸银反应生成3molAgCl沉淀,则该配合物的配体是___________ ,试判断NH3分子与钴离子形成配合物后,H—N—H键角会___________ (填“变大”、“变小”或“不变”)。
(3)具有双钙钛矿型结构的晶体通过掺杂改性可用作固体电解质材料。双钙钛矿型晶体的一种典型结构单元如图所示:

①该晶体的一个完整晶胞中含有___________ 个 原子。
原子。
②真实的晶体中存在5%的O原子缺陷,从而能让 在其中传导,已知
在其中传导,已知 为
为 价,
价, 为
为 价,则
价,则 价
价 与
与 价
价 的原子个数比为
的原子个数比为___________ 。
II.下图为石墨和石墨烯的结构示意图,石墨烯是从石墨材料中剥离出来,由碳原子组成的只有一层原子厚度的二维晶体。

(4)下列关于石墨与石墨烯的说法正确的是___________ 。
A.从石墨中剥离石墨烯需要破坏化学键
B.石墨中的碳原子采取 杂化
杂化
C.石墨属于混合型晶体,层与层之间存在分子间作用力
D.层内碳原子间存在共价键
E.石墨烯中平均每个六元碳环含有3个碳原子
(1)钴原子的价层电子排布图为
(2)为某含钴配合物的组成为CoCl3·5NH3·H2O,是该配合物中钴离子的配位数是6,1mol该配合物可以与足量的硝酸银反应生成3molAgCl沉淀,则该配合物的配体是
(3)具有双钙钛矿型结构的晶体通过掺杂改性可用作固体电解质材料。双钙钛矿型晶体的一种典型结构单元如图所示:

①该晶体的一个完整晶胞中含有
 原子。
原子。②真实的晶体中存在5%的O原子缺陷,从而能让
 在其中传导,已知
在其中传导,已知 为
为 价,
价, 为
为 价,则
价,则 价
价 与
与 价
价 的原子个数比为
的原子个数比为II.下图为石墨和石墨烯的结构示意图,石墨烯是从石墨材料中剥离出来,由碳原子组成的只有一层原子厚度的二维晶体。

(4)下列关于石墨与石墨烯的说法正确的是
A.从石墨中剥离石墨烯需要破坏化学键
B.石墨中的碳原子采取
 杂化
杂化C.石墨属于混合型晶体,层与层之间存在分子间作用力
D.层内碳原子间存在共价键
E.石墨烯中平均每个六元碳环含有3个碳原子
您最近一年使用:0次



