名校
1 . 氨硼烷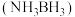 具有含氢量高,热稳定性好的特点,是一种具有潜力的固体储氢材料,回答下列问题。
具有含氢量高,热稳定性好的特点,是一种具有潜力的固体储氢材料,回答下列问题。
(1)基态N原子核外电子占据的最高能级的电子云轮廓图为___________ 形,基态N原子的轨道表示式为___________ 。
(2)已知 的第一电离能
的第一电离能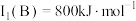 ,判断
,判断
___________ (填“>”或“<”) ,从核外电子排布的角度说明理由:
,从核外电子排布的角度说明理由:___________
(3) 分子中,与
分子中,与 原子相连的
原子相连的 原子对键合电子的吸引力小于
原子对键合电子的吸引力小于 原子,与
原子,与 原子相连的
原子相连的 原子对键合电子的吸引力大于
原子对键合电子的吸引力大于 原子。则在
原子。则在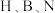 三种元素中:
三种元素中:
①电负性大小顺序是___________ (用元素符号表示,下同);
②原子半径大小顺序是___________ ;
③在元素周期表中的分区与其他两种元素不同的是___________ ;
(4)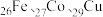 是目前氨硼烷水解产氢催化剂的研究热点。不同催化剂催化氨硼烷水解产氢的性能如图所示。
是目前氨硼烷水解产氢催化剂的研究热点。不同催化剂催化氨硼烷水解产氢的性能如图所示。___________ ,催化效果最差的金属的基态原子的价层电子排布式为___________ 。
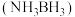 具有含氢量高,热稳定性好的特点,是一种具有潜力的固体储氢材料,回答下列问题。
具有含氢量高,热稳定性好的特点,是一种具有潜力的固体储氢材料,回答下列问题。(1)基态N原子核外电子占据的最高能级的电子云轮廓图为
(2)已知
 的第一电离能
的第一电离能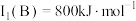 ,判断
,判断
 ,从核外电子排布的角度说明理由:
,从核外电子排布的角度说明理由:(3)
 分子中,与
分子中,与 原子相连的
原子相连的 原子对键合电子的吸引力小于
原子对键合电子的吸引力小于 原子,与
原子,与 原子相连的
原子相连的 原子对键合电子的吸引力大于
原子对键合电子的吸引力大于 原子。则在
原子。则在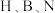 三种元素中:
三种元素中:①电负性大小顺序是
②原子半径大小顺序是
③在元素周期表中的分区与其他两种元素不同的是
(4)
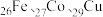 是目前氨硼烷水解产氢催化剂的研究热点。不同催化剂催化氨硼烷水解产氢的性能如图所示。
是目前氨硼烷水解产氢催化剂的研究热点。不同催化剂催化氨硼烷水解产氢的性能如图所示。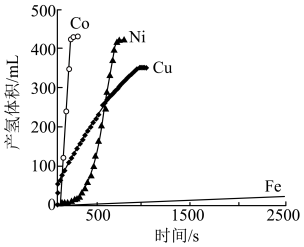
您最近一年使用:0次
名校
解题方法
2 . 七水硫酸亚铁,俗称绿矾,化学式为 ,能制造多种工业产品,其结构示意图如下。下列说法不正确的是
,能制造多种工业产品,其结构示意图如下。下列说法不正确的是
 ,能制造多种工业产品,其结构示意图如下。下列说法不正确的是
,能制造多种工业产品,其结构示意图如下。下列说法不正确的是
| A.第一电离能:O>S>Fe |
B. 的配位数为6 的配位数为6 |
C.气态基态 再失去一个电子比气态基态 再失去一个电子比气态基态 更难 更难 |
D. 中存在的作用力有离子键、极性键、配位键、氢键 中存在的作用力有离子键、极性键、配位键、氢键 |
您最近一年使用:0次
名校
解题方法
3 . 关于物质的结构与性质,下列说法正确的个数为
①p能级能量一定比s能级的能量高
②电负性越大,元素的非金属性越强,第一电离能也越大
③所有的σ键的强度都比π键的大
④可燃冰( )中甲烷分子与水分子间形成了氢键
)中甲烷分子与水分子间形成了氢键
⑤利用“杯酚”可分离 和
和 ,反映出超分子具有“分子识别”的特征
,反映出超分子具有“分子识别”的特征
⑥卤素单质、卤素氢化物、卤素碳化物(即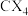 )的熔、沸点均随着相对分子质量的增大而升高
)的熔、沸点均随着相对分子质量的增大而升高
①p能级能量一定比s能级的能量高
②电负性越大,元素的非金属性越强,第一电离能也越大
③所有的σ键的强度都比π键的大
④可燃冰(
 )中甲烷分子与水分子间形成了氢键
)中甲烷分子与水分子间形成了氢键⑤利用“杯酚”可分离
 和
和 ,反映出超分子具有“分子识别”的特征
,反映出超分子具有“分子识别”的特征⑥卤素单质、卤素氢化物、卤素碳化物(即
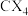 )的熔、沸点均随着相对分子质量的增大而升高
)的熔、沸点均随着相对分子质量的增大而升高| A.1个 | B.2个 | C.3个 | D.4个 |
您最近一年使用:0次
名校
4 . 钠、镁、铝、铜及其化合物在生活中具有重要作用。回答下列问题:
(1)基态 的价层轨道表示式为
的价层轨道表示式为________ 。
(2)Na、Mg、Al的第一电离能从小到大的顺序为_______ (填元素符号)。
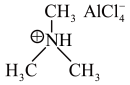
(3)铝离子电池一般采用离子液体作为电解质,某含铝离子液体的结构如图:_______ ;传统的有机溶剂大多易挥发,而离子液体相对难挥发,原因是________ 。
(4)几种氧化物的化学键中离子键成分的百分数和氧化物的熔点如下表:
离子键成分的百分数:MgO高于 ,其原因是
,其原因是_______ 。
(5)氮、铜形成的某一种化合物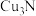 ,为立方晶系晶体,晶胞中氮原子只有一种位置,沿体对角线投影如图甲所示。
,为立方晶系晶体,晶胞中氮原子只有一种位置,沿体对角线投影如图甲所示。___ 个,请在图乙中画出该晶胞的结构示意图____ (○为N,●为Cu)已知晶胞中最近的两个Cu原子间距离为a pm,则晶体的密度为_____  (用含a、
(用含a、 的代数式表示)。
的代数式表示)。
(1)基态
 的价层轨道表示式为
的价层轨道表示式为(2)Na、Mg、Al的第一电离能从小到大的顺序为
(3)铝离子电池一般采用离子液体作为电解质,某含铝离子液体的结构如图:
(4)几种氧化物的化学键中离子键成分的百分数和氧化物的熔点如下表:
| 氧化物 |  | MgO |  |
| 离子键的百分数/% | 62 | 50 | 41 |
| 熔点/℃ | 1132 | 2852 | 2054 |
 ,其原因是
,其原因是(5)氮、铜形成的某一种化合物
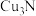 ,为立方晶系晶体,晶胞中氮原子只有一种位置,沿体对角线投影如图甲所示。
,为立方晶系晶体,晶胞中氮原子只有一种位置,沿体对角线投影如图甲所示。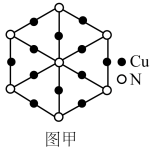
 (用含a、
(用含a、 的代数式表示)。
的代数式表示)。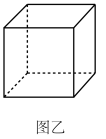
您最近一年使用:0次
名校
5 . 某种钾盐具有鲜艳的颜色,其阴离子结构如图所示。X、Y、Z、W为原子序数依次增加的前四周期元素,X、Y在第二周期且未成对电子数之比为2∶3,Z的最高化合价与最低化合价的代数和为4,W为日常生活中应用最广泛的过渡金属。下列说法正确的是

| A.W的化合价为+2 | B.第一电离能X>Y>Z>W |
| C.X的氢化物的沸点低于Y的氢化物 | D.Y、Z的氧化物大量排放会导致酸雨 |
您最近一年使用:0次
名校
解题方法
6 . W、X、Y、Z为同一短周期的元素,且原子序数依次增加。其中X、Y、Z相邻,W的核外电子数与X的价层电子数相等,Z2是氧化性最强的单质,X的最简单气态氢化物与其最高价氧化物对应的水化物可以反应生成一种常见的盐。下列说法正确的是
| A.分子的极性:WZ3<XZ3 | B.第一电离能:X<Y<Z |
| C.元素的电负性:Y>Z | D.键能:X2<Y2<Z2 |
您最近一年使用:0次
名校
7 . 回答以下关于元素及其化合物的问题.
(1)下列状态的铝中,最外层电离出一个电子所需要能量由大到小的顺序______________ (填标号)。______________ ,基态氧原子的价层电子不是重排结构,原因是不符合______________ 。
(3)下图中分别代表了碳单质的两种常见晶体,碳元素位于元素周期表的______________ 区;图1晶体中1个最小六元环平均含有C原子数与图2晶体中1个最小六元环平均含有C原子数之比为______________ ;图3是石墨层间插入氟得到层状结构化合物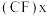 ,该物质仍具润滑性,与石墨相比,
,该物质仍具润滑性,与石墨相比,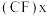 导电性
导电性______________ (填“增强”或“减弱”)。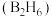 、丁硼烷
、丁硼烷 等.乙硼烷的结构式如图
等.乙硼烷的结构式如图 。分子中B原子通过氢桥键(
。分子中B原子通过氢桥键(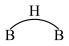 )形成一个四元环。丁硼烷
)形成一个四元环。丁硼烷 分子中存在4个氢桥键且有两个五元环,写出其结构式
分子中存在4个氢桥键且有两个五元环,写出其结构式______________ 。
(1)下列状态的铝中,最外层电离出一个电子所需要能量由大到小的顺序
A.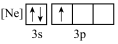 B.
B.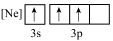 C.
C.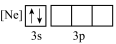 D.
D.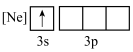
(3)下图中分别代表了碳单质的两种常见晶体,碳元素位于元素周期表的
 ,该物质仍具润滑性,与石墨相比,
,该物质仍具润滑性,与石墨相比, 导电性
导电性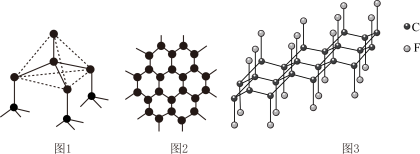
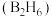 、丁硼烷
、丁硼烷 等.乙硼烷的结构式如图
等.乙硼烷的结构式如图 。分子中B原子通过氢桥键(
。分子中B原子通过氢桥键( )形成一个四元环。丁硼烷
)形成一个四元环。丁硼烷 分子中存在4个氢桥键且有两个五元环,写出其结构式
分子中存在4个氢桥键且有两个五元环,写出其结构式
您最近一年使用:0次
名校
8 . 我国科学家发现一种能用于“点击反应”的新分子,结构如下图所示。其中X、Y、Z和W是原子序数依次增大的短周期主族元素,Y与Z是同一主族元素。下列说法正确的是

| A.简单离子半径:W>Z>Y>X | B.第一电离能:Y>X>Z>W |
| C.简单氢化物的沸点:Y>X>Z | D. 分子中键角均为120° 分子中键角均为120° |
您最近一年使用:0次
2023-12-26更新
|
315次组卷
|
2卷引用:湖北省武汉市华中师范大学第一附属中学2023-2024学年高三上学期11月期中考试化学试题
名校
9 . 一种可用于头孢菌素改性剂的结构如下图所示,其中X、Y、Z、W是原子序数递增的短周期主族元素。下列说法不正确 的是
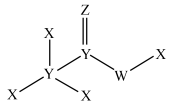

A.键角: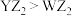 | B.第一电离能: |
C.沸点: | D.离子半径: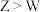 |
您最近一年使用:0次
10 . “嫦娥石”是中国首次在月球上发现的新矿物,其主要由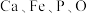 和
和 (钇,原子序数比
(钇,原子序数比 大13)组成,下列说法正确的是
大13)组成,下列说法正确的是
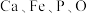 和
和 (钇,原子序数比
(钇,原子序数比 大13)组成,下列说法正确的是
大13)组成,下列说法正确的是| A.Y位于元素周期表的第ⅢB族 |
B.基态 原子的核外电子填充在6个轨道中 原子的核外电子填充在6个轨道中 |
C.5种元素中,第一电离能最小的是 |
D.5种元素中,电负性最大的是 |
您最近一年使用:0次
2023-09-28更新
|
4538次组卷
|
6卷引用:湖北省武汉市华中师范大学第一附属中学2023-2024学年高一下学期4月期中考试化学试题
湖北省武汉市华中师范大学第一附属中学2023-2024学年高一下学期4月期中考试化学试题江苏省淮安市高中校协作体2023-2024学年高三上学期期中联考化学试题2023年重庆市高考化学试卷(已下线)选择题6-10(已下线)题型20 物质结构与性质基础-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)山东省东营市第一中学2023-2024学年高二下学期开学收心考试化学试题



