名校
解题方法
1 . 下列说法中,正确的是
| A.N、P、S的第一电离能依次减小 | B.Li、Na、K的电负性依次增大 |
| C.F、O、Na的原子半径依次减小 | D.甲烷、氨气、水的键角依次增大 |
您最近半年使用:0次
2 . 按要求回答下列问题:
(1)下列B原子的电子排布式的状态中,能量最高的是________(用字母表示)。
(2)锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛,回答下列问题:
①基态Ge原子的简化的电子排布式为________ ,基态原子核外有________ 种空间运动状态。
②比较下列锗卤化物的熔点和沸点,分析呈现该变化规律的原因是________________________________ 。
③光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是________________ 。
(3)Na与N形成的NaN3可用于制造汽车的安全气囊,其中阴离子 的空间构型为
的空间构型为________ ,Na在空气中燃烧则发出黄色火焰,这种黄色焰色用光谱仪摄取的光谱为________ 光谱(填“发射”或“吸收”)。
(4)元素镍与镍钴合金的晶胞结构分别如图a、b所示:
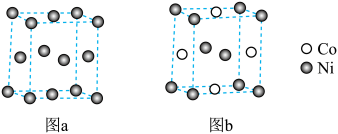
①镍钴合金若写作NixCo1-x,则图b合金中x=________
②已知晶胞(图a)的边长为m pm,设NA为阿伏加德罗常数的值,则镍的密度为________ g/cm3(列出计算式)。
(1)下列B原子的电子排布式的状态中,能量最高的是________(用字母表示)。
A. | B.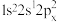 | C. | D.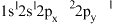 |
(2)锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛,回答下列问题:
①基态Ge原子的简化的电子排布式为
②比较下列锗卤化物的熔点和沸点,分析呈现该变化规律的原因是
| GeCl4 | GeBr4 | GeI4 | |
| 熔点/℃ | -49.5 | 26 | 146 |
| 沸点/℃ | 83.1 | 186 | 约400 |
(3)Na与N形成的NaN3可用于制造汽车的安全气囊,其中阴离子
 的空间构型为
的空间构型为(4)元素镍与镍钴合金的晶胞结构分别如图a、b所示:

①镍钴合金若写作NixCo1-x,则图b合金中x=
②已知晶胞(图a)的边长为m pm,设NA为阿伏加德罗常数的值,则镍的密度为
您最近半年使用:0次
名校
解题方法
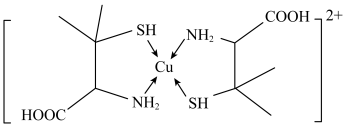
3 . 青霉胺可以用于医学上误食铜盐的解毒,解毒原理: 形成环状配合物,其结构如图所示。该配合物无毒、易溶于水,可经尿液排出。下列说法正确的是
形成环状配合物,其结构如图所示。该配合物无毒、易溶于水,可经尿液排出。下列说法正确的是
 形成环状配合物,其结构如图所示。该配合物无毒、易溶于水,可经尿液排出。下列说法正确的是
形成环状配合物,其结构如图所示。该配合物无毒、易溶于水,可经尿液排出。下列说法正确的是
A.共价键键角的大小关系为: |
B.电负性大小关系为: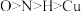 |
| C.该配合物易溶于水的主要原因是其与水可形成分子间氢键 |
D.与铜离子形成配位键强弱的大小关系为: |
您最近半年使用:0次
名校
4 . 类比推理是学习化学的重要的思维方法,下列陈述I及类比推理陈述Ⅱ均正确的是
| 选项 | 陈述I | 类比推理陈述II |
| A | 在空气中加热, 生成 生成 | 在空气中加热, 也生成 也生成 |
| B | 酸性: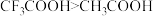 | 碱性: |
| C |  是强酸 是强酸 |  也是强酸 也是强酸 |
| D | 通入 可增强漂白粉溶液漂白性 可增强漂白粉溶液漂白性 | 通入 也可增强漂白粉溶液漂白性 也可增强漂白粉溶液漂白性 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
5 . X、Y、Z、W四种短周期主族元素,原子序数依次增大。X、Y与Z位于同一周期,且只有X、Y元素相邻,X基态原子核外有2个未成对电子,W原子在同周期中原子半径最大。下列说法不正确 的是
A.第一电离能: |
B.电负性: |
C.Z、W原子形成稀有气体电子构型的简单离子的半径: |
D.Y与Z形成的分子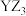 中每个原子均满足 中每个原子均满足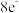 结构 结构 |
您最近半年使用:0次
2024-01-09更新
|
446次组卷
|
3卷引用:海南省农垦中学2023-2024学年高二上学期期中检测化学试题
名校
6 . 法匹拉韦是治疗新冠肺炎的一种药物,其结构简式如图所示。下列说法正确的是


A.该分子的分子式为 |
B.该分子中相邻C原子之间均以 杂化轨道重叠形成σ键 杂化轨道重叠形成σ键 |
| C.组成该分子的所有元素中氟的电负性最大 |
| D.该分子中有2个手性碳原子 |
您最近半年使用:0次
7 . 下图是元素周期表的一部分,图中所列字母分别代表一种化学元素。回答下列问题:

(1)j元素基态原子的电子排布式是___________ 。
(2)元素k位于周期表中___________ 区,其基态原子有___________ 个未成对电子,有___________ 种空间运动状态不同的电子。
(3)下列正确的是___________。
(4)基态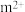 的离子结构示意图为
的离子结构示意图为___________ ,已知高温下化合物 比化合物
比化合物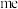 更稳定,试从
更稳定,试从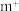 离子的核外电子排布的角度解释原因
离子的核外电子排布的角度解释原因___________ 。
(5)根据对角线规则,b与h的化学性质相似,请写出b的最高价氧化物对应的水化物与 溶液反应的离子方程式
溶液反应的离子方程式___________ 。
(6)传闻某国合成了第166号元素,若已知原子结构规律不变,该元素应是第___________ 周期、第___________ 族。

(1)j元素基态原子的电子排布式是
(2)元素k位于周期表中
(3)下列正确的是___________。
A.原子半径 | B.第一电离能 |
C.电负性 | D.最高价氧化物的水化物的酸性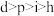 |
(4)基态
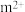 的离子结构示意图为
的离子结构示意图为 比化合物
比化合物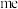 更稳定,试从
更稳定,试从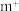 离子的核外电子排布的角度解释原因
离子的核外电子排布的角度解释原因(5)根据对角线规则,b与h的化学性质相似,请写出b的最高价氧化物对应的水化物与
 溶液反应的离子方程式
溶液反应的离子方程式(6)传闻某国合成了第166号元素,若已知原子结构规律不变,该元素应是第
您最近半年使用:0次
名校
解题方法
8 . C和Si元素在化学中占有极其重要的地位。
(1)写出Si的基态原子核外最外层电子排布式______ ,C、O、Si三种元素的电负性由大到小的顺序为______ 。
(2)干冰是分子晶体,其密度比冰大的原因是____________ 。
(3)氧化物XO的电子总数与SiC的相等,则X为______ (填元素符号),XO是优良的耐高温材料,其熔点比CaO高的原因是__________________ 。
(4)在30 g 晶体中含
晶体中含______ mol Si-O键。
(1)写出Si的基态原子核外最外层电子排布式
(2)干冰是分子晶体,其密度比冰大的原因是
(3)氧化物XO的电子总数与SiC的相等,则X为
(4)在30 g
 晶体中含
晶体中含
您最近半年使用:0次
名校
解题方法
9 . 按要求填空。
(1)一个基态原子电子排布为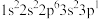 的元素最可能的价态是
的元素最可能的价态是___________ ;某元素原子的 原子轨道中有3个未成对电子,则该原子的
原子轨道中有3个未成对电子,则该原子的价电子轨道表示式 为___________ 。
(2)第四周期中,未成对电子数目最多的元素是___________ ;价层电子排布式为 的基态原子的原子结构示意图
的基态原子的原子结构示意图___________ 。
(3)元素周期表中能稳定存在且电负性相差最大的两种元素形成的化合物的化学式为_______ 。
(4) 三种短周期元素的原子序数
三种短周期元素的原子序数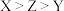 ,X和Z原子核外s电子与p电子数之比都为
,X和Z原子核外s电子与p电子数之比都为 ,Y原子最外层s电子与p电子数之比为
,Y原子最外层s电子与p电子数之比为 ,
,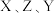 三者所形成的常见化合物的化学式为
三者所形成的常见化合物的化学式为_____ 。
(1)一个基态原子电子排布为
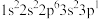 的元素最可能的价态是
的元素最可能的价态是 原子轨道中有3个未成对电子,则该原子的
原子轨道中有3个未成对电子,则该原子的(2)第四周期中,未成对电子数目最多的元素是
 的基态原子的原子结构示意图
的基态原子的原子结构示意图(3)元素周期表中能稳定存在且电负性相差最大的两种元素形成的化合物的化学式为
(4)
 三种短周期元素的原子序数
三种短周期元素的原子序数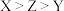 ,X和Z原子核外s电子与p电子数之比都为
,X和Z原子核外s电子与p电子数之比都为 ,Y原子最外层s电子与p电子数之比为
,Y原子最外层s电子与p电子数之比为 ,
,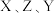 三者所形成的常见化合物的化学式为
三者所形成的常见化合物的化学式为
您最近半年使用:0次
名校
10 . X、Y、Z、W是元素周期表前四周期中的常见元素,其相关信息如表。下列说法错误的是
| 元素 | 相关信息 |
 |  的基态原子 的基态原子 层电子数是 层电子数是 层的2倍 层的2倍 |
 |  的基态原子最外层电子排布式为 的基态原子最外层电子排布式为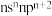 |
 |  存在质量数为23、中子数为12的核素 存在质量数为23、中子数为12的核素 |
 | W有多种化合价,其白色氢氧化物在空气中会迅速变成灰绿色,最后变成红褐色 |
A.W是 元素 元素 | B. 的电负性比 的电负性比 的大 的大 |
C. 中阴离子和阳离子个数比为 中阴离子和阳离子个数比为 | D. 是一种直线形分子 是一种直线形分子 |
您最近半年使用:0次



