1 . 下列有关说法正确的是
A.第一电离能: |
B.键角: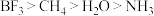 |
C.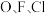 电负性由大到小的顺序为 电负性由大到小的顺序为 |
D. 溶于水和干冰升华都只有分子间作用力改变 溶于水和干冰升华都只有分子间作用力改变 |
您最近一年使用:0次
名校
2 . 氢键对生命活动具有重要意义。DNA中四种碱基间的配对方式如下图。(~ 代表糖苷键)
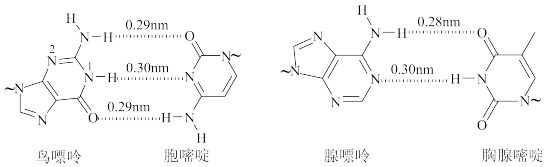
请回答下列问题:
(1)基态N的核外电子排布式为___________ ;N和O第一电离能较大的是___________ 。
(2)①碱基中的-NH2具有一定的碱性,可以结合H+形成-NH ,从结构角度解释可以结合的原因:
,从结构角度解释可以结合的原因:___________ 。
②写出甘氨酸(H2NCH2COOH)在pH=1和pH=13时的粒子存在形态:pH=1时___________ ,pH=13时___________ 。
(3)鸟嘌呤是一种常见的碱基。
①鸟嘌呤中2号N的杂化类型为___________ 。
②鸟嘌呤中N-H键的平均键长___________ (填“大于”“小于”或“等于”)0.29nm。
(4)氢键在DNA复制过程中起重要作用。
①碱基中,O、N能与H形成氢键而C不能,原因是___________ 。
②下列说法正确的是___________ (填序号)。
a.氢键的强度较小,在DNA解旋和复制时容易断裂和形成
b.鸟嘌呤与胞嘧啶之间的相互作用比鸟嘌呤与胸腺嘧啶之间的更强
c.碱基配对时,一个H可以同时与多个原子形成氢键
d.DNA在形成双螺旋结构时,碱基遵循互补配对原则,形成的氢键多,结构更稳定
(5)一定条件下鸟嘌呤会发生异构化,其1号N上的H会转移到O上形成-OH。
①鸟嘌呤异构化后的结构简式为___________ 。
②鸟嘌呤异构化后最有可能配对的嘧啶碱基是___________ 。

请回答下列问题:
(1)基态N的核外电子排布式为
(2)①碱基中的-NH2具有一定的碱性,可以结合H+形成-NH
 ,从结构角度解释可以结合的原因:
,从结构角度解释可以结合的原因:②写出甘氨酸(H2NCH2COOH)在pH=1和pH=13时的粒子存在形态:pH=1时
(3)鸟嘌呤是一种常见的碱基。
①鸟嘌呤中2号N的杂化类型为
②鸟嘌呤中N-H键的平均键长
(4)氢键在DNA复制过程中起重要作用。
①碱基中,O、N能与H形成氢键而C不能,原因是
②下列说法正确的是
a.氢键的强度较小,在DNA解旋和复制时容易断裂和形成
b.鸟嘌呤与胞嘧啶之间的相互作用比鸟嘌呤与胸腺嘧啶之间的更强
c.碱基配对时,一个H可以同时与多个原子形成氢键
d.DNA在形成双螺旋结构时,碱基遵循互补配对原则,形成的氢键多,结构更稳定
(5)一定条件下鸟嘌呤会发生异构化,其1号N上的H会转移到O上形成-OH。
①鸟嘌呤异构化后的结构简式为
②鸟嘌呤异构化后最有可能配对的嘧啶碱基是
您最近一年使用:0次
3 . 元素N、O、F的某些性质随核电荷数的变化趋势如图所示。下列图示不正确的是
A. | B. |
C. | D. |
您最近一年使用:0次
解题方法
4 . 下列说法正确的是
| A.元素的第一电离能越大,其金属性一定越强 |
| B.元素的第一电离能越小,其金属性一定越强 |
| C.同主族元素的单质从上到下,熔点升高 |
| D.一般情况下,金属单质与酸反应越容易,其元素的电负性越小 |
您最近一年使用:0次
5 . 现有三种元素的基态原子的电子排布式如下:①1s22s22p63s23p4;②1s22s22p63s23p3;③1s22s22p63s23p5,下列排序正确的是
| A.含氧酸的酸性:③>①>② | B.原子半径:③>②>① |
| C.第一电离能:③>②>① | D.电负性:③>②>① |
您最近一年使用:0次
解题方法
6 . 立方氮化硼硬度高,耐磨性好,在机械加工行业有广泛应用。制备立方氮化硼的一种方法为BCl3(g)+NH3(g)=BN(s)+3HCl(g),下列说法错误的是
| A.反应混合物中所有化学键均为共价键 |
| B.元素电负性大小为N>B |
| C.BCl3和BN均为共价晶体 |
D.形成BCl3时B原子先激发后杂化,其激发态价电子轨道表示式为: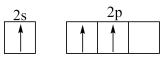 |
您最近一年使用:0次
解题方法
7 . W、X、Y、Z、R是五种短周期主族元素,原子序数依次增大。W元素的一种离子与 具有相同的电子层排布且半径稍大,X原子核外L层的电子数与Y原子核外M层的电子数之比为3:2,X与Z同主族,Z的价层电子排布式为
具有相同的电子层排布且半径稍大,X原子核外L层的电子数与Y原子核外M层的电子数之比为3:2,X与Z同主族,Z的价层电子排布式为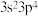 。下列说法错误的是
。下列说法错误的是
 具有相同的电子层排布且半径稍大,X原子核外L层的电子数与Y原子核外M层的电子数之比为3:2,X与Z同主族,Z的价层电子排布式为
具有相同的电子层排布且半径稍大,X原子核外L层的电子数与Y原子核外M层的电子数之比为3:2,X与Z同主族,Z的价层电子排布式为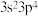 。下列说法错误的是
。下列说法错误的是| A.简单气态氢化物的热稳定性:Z>Y |
| B.W与Li的原子半径:W<Li |
| C.X和Y的第一电离能:X>Y |
| D.X、Z、R的电负性:R<Z<X |
您最近一年使用:0次
解题方法
8 . 化学作为一门基础自然科学,在材料科学、生命科学、能源科学等诸多领域发挥着重要作用。
(1)高温超导材料钇钡铜氧的化学式为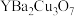 ,其中
,其中 的Cu以罕见的
的Cu以罕见的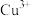 形式存在。按照核外电子排布,把元素周期表划分成5个区,则O在元素周期表中的
形式存在。按照核外电子排布,把元素周期表划分成5个区,则O在元素周期表中的_______ 区,基态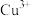 的核外电子排布式为
的核外电子排布式为_______
(2)下列状态的镁中,电离最外层一个电子所需能量最大的是_______。
(3)青蒿素的结构简式如图所示,其组成元素的电负性由大到小的顺序为_______ 。

(1)高温超导材料钇钡铜氧的化学式为
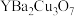 ,其中
,其中 的Cu以罕见的
的Cu以罕见的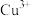 形式存在。按照核外电子排布,把元素周期表划分成5个区,则O在元素周期表中的
形式存在。按照核外电子排布,把元素周期表划分成5个区,则O在元素周期表中的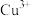 的核外电子排布式为
的核外电子排布式为(2)下列状态的镁中,电离最外层一个电子所需能量最大的是_______。
A.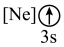 | B.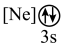 | C.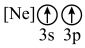 | D.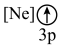 |

您最近一年使用:0次
9 . 现有四种元素的基态原子的核外电子排布式如下:① ;②
;② ;③
;③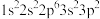 ;④
;④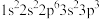 。下列说法错误的是
。下列说法错误的是
 ;②
;② ;③
;③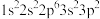 ;④
;④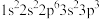 。下列说法错误的是
。下列说法错误的是| A.电负性:②>①>④>③ |
| B.原子半径:③>④>①>② |
| C.简单气态氢化物的稳定性:①>②>③>④ |
| D.第一电离能:①>②>④>③ |
您最近一年使用:0次
2023-01-13更新
|
321次组卷
|
3卷引用:山东省临沂第一中学2021-2022学年高二上学期期末检测化学试题
解题方法
10 . 乙二酸( )俗称草酸,为无色晶体,是二元弱酸,广泛分布于植物、动物和真菌体中,在实验研究和化学工业中应用广泛。乙二酸与氧化剂作用易被氧化成二氧化碳和水,如
)俗称草酸,为无色晶体,是二元弱酸,广泛分布于植物、动物和真菌体中,在实验研究和化学工业中应用广泛。乙二酸与氧化剂作用易被氧化成二氧化碳和水,如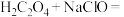
 。下列说法正确的是
。下列说法正确的是
 )俗称草酸,为无色晶体,是二元弱酸,广泛分布于植物、动物和真菌体中,在实验研究和化学工业中应用广泛。乙二酸与氧化剂作用易被氧化成二氧化碳和水,如
)俗称草酸,为无色晶体,是二元弱酸,广泛分布于植物、动物和真菌体中,在实验研究和化学工业中应用广泛。乙二酸与氧化剂作用易被氧化成二氧化碳和水,如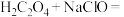
 。下列说法正确的是
。下列说法正确的是A.乙二酸的电离方程式: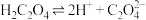 |
| B.电负性:O>Cl>C>H |
C.若基态 原子的电子排布式写为 原子的电子排布式写为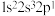 ,则违背了洪特规则 ,则违背了洪特规则 |
D.氧的基态原子的轨道表示式: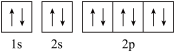 |
您最近一年使用:0次



