1 . 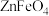 是一种性能优良的软磁材料,也是一种催化剂。工业上利用反应:
是一种性能优良的软磁材料,也是一种催化剂。工业上利用反应: 制备
制备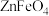 。下列说法错误的是
。下列说法错误的是
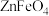 是一种性能优良的软磁材料,也是一种催化剂。工业上利用反应:
是一种性能优良的软磁材料,也是一种催化剂。工业上利用反应: 制备
制备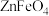 。下列说法错误的是
。下列说法错误的是A.电负性 |
B. 分子中有2个 分子中有2个 键,2个 键,2个 键 键 |
C.基态 的核外电子排布式为 的核外电子排布式为 |
D.基态氧原子中,电子占据的最高能级符号为 |
您最近一年使用:0次
解题方法
2 . 硼的化合物在生产、生活和科研中应用广泛。回答下列问题:
(1)基态硼原子的价电子排布图为:___________ ;B、N、H的电负性由大到小的顺序为___________ 。
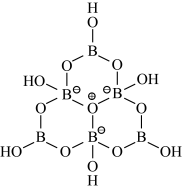
(2)科学家合成了一种含硼阴离子 ,其结构如图所示。其中硼原子的杂化方式为
,其结构如图所示。其中硼原子的杂化方式为___________ ,该结构中共有___________ 种不同化学环境的氧原子。
(3) 与
与 结合形成固态化合物
结合形成固态化合物 ,该物质在
,该物质在 时熔化电离出
时熔化电离出 和一含硼阴离子
和一含硼阴离子___________ (填离子符号); 空间构型为
空间构型为___________ 。
(1)基态硼原子的价电子排布图为:
(2)科学家合成了一种含硼阴离子
 ,其结构如图所示。其中硼原子的杂化方式为
,其结构如图所示。其中硼原子的杂化方式为
(3)
 与
与 结合形成固态化合物
结合形成固态化合物 ,该物质在
,该物质在 时熔化电离出
时熔化电离出 和一含硼阴离子
和一含硼阴离子 空间构型为
空间构型为
您最近一年使用:0次
名校
3 . 碳、硫、氧、氮是中学常见元素,下列说法不正确的是
A. 、 、 、 、 都是直线形分子 都是直线形分子 |
B. 、 、 、 、 的键角依次减小 的键角依次减小 |
C. 、 、 分子的中心原子都是 分子的中心原子都是 化 化 |
| D.C、N、F元素的电负性依次增大 |
您最近一年使用:0次
2023-06-08更新
|
148次组卷
|
5卷引用:福建省三明市四地四校2021-2022学年高二下学期期中联考化学试题
解题方法
4 . 高铁酸钾(K2FeO4)是一种高效绿色水处理剂,工业上可由KClO在碱性条件下氧化Fe(OH)3制得,下列说法正确的是
| A.半径大小:r (Cl-)>r(K+) |
| B.O和Cl的电负性大小: Cl > O |
| C.第一电离能大小: I1(O)< I1(K) |
| D.碱性强弱: KOH < Fe(OH)3 |
您最近一年使用:0次
2022-12-29更新
|
434次组卷
|
2卷引用:江苏省南京市六校联合体2022-2023学年高三上学期11月联考化学试题
5 . 某化学兴趣小组对BeCl2是离子化合物还是共价化合物进行探究,从经验看铍是金属元素,易失去电子,氯是非金属元素,易得到电子。
(1)查表得知,Be的电负性是1.5,Cl的电负性是3.0,则BeCl2应为_______ (填“离子”或“共价”)化合物。
(2)工业上制取BeCl2的方法是将得到的BeCl2溶液在HCl气流中蒸干灼烧,防止BeCl2水解,请写出BeCl2水解的化学方程式:_______ 。
(3)经实验验证,熔融的BeCl2不能导电,说明它是_______ (填“离子”或“共价”)化合物;BeCl2能溶于水,水溶液能导电,是因为它在溶液中能电离,写出它的电离方程式:_______ 。
(4)在周期表中,铍元素和铝元素恰好处于对角线位置,根据对角线法则,BeCl2应与_______ (填“MgCl2”或“AlCl3”)的化学性质更相似。
(5)氢氧化铍能与氢氧化钠溶液发生反应,写出该反应的化学方程式:_______ 。
(1)查表得知,Be的电负性是1.5,Cl的电负性是3.0,则BeCl2应为
(2)工业上制取BeCl2的方法是将得到的BeCl2溶液在HCl气流中蒸干灼烧,防止BeCl2水解,请写出BeCl2水解的化学方程式:
(3)经实验验证,熔融的BeCl2不能导电,说明它是
(4)在周期表中,铍元素和铝元素恰好处于对角线位置,根据对角线法则,BeCl2应与
(5)氢氧化铍能与氢氧化钠溶液发生反应,写出该反应的化学方程式:
您最近一年使用:0次
解题方法
6 . 钙钛矿(CaTiO3)型化合物是一类可用于生产太阳能电池、传感器、固体电阻器等的功能材料,回答下列问题:
(1)基态Ti原子的核外电子排布式为____ 。Ti在元素周期表中的位置____ 。
(2)Ti的四卤化物熔点如表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是____ 。
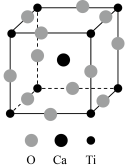
(3)CaTiO3的晶胞如图所示,其组成元素的电负性大小顺序是____ ;金属离子与氧离子间的作用力为____ ,Ca2+的配位数是____ 。
(1)基态Ti原子的核外电子排布式为
(2)Ti的四卤化物熔点如表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是
| 化合物 | TiF4 | TiCl4 | TiBr4 | TiI4 |
| 熔点/℃ | 377 | ﹣24.12 | 38.3 | 155 |
(3)CaTiO3的晶胞如图所示,其组成元素的电负性大小顺序是

您最近一年使用:0次
名校
解题方法
7 . 磷酸氯喹在细胞水平上能有效抑制新型冠状病毒的感染,其结构简式如图所示。下列说法正确的是


| A.电负性: N>O>C |
| B.该有机物中碳原子只采取sp2杂化 |
| C.基态氮原子核外有7种空间运动状态的电子 |
D.PO 的键角大于PO 的键角大于PO 的键角 的键角 |
您最近一年使用:0次
名校
8 . 实验室用KMnO4和浓盐酸制Cl2。下列说法正确的是
| A.半径大小:r(K+)>r(Cl-) | B.电离能大小:I1(K)>I1(Mn) |
| C.电负性大小:x(О)>x(Cl) | D.Mn元素在元素周期表的ds区 |
您最近一年使用:0次
2022-11-29更新
|
457次组卷
|
3卷引用:江苏省徐州市第七中学2022-2023学年高三上学期期中抽测化学试题
江苏省徐州市第七中学2022-2023学年高三上学期期中抽测化学试题江苏省徐州市2022-2023学年高三上学期11月期中考试化学试题(已下线)专题01 原子结构与性质(知识串讲+专题过关)-2022-2023学年高二化学下学期期中期末考点大串讲(人教版2019)
名校
解题方法
9 . 短周期元素X、Y、Z和W的原子序数依次增大。Z的原子序数等于X和Y原子序数之和,X是宇宙中最丰富的元素,XZ用于刻蚀玻璃时生成化合物WZ4。下列说法错误的是
| A.Z的电负性在四种元素中最大 |
| B.X2Y和WY2的中心原子均采用sp3杂化 |
| C.1mol WY2中有2mol W-Y共价键 |
| D.WZ4分子中所有原子最外层均满足8电子结构 |
您最近一年使用:0次
名校
解题方法
10 . 当汽车遭受一定碰撞力量以后,安全气囊中的物质会发生剧烈的反应:NaN3+KNO3=K2O+Na2O+N2↑(未配平),生成大量气体。下列说法正确的是
| A.半径大小:r(Na+)<r(N3-) | B.电负性大小:χ(N)>χ(O) |
| C.电离能大小:I1(Na)>I1(O) | D.碱性强弱:KOH<NaOH |
您最近一年使用:0次
2022-11-27更新
|
245次组卷
|
3卷引用:江苏省南通市海安市2022-2023学年高三上学期11月期中化学试题



