解题方法
1 . ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种化合价,含ⅥA族元素的化合物在研究和生产中有许多重要用途。回答下列问题:
(1)基态O原子电子占据最高能级的电子云轮廓图为_______ 形。
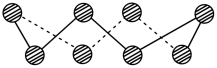
(2)S单质的常见形式为 ,其环状结构如图所示,S原子的杂化轨道类型是
,其环状结构如图所示,S原子的杂化轨道类型是_______ 。
(3)基态Se原子的核外电子排布式为_______ 。
(4)S、Se、Te三种元素电负性由大到小的顺序是_______ ,三种元素氢化物水溶液的酸性最强的是_______ (填化学式)。
(5) 分子中共价键的类型是
分子中共价键的类型是_______ ,常温下 是气体而
是气体而 是液体的原因是
是液体的原因是_______ 。
(6)ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如图所示,S周围紧邻且等距的Zn有_______ 个。晶胞棱长为a pm,密度为_______  (NA表示阿伏加德罗常数的值)。
(NA表示阿伏加德罗常数的值)。

(1)基态O原子电子占据最高能级的电子云轮廓图为
(2)S单质的常见形式为
 ,其环状结构如图所示,S原子的杂化轨道类型是
,其环状结构如图所示,S原子的杂化轨道类型是
(3)基态Se原子的核外电子排布式为
(4)S、Se、Te三种元素电负性由大到小的顺序是
(5)
 分子中共价键的类型是
分子中共价键的类型是 是气体而
是气体而 是液体的原因是
是液体的原因是(6)ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如图所示,S周围紧邻且等距的Zn有
 (NA表示阿伏加德罗常数的值)。
(NA表示阿伏加德罗常数的值)。
您最近一年使用:0次
解题方法
2 . 下图为元素周期表前四周期的一部分。
下列有关W、X、Y、Z四种元素的说法中,正确的是
| X | |||
| W | Y | ||
| Z | |||
| A.电负性:Z>X | B.单质熔点:Y>Z |
| C.原子半径:Y>W | D.第一电离能:Y>W |
您最近一年使用:0次
2022-04-28更新
|
370次组卷
|
3卷引用:天津市南开区2022届高三一模化学试题
名校
3 . 一种由短周期主族元素组成的化合物(如下图所示),具有良好的储氢性能,其中元素W、X、Y、Z的原子序数依次增大、且总和为24。下列有关叙述错误的是
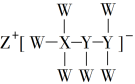
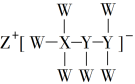
| A.该化合物中,W、X、Y之间均为共价键 |
| B.Z的单质既能与水反应,也可与甲醇反应 |
| C.W、X、Y、Z四种元素电负性Z<X<W<Y |
| D.X的氟化物XF3中原子均为8电子稳定结构 |
您最近一年使用:0次
2022-03-04更新
|
337次组卷
|
2卷引用:天津市南开中学2023-2024学年高三上学期统练5化学试题
名校
解题方法
4 . 短周期主族元素X、Y、Z、W原子序数依次增大,X原子核外有7个电子,基态Y原子无未成对电子,Z与X为同族元素,W最高价含氧酸为二元酸,下列说法正确的是
A.原子半径: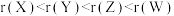 |
| B.元素Y、W的简单离子具有相同的电子层结构 |
| C.Z的最高价氧化物对应水化物的酸性比X的强 |
| D.电负性大小:Y<Z<W |
您最近一年使用:0次
2022-03-03更新
|
348次组卷
|
3卷引用:天津市南开区南开中学2021-2022学年高二上学期期末检测化学试题
名校
5 . 下列说法不正确的是
| A.从空间角度看,2s轨道比1s轨道大,其空间包含了1s轨道 |
B.s-s 键与s-p 键与s-p 键的电子云形状的对称性相同 键的电子云形状的对称性相同 |
| C.电负性大于1.8的为非金属,小于1.8的为金属 |
| D.共价键是原子间通过共用电子对所形成的相互作用 |
您最近一年使用:0次
名校
6 . 下列说法正确的是
| A.电负性:Se>As | B.离子半径:Na+>Cl− |
| C.第一电离能:Al>Mg | D.键长:Cl−Cl>Br−Br |
您最近一年使用:0次
2022-01-07更新
|
500次组卷
|
6卷引用:天津市南开区2021-2022学年高三上学期期末考试化学试卷
名校
7 . 下列说法正确的是
| A.2px、2py、2pz轨道相互垂直,能量不等 |
| B.元素周期表各周期总是从ns能级开始,以np能级结束 |
| C.电负性越大,元素的非金属性越强,第一电离能也越大 |
| D.d区、ds区全部是金属元素 |
您最近一年使用:0次
2021-12-10更新
|
445次组卷
|
2卷引用:天津市南开区南开中学2021-2022学年高二上学期期末检测化学试题
名校
解题方法
8 . 近年来我国科学家发现了一系列意义重大的铁系超导材料,其中一类为Fe-Sm-As-F-O组成的化合物。回答下列问题:
(1)元素As与N同族。预测As的氢化物分子的立体结构为__________________ ,其沸点比NH3的____________ (填“高”或“低”),其判断理由是________________________ 。
(2)Fe成为阳离子时首先失去_____________ 轨道电子。
(3)比较离子半径:F-______ O2-(填“大于”“等于”或“小于”)。
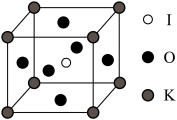
(4)晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示。与K紧邻的O个数为________ 。在KIO3晶胞结构的另一种表示中,I处于各顶角位置,则K处于__________ 位置,O处于_________________ 位置。
(1)元素As与N同族。预测As的氢化物分子的立体结构为
(2)Fe成为阳离子时首先失去
(3)比较离子半径:F-
(4)晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示。与K紧邻的O个数为

您最近一年使用:0次
解题方法
9 . N、P、As的化合物在研究和生产中有许多重要用途。
(1)基态As原子的核外电子排布式为_________ 。
(2)N的第一电离能比O大,原因是______________ 。
(3)NH4+中H-N-H的键角比NH3中H-N-H 的键角_______ (填“大”或“小”),原因是____________ 。
(4)K3AsO4中含有的化学键类型包括________ ;AsO43- 的空间构型为______ 。As4O6的分子结构如图1所示,则该化合物中As的杂化方式是__________ 。

(5)化合物NH5中的所有原子最外层都满足稳定结构,则NH5 是_______ 晶体。
(6)白磷(P4)的晶体属于分子晶体,其晶胞结构如图2 (小圆圈表示白磷分子)。已知晶胞的边长为acm,阿伏伽德罗常数的数值为NA,则该晶胞中含有P 原子的个数为______ ,该晶体的密度为_________ (用含NA、a 的代数式表示) g.cm-3。
(1)基态As原子的核外电子排布式为
(2)N的第一电离能比O大,原因是
(3)NH4+中H-N-H的键角比NH3中H-N-H 的键角
(4)K3AsO4中含有的化学键类型包括

(5)化合物NH5中的所有原子最外层都满足稳定结构,则NH5 是
(6)白磷(P4)的晶体属于分子晶体,其晶胞结构如图2 (小圆圈表示白磷分子)。已知晶胞的边长为acm,阿伏伽德罗常数的数值为NA,则该晶胞中含有P 原子的个数为
您最近一年使用:0次
2018-02-28更新
|
314次组卷
|
3卷引用:天津市南开区南大奥宇培训学校2020届高三下学期第三次月考化学试题



