名校
1 . 利用铜矿石主要成分为 。还含少量
。还含少量 、
、 ,制备
,制备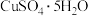 晶体的流程如下图所示。已知
晶体的流程如下图所示。已知 在酸性条件下不稳定,易生成金属
在酸性条件下不稳定,易生成金属 和
和 .下列说法错误的是
.下列说法错误的是
 。还含少量
。还含少量 、
、 ,制备
,制备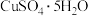 晶体的流程如下图所示。已知
晶体的流程如下图所示。已知 在酸性条件下不稳定,易生成金属
在酸性条件下不稳定,易生成金属 和
和 .下列说法错误的是
.下列说法错误的是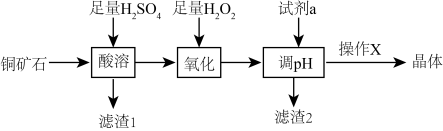
A.“滤渣1”的成分为 、Cu 、Cu |
B.“氧化”过程中的离子方程式: |
| C.操作X为蒸发浓缩,冷却结晶,过滤,洗涤,干燥 |
D.“滤渣2”的成分为 和 和 |
您最近一年使用:0次
名校
2 . 氮的化合物是重要化工原料,也是空气污染物的重要来源,其转化一直是化学研究的热点。
(1)氨催化氧化法是制硝酸的重要步骤,探究氨催化氧化反应的装置如图所示: 。分别生成含等物质的量氮元素的NO和
。分别生成含等物质的量氮元素的NO和 时,各自消耗的
时,各自消耗的 的物质的量之比为
的物质的量之比为______ 。
②一段时间后,观察到装置M中有白烟生成。该白烟成分是______ (写化学式).
(2)可用 将氮氧化物转化成
将氮氧化物转化成 。向1L含200mg
。向1L含200mg 的溶液中加入NaOH溶液调节至碱性,
的溶液中加入NaOH溶液调节至碱性, 转化为去除氮氧化物效果更好的
转化为去除氮氧化物效果更好的 ,再通入NO气体进行反应。碱性条件下
,再通入NO气体进行反应。碱性条件下 去除NO反应的离子方程式为
去除NO反应的离子方程式为______ 。
(3)纳米铁粉可去除水中的 。控制其他条件不变,用纳米铁粉还原水体中的
。控制其他条件不变,用纳米铁粉还原水体中的 ,测得溶液中含氮物质(
,测得溶液中含氮物质( 、
、 、
、 )浓度随时间变化如图所示:
)浓度随时间变化如图所示: 的机理:
的机理: 得到纳米铁粉失去电子转化为
得到纳米铁粉失去电子转化为 ,极少量
,极少量 在纳米铁粉或Cu表面得到电子转化为
在纳米铁粉或Cu表面得到电子转化为 。与不添加少量铜粉相比,添加少量铜粉时去除
。与不添加少量铜粉相比,添加少量铜粉时去除 效率更高,主要原因是
效率更高,主要原因是______ 。
(4)NO也可以利用电化学手段将其转化为 脱除,装置如图所示,电极为多孔惰性材料.则负极的电极反应式是
脱除,装置如图所示,电极为多孔惰性材料.则负极的电极反应式是______ 。______ 。
②b中发生反应的化学方程式为______ 。
③实验中观察到能证明浓硝酸具有强氧化性的现象是______ 。
(1)氨催化氧化法是制硝酸的重要步骤,探究氨催化氧化反应的装置如图所示:
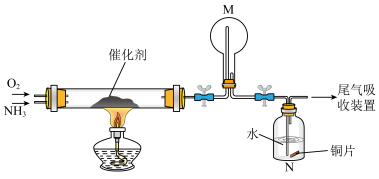
 。分别生成含等物质的量氮元素的NO和
。分别生成含等物质的量氮元素的NO和 时,各自消耗的
时,各自消耗的 的物质的量之比为
的物质的量之比为②一段时间后,观察到装置M中有白烟生成。该白烟成分是
(2)可用
 将氮氧化物转化成
将氮氧化物转化成 。向1L含200mg
。向1L含200mg 的溶液中加入NaOH溶液调节至碱性,
的溶液中加入NaOH溶液调节至碱性, 转化为去除氮氧化物效果更好的
转化为去除氮氧化物效果更好的 ,再通入NO气体进行反应。碱性条件下
,再通入NO气体进行反应。碱性条件下 去除NO反应的离子方程式为
去除NO反应的离子方程式为(3)纳米铁粉可去除水中的
 。控制其他条件不变,用纳米铁粉还原水体中的
。控制其他条件不变,用纳米铁粉还原水体中的 ,测得溶液中含氮物质(
,测得溶液中含氮物质( 、
、 、
、 )浓度随时间变化如图所示:
)浓度随时间变化如图所示: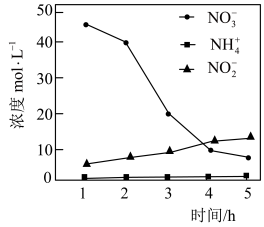
 的机理:
的机理: 得到纳米铁粉失去电子转化为
得到纳米铁粉失去电子转化为 ,极少量
,极少量 在纳米铁粉或Cu表面得到电子转化为
在纳米铁粉或Cu表面得到电子转化为 。与不添加少量铜粉相比,添加少量铜粉时去除
。与不添加少量铜粉相比,添加少量铜粉时去除 效率更高,主要原因是
效率更高,主要原因是(4)NO也可以利用电化学手段将其转化为
 脱除,装置如图所示,电极为多孔惰性材料.则负极的电极反应式是
脱除,装置如图所示,电极为多孔惰性材料.则负极的电极反应式是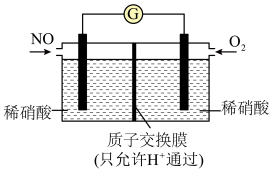
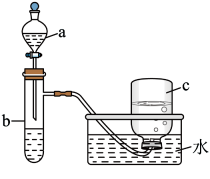
②b中发生反应的化学方程式为
③实验中观察到能证明浓硝酸具有强氧化性的现象是
您最近一年使用:0次
名校
3 . 按要求书写方程式:
(1)工业合成氨每转移7.2mol电子放热112.8kJ,其热化学方程式为______ 。
(2)11.2g铁与2.7g水蒸气反应吸收30kJ热量,其热化学方程式为______ 。
(3)燃烧1.3g乙炔( )气体时。放出热量65kJ,表示乙炔燃烧热的热化学反应方程式为
)气体时。放出热量65kJ,表示乙炔燃烧热的热化学反应方程式为______ 。已知: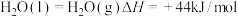 ,则11.2L(标准状况)乙炔完全燃烧生成气态水时放出的热量是
,则11.2L(标准状况)乙炔完全燃烧生成气态水时放出的热量是______ kJ。
(4)2.3g的 气体溶于水,放出akJ热量,其热化学方程式为
气体溶于水,放出akJ热量,其热化学方程式为______ 。
(5) 溶液中滴加硫酸,其离子方程式为
溶液中滴加硫酸,其离子方程式为______ 。
(6)工业上由黄铁矿制硫酸的第二步反应,其化学方程式为______ 。
(7)请用化学方程式解释,在无氧环境中才能观察到氢氧化亚铁沉淀颜色______ 。
(8)检验 的方法,其离子方程式为
的方法,其离子方程式为______ 。
(9)工业制漂白粉,其化学方程式为______ 。
(10)氨水与稀硫酸反应生成1mol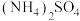 放热24.2kJ;已知
放热24.2kJ;已知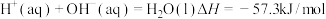 ,
, 电离的热化学方程式为
电离的热化学方程式为______ 。
(1)工业合成氨每转移7.2mol电子放热112.8kJ,其热化学方程式为
(2)11.2g铁与2.7g水蒸气反应吸收30kJ热量,其热化学方程式为
(3)燃烧1.3g乙炔(
 )气体时。放出热量65kJ,表示乙炔燃烧热的热化学反应方程式为
)气体时。放出热量65kJ,表示乙炔燃烧热的热化学反应方程式为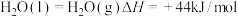 ,则11.2L(标准状况)乙炔完全燃烧生成气态水时放出的热量是
,则11.2L(标准状况)乙炔完全燃烧生成气态水时放出的热量是(4)2.3g的
 气体溶于水,放出akJ热量,其热化学方程式为
气体溶于水,放出akJ热量,其热化学方程式为(5)
 溶液中滴加硫酸,其离子方程式为
溶液中滴加硫酸,其离子方程式为(6)工业上由黄铁矿制硫酸的第二步反应,其化学方程式为
(7)请用化学方程式解释,在无氧环境中才能观察到氢氧化亚铁沉淀颜色
(8)检验
 的方法,其离子方程式为
的方法,其离子方程式为(9)工业制漂白粉,其化学方程式为
(10)氨水与稀硫酸反应生成1mol
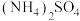 放热24.2kJ;已知
放热24.2kJ;已知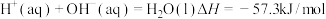 ,
, 电离的热化学方程式为
电离的热化学方程式为
您最近一年使用:0次
名校
4 . X、Y、Z、W为原子序数依次增大的四种短周期元素。X与Z同族,Z的核电荷数是X的2倍,Y原子K层电子数与M层电子数的乘积等于其L层的电子数,下列说法不正确的是
| A.非金属性:X>Z>Y |
| B.Y的氧化物、W的单质均可与NaOH溶液反应 |
| C.W的单质具有漂白性 |
D.化合物 中各原子最外层均满足8电子稳定结构 中各原子最外层均满足8电子稳定结构 |
您最近一年使用:0次
5 . 以下变化中, 大于
大于 的是
的是
 大于
大于 的是
的是A.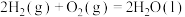  ; ;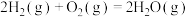  |
B.  ; ;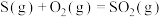  |
C.NaOH固体溶解于水 ; ;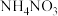 固体溶解于水 固体溶解于水 |
D.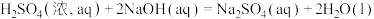  ; ;  |
您最近一年使用:0次
名校
6 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.含1mol硅原子的硅酸钠中,氡原子数为4 |
B.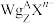 中所含电子总数为 中所含电子总数为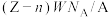 |
C.1mol氮气分子中共用电子对数为3 |
D.25℃时,1mol氯气和足量水反应,转移电子数为 |
您最近一年使用:0次
名校
解题方法
7 . 某研究小组用氨基钠( )与
)与 反应制备叠氮化钠(
反应制备叠氮化钠( )并对制得的叠氮化钠产品纯度进行测定。已知叠氮化钠为易溶于水的白色晶体,微溶于乙醇,不溶于乙醚,NaOH溶于乙醇不溶于乙醚。氨基钠极易水解和氧化;
)并对制得的叠氮化钠产品纯度进行测定。已知叠氮化钠为易溶于水的白色晶体,微溶于乙醇,不溶于乙醚,NaOH溶于乙醇不溶于乙醚。氨基钠极易水解和氧化; 不与酸或碱反应;
不与酸或碱反应; 具有较强还原性(Sn与碳同族)。回答下列问题:
具有较强还原性(Sn与碳同族)。回答下列问题:
(1)制备叠氮化钠:连接好装置后,打开A中分液漏斗活塞,向圆底烧瓶中滴加溶液,充分反应。___________ 。
②装置的连接顺序为a→___________ →h(填仪器接口字母)。
③A中发生反应的化学方程式为___________ ,E装置的作用为___________ 。
④C中发生的反应为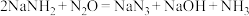 ,反应后待装置冷却,在混合物中加入
,反应后待装置冷却,在混合物中加入___________ ,过滤,用___________ (选填字母)洗涤,晾干得到粗产品。
A.冷水 B.乙醚 C.热水 D.乙醇
(2)测定产品纯度:取装置C中制得的叠氮化钠样品m克放入圆底烧瓶中进行纯度的测定,如图。___________ 。
②读取气体体积时,应注意冷却至室温、___________ 、视线与凹液面最低点水平相切。
③若量气管的初始读数为x mL、末读数为y mL,本实验条件下气体摩尔体积为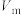 L/mol,则产品中
L/mol,则产品中 的质量分数为
的质量分数为___________ %(表达式)。(提示:量气管刻度与滴定管类似)
④若对所得产品进行X射线衍射实验得到图谱如图所示,该产品属于___________ (填“晶体”或“非晶体”)。
 )与
)与 反应制备叠氮化钠(
反应制备叠氮化钠( )并对制得的叠氮化钠产品纯度进行测定。已知叠氮化钠为易溶于水的白色晶体,微溶于乙醇,不溶于乙醚,NaOH溶于乙醇不溶于乙醚。氨基钠极易水解和氧化;
)并对制得的叠氮化钠产品纯度进行测定。已知叠氮化钠为易溶于水的白色晶体,微溶于乙醇,不溶于乙醚,NaOH溶于乙醇不溶于乙醚。氨基钠极易水解和氧化; 不与酸或碱反应;
不与酸或碱反应; 具有较强还原性(Sn与碳同族)。回答下列问题:
具有较强还原性(Sn与碳同族)。回答下列问题:(1)制备叠氮化钠:连接好装置后,打开A中分液漏斗活塞,向圆底烧瓶中滴加溶液,充分反应。
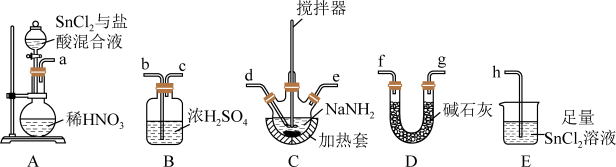
②装置的连接顺序为a→
③A中发生反应的化学方程式为
④C中发生的反应为
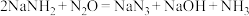 ,反应后待装置冷却,在混合物中加入
,反应后待装置冷却,在混合物中加入A.冷水 B.乙醚 C.热水 D.乙醇
(2)测定产品纯度:取装置C中制得的叠氮化钠样品m克放入圆底烧瓶中进行纯度的测定,如图。
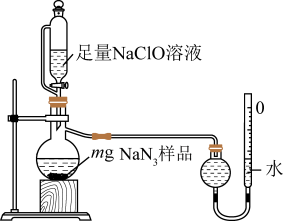
②读取气体体积时,应注意冷却至室温、
③若量气管的初始读数为x mL、末读数为y mL,本实验条件下气体摩尔体积为
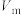 L/mol,则产品中
L/mol,则产品中 的质量分数为
的质量分数为④若对所得产品进行X射线衍射实验得到图谱如图所示,该产品属于
您最近一年使用:0次
名校
解题方法
8 . 有机物K作为一种高性能发光材料,广泛用于有机电致发光器件(OLED)。K的一种合成路线如下所示,部分试剂及反应条件省略。___________ ,F中含氧官能团的电子式为___________ 。
(2)D→E的反应类型为___________ ,G→H的反应方程式为___________ 。
(3)下列说法正确的是___________ (选填字母)。
a.K存在顺反异构
b.C的水溶性比D差
c.1mol J最多可以与7mol氢气发生反应
d.G分子中所有原子可能共平面
e.J的核磁共振氢谱有4个峰
(4)请写出A的同系物中满足条件的结构简式___________ (不考虑不稳定结构)。
①相对分子质量比A小14
②所有碳原子一定在一个平面上
(5)以下合成线路: 步的反应试剂为
步的反应试剂为___________ ,为什么要设计步骤 和步骤
和步骤
___________ 。
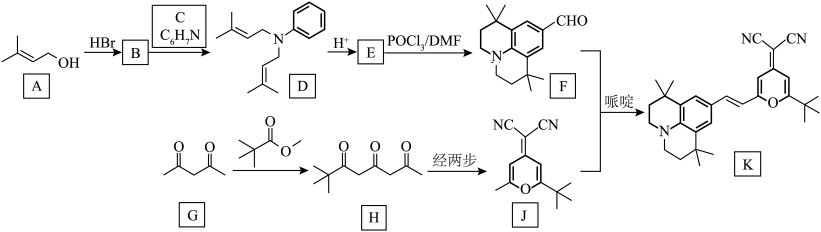
已知: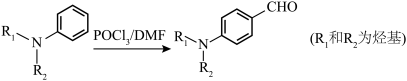
(2)D→E的反应类型为
(3)下列说法正确的是
a.K存在顺反异构
b.C的水溶性比D差
c.1mol J最多可以与7mol氢气发生反应
d.G分子中所有原子可能共平面
e.J的核磁共振氢谱有4个峰
(4)请写出A的同系物中满足条件的结构简式
①相对分子质量比A小14
②所有碳原子一定在一个平面上
(5)以下合成线路:
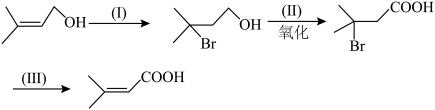
 步的反应试剂为
步的反应试剂为 和步骤
和步骤
您最近一年使用:0次
名校
9 . PtNiFe-LDHGO催化甲醛氧化的反应机理如图:
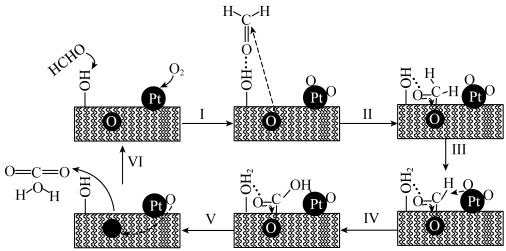
| A.步骤1中甲醛通过氢键吸附在催化剂表面的—OH上 |
| B.PtNiFe-LDHGO降低了该反应的活化能 |
C.该反应每生成1mol  ,转移4mol电子 ,转移4mol电子 |
| D.上述反应机理涉及极性键和非极性键的形成 |
您最近一年使用:0次
名校
10 . 臭氧( )在
)在 催化下能将烟气中的
催化下能将烟气中的 、
、 分别氧化为
分别氧化为 和
和 。下列关于N、O、S、Fe元素及其化合物的说法正确的是
。下列关于N、O、S、Fe元素及其化合物的说法正确的是
 )在
)在 催化下能将烟气中的
催化下能将烟气中的 、
、 分别氧化为
分别氧化为 和
和 。下列关于N、O、S、Fe元素及其化合物的说法正确的是
。下列关于N、O、S、Fe元素及其化合物的说法正确的是A. 是含有极性键的非极性分子 是含有极性键的非极性分子 |
B.由于O、N、S非金属性依次递减,所以沸点: |
C. 的VSEPR模型: 的VSEPR模型: |
D.1mol  含有σ键12mol 含有σ键12mol |
您最近一年使用:0次



