名校
解题方法
1 . 前四周期元素X、Y、Z、Q、W、R原子序数依次增大,Y、Z、Q位于同一周期,X与Z能构成4核18电子分子,化合物甲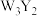 和乙
和乙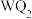 均为离子化合物,W的s电子数和p电子数相等,R是前四周期元素中未成对电子最多的元素,请回答下列有关问题。
均为离子化合物,W的s电子数和p电子数相等,R是前四周期元素中未成对电子最多的元素,请回答下列有关问题。
(1)R在元素周期表中的位置是_______ 。
(2)写出化合物甲的电子式_______ ,化合物甲与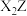 反应的化学方程式为
反应的化学方程式为_______ (用元素符号进行回答,下同) 。
(3)Y、Z、Q三种元素的第一电离能从大到小的顺序是_______ ;Z、Q两元素电负性大小顺序为_______ 。
(4)物质丙、丁、戊、己是由X、Y、Z、Q中的部分元素组成的二元化合物,丙、丁、戊三种分子中电子数相同,单质a和单质b是上述元素构成的单质,上述物质有如下图转化关系。
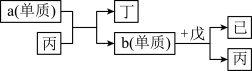
①丁与戊反应生成的化合物中存在的化学键类型是_______ 。
②b单质与戊反应的化学方程式为:_______ 。
(5)元素R的逐级电离能如下表:
R元素在化合物中常表现为+6价,试结合原子结构从电离能角度解释其原因_______ ;
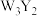 和乙
和乙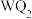 均为离子化合物,W的s电子数和p电子数相等,R是前四周期元素中未成对电子最多的元素,请回答下列有关问题。
均为离子化合物,W的s电子数和p电子数相等,R是前四周期元素中未成对电子最多的元素,请回答下列有关问题。(1)R在元素周期表中的位置是
(2)写出化合物甲的电子式
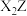 反应的化学方程式为
反应的化学方程式为(3)Y、Z、Q三种元素的第一电离能从大到小的顺序是
(4)物质丙、丁、戊、己是由X、Y、Z、Q中的部分元素组成的二元化合物,丙、丁、戊三种分子中电子数相同,单质a和单质b是上述元素构成的单质,上述物质有如下图转化关系。

①丁与戊反应生成的化合物中存在的化学键类型是
②b单质与戊反应的化学方程式为:
(5)元素R的逐级电离能如下表:
| 电离能 | I1 | I2 | I3 | I4 | I5 | I6 | I7 |
 | 652.9 | 1590.6 | 2987 | 4743 | 6702 | 8744.9 | 15455 |
您最近半年使用:0次
2 . 化合物M由两种短周期主族元素组成,在一定条件下可以发生下列转化:
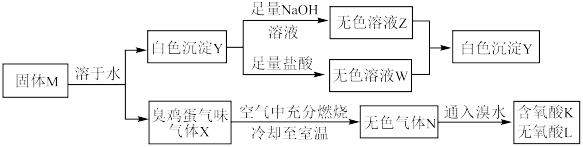
请回答下列问题:
(1)固体M的化学式为___________ 。
(2)无氧酸L中阴离子对应元素在元素周期表中的位置为___________ ,其基态原子中电子的空间运动状态有___________ 种。
(3)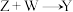 的化学方程式为
的化学方程式为___________ 。
(4)上述流程的反应中涉及的短周期非金属元素的电负性由大到小的顺序为___________ 。
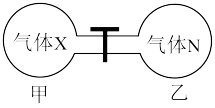
(5)如图所示,在室温下向甲、乙两相同密闭容器中,分别充入等物质的量气体X和气体N。
①反应前两容器中的气体密度: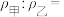
___________ 。
②打开活塞,使气体充分反应,则反应前后的压强: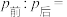
___________ 。
(6)将无色气体N通入到浓硝酸中,有红棕色气体冒出,在反应中n(氧化剂):n(还原剂)=___________ 。

请回答下列问题:
(1)固体M的化学式为
(2)无氧酸L中阴离子对应元素在元素周期表中的位置为
(3)
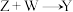 的化学方程式为
的化学方程式为(4)上述流程的反应中涉及的短周期非金属元素的电负性由大到小的顺序为
(5)如图所示,在室温下向甲、乙两相同密闭容器中,分别充入等物质的量气体X和气体N。

①反应前两容器中的气体密度:
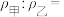
②打开活塞,使气体充分反应,则反应前后的压强:
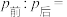
(6)将无色气体N通入到浓硝酸中,有红棕色气体冒出,在反应中n(氧化剂):n(还原剂)=
您最近半年使用:0次
2023-11-22更新
|
86次组卷
|
2卷引用:江西省2024届高三上学期11 月一轮总复习调研测试化学试题
名校
解题方法
3 . A、B、C、D、E、F、G、H是元素周期表前四周期常见元素,且原子序数依次增大,相关信息如下表:
请用化学用语填空:
(1)A元素在元素周期表中的位置___________ ;C元素和F元素的电负性比较,较小的是___________ (填元素符号)。
(2)B元素与宇宙中含量最丰富的元素形成的最简单化合物的电子式为___________ ,B元素所形成的单质分子中σ键与π键数目之比为___________ 。
(3)F元素原子的价电子的轨道表示式是___________ ;G的高价阳离子的溶液与H单质反应的离子方程式为___________ ;元素X与元素E在周期表中呈对角线关系,且元素X的最高价氧化物的水化物也具有两性,试写出X元素的最高价氧化物的水化物与D元素的最高价氧化物的水化物反应的化学方程式___________ 。
| 元素 | 元素相关信息 |
| A | 原子核外有6种不同运动状态的电子 |
| C | 基态原子中s电子总数与p电子总数相等 |
| D | 原子半径在同周期元素中最大 |
| E | 基态原子最外层电子排布式为 |
| F | 基态原子的最外层p轨道有两个电子的自旋方向与其他电子的自旋方向相反 |
| G | 基态原子核外有7个能级且能量最高的能级上有6个电子 |
| H | 是我国使用最早的合金中的最主要元素 |
(1)A元素在元素周期表中的位置
(2)B元素与宇宙中含量最丰富的元素形成的最简单化合物的电子式为
(3)F元素原子的价电子的轨道表示式是
您最近半年使用:0次
4 . W、X、Y为同一周期的四种主族元素,原子序数依次增大。基态Y原子的价电子排布为3s23p4,X的电离能数据如下表所示。
(1)Y在元素周期表中的位置是___________ 。
(2)为了进一步研究最高价氧化物对应水化物的酸碱性与元素金属性、非金属性的关系,查阅如下资料。
资料:ⅰ.某元素最高价氧化物对应的水化物脱水前的化学式通常可以表示为 ,该水化物中的M—O—H结构有两种断键方式:断M—O键在水中电离出OH-;断O—H键在水中离出H+。
,该水化物中的M—O—H结构有两种断键方式:断M—O键在水中电离出OH-;断O—H键在水中离出H+。
ⅱ.在水等强极性溶剂中,成键原子电负性的差异是影响化学键断裂难易程度的原因之一,水化物的M—O—H结构中,成键原子电负性差异越大,所形成的化学键越容易断。
①已知:O、H元素的电负性数值分别为3.5和2.1;某元素M的电负性数值为2.5,且电负性差异是影响M—O—H中化学键断裂难易程度的主要原因。该元素最高价氧化物对应的水化物呈___________ (填“酸”或“碱”)性,依据是___________ 。
②W和X的最高价氧化物对应的水化物中,碱性较强的是___________ (写化学式),结合资料说明理由:___________ 。
| 电离能 |  |  |  |  | … |
 | 738 | 1451 | 7733 | 10540 | … |
(2)为了进一步研究最高价氧化物对应水化物的酸碱性与元素金属性、非金属性的关系,查阅如下资料。
资料:ⅰ.某元素最高价氧化物对应的水化物脱水前的化学式通常可以表示为
 ,该水化物中的M—O—H结构有两种断键方式:断M—O键在水中电离出OH-;断O—H键在水中离出H+。
,该水化物中的M—O—H结构有两种断键方式:断M—O键在水中电离出OH-;断O—H键在水中离出H+。ⅱ.在水等强极性溶剂中,成键原子电负性的差异是影响化学键断裂难易程度的原因之一,水化物的M—O—H结构中,成键原子电负性差异越大,所形成的化学键越容易断。
①已知:O、H元素的电负性数值分别为3.5和2.1;某元素M的电负性数值为2.5,且电负性差异是影响M—O—H中化学键断裂难易程度的主要原因。该元素最高价氧化物对应的水化物呈
②W和X的最高价氧化物对应的水化物中,碱性较强的是
您最近半年使用:0次
5 . A、B、C、D、E、F、G是元素周期表前四周期常见的元素,且原子序数依次增大,其相关信息如表所示,请回答下列问题。
(1)A在元素周期表中的位置为___________ ,画出基态B原子的轨道表示式___________ 。
(2)F元素基态原子的最高能级具有的原子轨道数为___________ ,该原子轨道呈___________ 形。
(3)已知元素A、B形成的 链状分子中所有的原子都满足8电子稳定结构,则其分子中σ键与π键数目之比为
链状分子中所有的原子都满足8电子稳定结构,则其分子中σ键与π键数目之比为___________ 。
(4)C元素可形成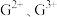 ,其中较稳定的是
,其中较稳定的是 ,原因是
,原因是___________ 。
(5)短周期元素M与元素E在周期表中的位置呈现对角线关系,已知元素M、F的电负性分别为1.5和3.0,预测它们形成的化合物是___________ (填“离子”或“共价”)化合物。推测M的最高价氧化物对应的水化物___________ (填“能”或“不能”)与D的最高价氧化物对应水化物发生反应。
| A | 原子核外有6个电子 |
| B | 原子序数比A大1 |
| C | 基态原子中s电子总数与p电子总数相等 |
| D | 原子半径在同周期元素中最大 |
| E | 基态原子价层电子排布式为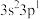 |
| F | 基态原子的最外层p轨道有2个电子的自旋状态与其他电子的自旋状态相反 |
| G | 生活中使用最多的一种金属,其高价氯化物的盐溶液常用于刻蚀铜制印刷电路板 |
(2)F元素基态原子的最高能级具有的原子轨道数为
(3)已知元素A、B形成的
 链状分子中所有的原子都满足8电子稳定结构,则其分子中σ键与π键数目之比为
链状分子中所有的原子都满足8电子稳定结构,则其分子中σ键与π键数目之比为(4)C元素可形成
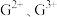 ,其中较稳定的是
,其中较稳定的是 ,原因是
,原因是(5)短周期元素M与元素E在周期表中的位置呈现对角线关系,已知元素M、F的电负性分别为1.5和3.0,预测它们形成的化合物是
您最近半年使用:0次
名校
解题方法
6 . X、Y、Z、M、Q、R是元素周期表前四周期的元素,且原子序数依次增大,其相关信息如表所示:
请回答下列问题。
(1)请写出元素R在元素周期表中位置:_______ 。
(2)X、Y、Z、M四种元素的原子半径由小到大的顺序是_______ (用元素符号表示)。
(3)元素R可形成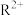 和
和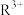 ,其中较稳定的是
,其中较稳定的是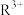 ,原因是
,原因是_______ 。
(4)短周期元素T与元素M在周期表中的位置呈现对角线关系,则元素T为_______ (填元素符号);已知元素T、Q的电负性分别为1.5和3.0,则它们形成的化合物是_______ (填“离子化合物”或“共价化合物”)。
| 元素代号 | 相关信息 |
| X | 原子核外有6种不同运动状态的电子 |
| Y | 基态原子中s电子总数与p电子总数相等 |
| Z | 原子半径在同周期元素中最大 |
| M | 第一至第六电离能(kJ/mol)依次为578、1817、2745、11575、14830、18376 |
| Q | 基态原子的最外层p轨道上有两个电子的自旋方向与其他电子的自旋方向相反 |
| R | 基态原子核外有7个能级上有电子且能量最高的能级上有6个电子 |
(1)请写出元素R在元素周期表中位置:
(2)X、Y、Z、M四种元素的原子半径由小到大的顺序是
(3)元素R可形成
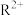 和
和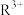 ,其中较稳定的是
,其中较稳定的是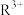 ,原因是
,原因是(4)短周期元素T与元素M在周期表中的位置呈现对角线关系,则元素T为
您最近半年使用:0次
解题方法
7 . 上海有机化学研究所施世良课题组以Ni(cod)2为催化剂实现了叔醇的手性合成。
(1)Ni在元素周期表中的位置是_______ ,写出其基态原子的价电子排布式:_______ 。
(2)Ni(cod)2是指双-(1,5-环辛二烯)镍,其结构如图所示。
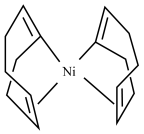
①与碳元素同周期且电负性大于碳的元素有_______ 种。
②Ni(cod)2分子内存在的作用力有_______ (填序号)。
a.配位键 b.金属键 c.极性键 d.非极性键 e.氢键
③Ni(cod)2分子中碳原子的杂化方式为_______ 。
(3)葡萄糖(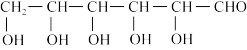 )分子中,手性碳原子个数为
)分子中,手性碳原子个数为 _______ 。
(4)下图三种叔醇的沸点从高到低的顺序及原因是_______ 。

(5)红银矿NiAs晶体结构如图所示:
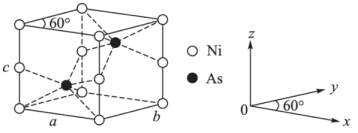
①Ni原子的配位数为_______ 。
②两个As原子的原子分数坐标依次为( ,
, ,
, )和
)和_______ 。
③已知晶体密度为pg·cm-3,X射线光谱测算出的晶胞参数为a=b=m pm、c=n pm,则阿伏加德罗常数NA可表示为_______ mol-1(用含m、n和p的代数式表示)。
(1)Ni在元素周期表中的位置是
(2)Ni(cod)2是指双-(1,5-环辛二烯)镍,其结构如图所示。

①与碳元素同周期且电负性大于碳的元素有
②Ni(cod)2分子内存在的作用力有
a.配位键 b.金属键 c.极性键 d.非极性键 e.氢键
③Ni(cod)2分子中碳原子的杂化方式为
(3)葡萄糖(
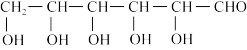 )分子中,手性碳原子个数为
)分子中,手性碳原子个数为 (4)下图三种叔醇的沸点从高到低的顺序及原因是

(5)红银矿NiAs晶体结构如图所示:

①Ni原子的配位数为
②两个As原子的原子分数坐标依次为(
 ,
, ,
, )和
)和③已知晶体密度为pg·cm-3,X射线光谱测算出的晶胞参数为a=b=m pm、c=n pm,则阿伏加德罗常数NA可表示为
您最近半年使用:0次
解题方法
8 . Ⅰ.硒-钴-镧(La)三元整流剂在导电玻璃中应用广泛,且三种元素形成的单质及其化合物均有重要的应用。请回答下列问题:
(1)镧与Sc同族位于第六周期,镧位于元素周期表中_____ 区。
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+ 表示,则与之相反的用-
表示,则与之相反的用- 表示,称为电子的自旋磁量子数。对于基态Co原子,其核外电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态Co原子,其核外电子自旋磁量子数的代数和为_____ 。
(3)一种含Se的新型AIE分子Ⅳ的合成路线如图:
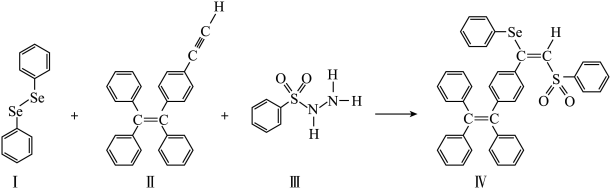
下列说法正确的是_____ 。
A.I中仅有σ键
B.I中Se-Se键为非极性共价键
C.Ⅱ易溶于水
D.Ⅱ中原子的杂化轨道类型有sp、sp2和sp3
E.I~Ⅲ含有的元素中,O电负性最大
F.Ⅳ中具有孤电子对的原子有O和Se
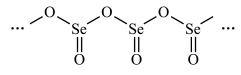
(4)硒的某种氧化物为链状聚合结构,该氧化物的化学式为_____ 。研究发现,给小鼠喂食适量硒酸钠(Na2SeO4)可减轻重金属铊引起的中毒,SeO 的立体构型为
的立体构型为_____ 。
Ⅱ.硼是第ⅢA族中唯一的非金属元素,可以形成众多的化合物。
(5)自然界中不存在单质硼,硼的氢化物也很少,主要存在的是硼的含氧化合物,根据表中数据分析其原因是_____ 。
(6)氨硼烷(H3N·BH3)是目前最具潜力的储氢材料之一。氮硼烷分子中与N相连的H呈正电性,与B原子相连的H呈负电性,它们之间存在静电相互吸引作用,称为双氢键,用“N-H…H-B”表示。以下物质之间可能形成双氢键的是_____ 。
(1)镧与Sc同族位于第六周期,镧位于元素周期表中
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+
 表示,则与之相反的用-
表示,则与之相反的用- 表示,称为电子的自旋磁量子数。对于基态Co原子,其核外电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态Co原子,其核外电子自旋磁量子数的代数和为(3)一种含Se的新型AIE分子Ⅳ的合成路线如图:

下列说法正确的是
A.I中仅有σ键
B.I中Se-Se键为非极性共价键
C.Ⅱ易溶于水
D.Ⅱ中原子的杂化轨道类型有sp、sp2和sp3
E.I~Ⅲ含有的元素中,O电负性最大
F.Ⅳ中具有孤电子对的原子有O和Se
(4)硒的某种氧化物为链状聚合结构,该氧化物的化学式为
 的立体构型为
的立体构型为
Ⅱ.硼是第ⅢA族中唯一的非金属元素,可以形成众多的化合物。
(5)自然界中不存在单质硼,硼的氢化物也很少,主要存在的是硼的含氧化合物,根据表中数据分析其原因是
| 化学键 | B-H | B-O | B-B |
| 键能/(kJ•mol-1) | 389 | 561 | 293 |
| A.H2O2和H2O | B.苯和三氯甲烷 | C.C2H4和C2H2 | D.B2H6和NH3 |
您最近半年使用:0次
9 . 根据原子结构与性质的相关知识,请回答下列问题:
(1)基态S原子电子占据最高能层的符号是______ ,最高能级的电子云轮廓图为______ 形。
(2)电负性As______ Se(填“大于”或“小于”)。
(3) 基态核外电子排布式为
基态核外电子排布式为______ ,基态磷原子的核外价电子排布图为______ 。
(4)铜元素在元素周期表中的位置是______ ,位于元素周期表的______ 区。
(5)C、N、O的第一电离能由大到小的顺序为______ 。
(6)已知 和
和 反应放热,且断开1molH−H键、1molO=O键、1molO−H键吸收的能量分别为
反应放热,且断开1molH−H键、1molO=O键、1molO−H键吸收的能量分别为 kJ、
kJ、 kJ、
kJ、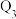 kJ,由此推知下列关系正确的是______(填选项字母)。
kJ,由此推知下列关系正确的是______(填选项字母)。
(1)基态S原子电子占据最高能层的符号是
(2)电负性As
(3)
 基态核外电子排布式为
基态核外电子排布式为(4)铜元素在元素周期表中的位置是
(5)C、N、O的第一电离能由大到小的顺序为
(6)已知
 和
和 反应放热,且断开1molH−H键、1molO=O键、1molO−H键吸收的能量分别为
反应放热,且断开1molH−H键、1molO=O键、1molO−H键吸收的能量分别为 kJ、
kJ、 kJ、
kJ、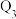 kJ,由此推知下列关系正确的是______(填选项字母)。
kJ,由此推知下列关系正确的是______(填选项字母)。A.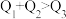 | B.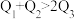 | C.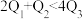 | D.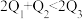 |
您最近半年使用:0次
10 . 我国科学家制备了一种高性能Bi@氮掺杂碳纳米笼。其合成过程如下图。
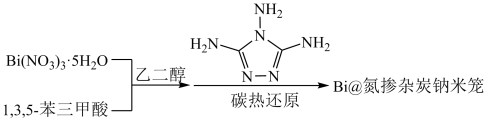
回答下列问题。
(1)元素Bi的基态原子的价电子排布式为6s26p3,则元素Bi在元素周期表中的位置为_______ 。
(2)1,3,5-苯三甲酸中各元素电负性从大到小的顺序为_______ 。
(3)与Bi(NO3)3·5H2O中阴离子互为等电子体的分子有_______ 。(用短周期元素写出两种)
(4)下列状态的N中,失去一个电子所需能量最大的是_______。
(5)铁酸铋(BiFeO3)属于多铁材料的一种,具有铁电性和反铁磁性,并伴随弱的铁磁性。其晶胞结构如图所示。
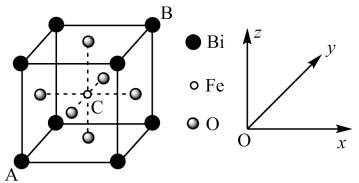
①距离Bi最近且等距离的O有_______ 个。
②晶胞有两个基本要素:一是原子坐标参数,表示晶胞内部各原子的相对位置。在铁酸铋(BiFeO3)的晶胞中,原子坐标参数A为(0,0,0);B为(1,1,1)。则C原子的坐标参数为_______ 。二是晶胞参数,用于描述晶胞的大小和形状。已知铁酸铋(BiFeO3)的晶胞参数a=565.76pm,其密度为_______ g/cm3(列出含NA的计算式即可)。

回答下列问题。
(1)元素Bi的基态原子的价电子排布式为6s26p3,则元素Bi在元素周期表中的位置为
(2)1,3,5-苯三甲酸中各元素电负性从大到小的顺序为
(3)与Bi(NO3)3·5H2O中阴离子互为等电子体的分子有
(4)下列状态的N中,失去一个电子所需能量最大的是_______。
A.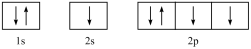 | B. |
C. | D. |

①距离Bi最近且等距离的O有
②晶胞有两个基本要素:一是原子坐标参数,表示晶胞内部各原子的相对位置。在铁酸铋(BiFeO3)的晶胞中,原子坐标参数A为(0,0,0);B为(1,1,1)。则C原子的坐标参数为
您最近半年使用:0次



