名校
解题方法
1 . 青霉胺可以用于医学上误食铜盐的解毒,解毒原理: 形成环状配合物,其结构如图所示。该配合物无毒、易溶于水,可经尿液排出。下列说法正确的是
形成环状配合物,其结构如图所示。该配合物无毒、易溶于水,可经尿液排出。下列说法正确的是
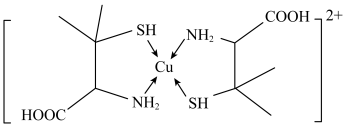
 形成环状配合物,其结构如图所示。该配合物无毒、易溶于水,可经尿液排出。下列说法正确的是
形成环状配合物,其结构如图所示。该配合物无毒、易溶于水,可经尿液排出。下列说法正确的是
A.共价键键角的大小关系为: |
B.电负性大小关系为: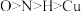 |
| C.该配合物易溶于水的主要原因是其与水可形成分子间氢键 |
D.与铜离子形成配位键强弱的大小关系为: |
您最近一年使用:0次
名校
2 . 类比推理是学习化学的重要的思维方法,下列陈述I及类比推理陈述Ⅱ均正确的是
| 选项 | 陈述I | 类比推理陈述II |
| A | 在空气中加热, 生成 生成 | 在空气中加热, 也生成 也生成 |
| B | 酸性: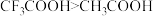 | 碱性: |
| C |  是强酸 是强酸 |  也是强酸 也是强酸 |
| D | 通入 可增强漂白粉溶液漂白性 可增强漂白粉溶液漂白性 | 通入 也可增强漂白粉溶液漂白性 也可增强漂白粉溶液漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . X、Y、Z、W四种短周期主族元素,原子序数依次增大。X、Y与Z位于同一周期,且只有X、Y元素相邻,X基态原子核外有2个未成对电子,W原子在同周期中原子半径最大。下列说法不正确 的是
A.第一电离能: |
B.电负性: |
C.Z、W原子形成稀有气体电子构型的简单离子的半径: |
D.Y与Z形成的分子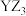 中每个原子均满足 中每个原子均满足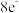 结构 结构 |
您最近一年使用:0次
2024-01-09更新
|
460次组卷
|
3卷引用:海南省农垦中学2023-2024学年高二上学期期中检测化学试题
名校
4 . 法匹拉韦是治疗新冠肺炎的一种药物,其结构简式如图所示。下列说法正确的是


A.该分子的分子式为 |
B.该分子中相邻C原子之间均以 杂化轨道重叠形成σ键 杂化轨道重叠形成σ键 |
| C.组成该分子的所有元素中氟的电负性最大 |
| D.该分子中有2个手性碳原子 |
您最近一年使用:0次
5 . 下图是元素周期表的一部分,图中所列字母分别代表一种化学元素。回答下列问题:

(1)j元素基态原子的电子排布式是___________ 。
(2)元素k位于周期表中___________ 区,其基态原子有___________ 个未成对电子,有___________ 种空间运动状态不同的电子。
(3)下列正确的是___________。
(4)基态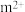 的离子结构示意图为
的离子结构示意图为___________ ,已知高温下化合物 比化合物
比化合物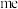 更稳定,试从
更稳定,试从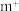 离子的核外电子排布的角度解释原因
离子的核外电子排布的角度解释原因___________ 。
(5)根据对角线规则,b与h的化学性质相似,请写出b的最高价氧化物对应的水化物与 溶液反应的离子方程式
溶液反应的离子方程式___________ 。
(6)传闻某国合成了第166号元素,若已知原子结构规律不变,该元素应是第___________ 周期、第___________ 族。

(1)j元素基态原子的电子排布式是
(2)元素k位于周期表中
(3)下列正确的是___________。
A.原子半径 | B.第一电离能 |
C.电负性 | D.最高价氧化物的水化物的酸性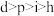 |
(4)基态
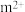 的离子结构示意图为
的离子结构示意图为 比化合物
比化合物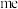 更稳定,试从
更稳定,试从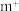 离子的核外电子排布的角度解释原因
离子的核外电子排布的角度解释原因(5)根据对角线规则,b与h的化学性质相似,请写出b的最高价氧化物对应的水化物与
 溶液反应的离子方程式
溶液反应的离子方程式(6)传闻某国合成了第166号元素,若已知原子结构规律不变,该元素应是第
您最近一年使用:0次
6 . 一水合甘氨酸锌是一种矿物类饲料添加剂,结构简式如图:

(1)基态Zn2+的价电子排布式为____ ;一水合甘氨酸锌中所涉及的非金属元素电负性由大到小的顺序是______ 。
(2)甘氨酸H2N-CH2-COOH中N的杂化轨道类型为__________ ;甘氨酸易溶于水,试从结构角度解释__________ 。
(3)一水合甘氨酸锌中Zn2+的配位数为__________ 。
(4)Zn与S形成某种化合物的晶胞如图所示。
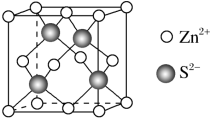
①Zn与S形成某种化合物的化学式__________ ;
②已知晶胞的边长为a pm,则晶体密度:__________ g/cm3 (写计算表达式)。

(1)基态Zn2+的价电子排布式为
(2)甘氨酸H2N-CH2-COOH中N的杂化轨道类型为
(3)一水合甘氨酸锌中Zn2+的配位数为
(4)Zn与S形成某种化合物的晶胞如图所示。

①Zn与S形成某种化合物的化学式
②已知晶胞的边长为a pm,则晶体密度:
您最近一年使用:0次
7 . 我国科学家研究发现,在KOH催化下,CO(NH2)2和LiTPSI还原形成稳定的LiF/高分子双层SEI,使LiMn2O4//Li4T15O12电池稳定工作。请回答下列问题:
(1)基态Mn2+的电子排布式为[Ar]____ 。基态K原子核外电子云轮廓图呈球形的能级上占据的电子总数为____ 。
(2)Mn的第三电离能大于Fe的第三电离能的主要原因是____ 。
(3)CO(NH2)2中元素电负性由大到小的顺序为____ (用元素符号表示)。CO(NH2)2分子中碳原子的杂化方式为____ 。
(4)几种钛的卤化物的熔点如表所示:
钛的卤化物熔点呈上述变化的主要原因是____ 。
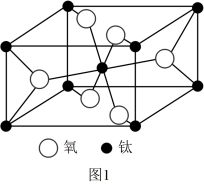
(5)一种钛的氧化物晶胞如图1所示,其化学式为____ 。
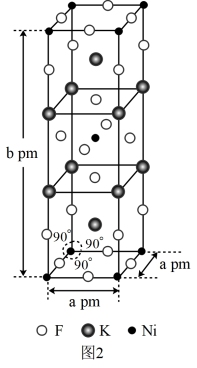
(6)由钾、镍、氟组成的一种晶体结构如图2所示,该晶体密度为____ g·cm-3(只列计算式即可)。
(1)基态Mn2+的电子排布式为[Ar]
(2)Mn的第三电离能大于Fe的第三电离能的主要原因是
(3)CO(NH2)2中元素电负性由大到小的顺序为
(4)几种钛的卤化物的熔点如表所示:
| 卤化物 | TiF4 | TiCl4 | TiBr4 | TiI4 |
| 熔点/℃ | 377 | -25 | 39 | 150 |
(5)一种钛的氧化物晶胞如图1所示,其化学式为

(6)由钾、镍、氟组成的一种晶体结构如图2所示,该晶体密度为

您最近一年使用:0次
解题方法
8 . 新型储氢材料是开发利用氢能的重要研究方向。
(1)Ti(BH4)3是一种储氢材料,可由TiC14和LiBH4反应制得。LiBH4由Li+和BH 构成,BH
构成,BH 的立体结构是
的立体结构是_______ ,B原子的杂化轨道类型是_______ 。Li、B、H元素的电负性由大到小排列顺序为_______ 。
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li+_______ H-(填“>”、“=”或“<”)。
②某储氢材料是第三周期金属元素M的氢化物。M的部分电离能如表所示:
M是_______ (填元素符号)。
(3)NaH具有NaCl型晶体结构,已知NaH晶体的晶胞参数a=488pm(棱长),NaH的理论密度是_______ g/cm3(只列算式,不必计算出数值,阿伏加德罗常数为NA)。
(1)Ti(BH4)3是一种储氢材料,可由TiC14和LiBH4反应制得。LiBH4由Li+和BH
 构成,BH
构成,BH 的立体结构是
的立体结构是(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径:Li+
②某储氢材料是第三周期金属元素M的氢化物。M的部分电离能如表所示:
| I1(kJ/mol) | I2(kJ/mol) | I3(kJ/mol) | I4(kJ/mol) | I5(kJ/mol) |
| 738 | 1451 | 7733 | 10540 | 13630 |
M是
(3)NaH具有NaCl型晶体结构,已知NaH晶体的晶胞参数a=488pm(棱长),NaH的理论密度是
您最近一年使用:0次
名校
解题方法
9 . 现有四种元素的基态原子的电子排布式如下:
① 1s22s22p4 ② 1s22s22p63s23p3 ③ 1s22s22p3 ④ 1s22s22p5
则下列有关比较中正确的是( )
① 1s22s22p4 ② 1s22s22p63s23p3 ③ 1s22s22p3 ④ 1s22s22p5
则下列有关比较中正确的是( )
| A.最高正化合价:④>①>③=② | B.电负性:④>①>③>② |
| C.原子半径:④>③>②>① | D.第一电离能:④>③>①>② |
您最近一年使用:0次
名校
10 . 下列各组元素中,电负性依次减小的是
| A.O、Cl、H | B.K、Na、Al | C.As、P、H | D.O、S、Cl |
您最近一年使用:0次
2020-04-27更新
|
377次组卷
|
11卷引用:海南省三亚华侨学校2019-2020学年高二上学期期中考试化学试题
海南省三亚华侨学校2019-2020学年高二上学期期中考试化学试题2014-2015学年宁夏平罗中学高二上学期期中化学试卷河北省唐山市第十一中学2018-2019学年高二下学期期中考试化学试题新疆喀什地区巴楚县第一中学2020-2021学年高二上学期期中考试化学试题海南省海南鑫源高级中学2020-2021学年高二下学期第一次月考化学试题福建省福州市金山中学2020-2021学年高二下期中考试化学试题2015-2016学年湖北省长阳一中高二第一学期第一次月考化学试卷辽宁省丹东市2017-2018学年高二下学期期末质量监测化学试题第二节 原子结构与元素的性质 第2课时 元素周期律——原子半径、电离能、电负性的递变规律1.3.2元素的电离能、电负性及其变化规律(课中)-鲁科版选择性必修21.2.2 元素周期律-课堂例题



