名校
解题方法
1 . 扬州大学俞磊教授团队利用萤石直接制备电池电解质材料甲( )的新方法如下:
)的新方法如下: 、
、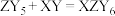 ,其中X、Y、Z、M、Q为原子序数依次增大的前20号主族元素,X、Q为金属元素,Y、M为同主族元素,且Y是电负性最大的元素,基态Z原子的成对电子数与未成对电子数之比为4∶1。下列说法错误的是
,其中X、Y、Z、M、Q为原子序数依次增大的前20号主族元素,X、Q为金属元素,Y、M为同主族元素,且Y是电负性最大的元素,基态Z原子的成对电子数与未成对电子数之比为4∶1。下列说法错误的是
 )的新方法如下:
)的新方法如下: 、
、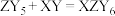 ,其中X、Y、Z、M、Q为原子序数依次增大的前20号主族元素,X、Q为金属元素,Y、M为同主族元素,且Y是电负性最大的元素,基态Z原子的成对电子数与未成对电子数之比为4∶1。下列说法错误的是
,其中X、Y、Z、M、Q为原子序数依次增大的前20号主族元素,X、Q为金属元素,Y、M为同主族元素,且Y是电负性最大的元素,基态Z原子的成对电子数与未成对电子数之比为4∶1。下列说法错误的是| A.基态X原子核外只有1个未成对电子 | B.第一电离能:Q<Z<M<Y |
| C.简单离子半径:Q>M>Y | D.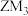 、 、 均为三角锥形分子 均为三角锥形分子 |
您最近一年使用:0次
2024-03-30更新
|
377次组卷
|
4卷引用:河北省唐山市第二中学2024届高三下学期五月联考化学试卷
河北省唐山市第二中学2024届高三下学期五月联考化学试卷湖南省衡阳市2024届高三下学期第二次联考(二模) 化学试题2024届山东省泰安肥城市高考仿真模拟(三)化学试题(已下线)压轴题05?“位-构-性”元素推断(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)
名校
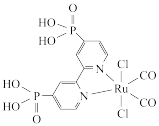
2 . 近年来,光催化剂的研究是材料领域的热点。一种Ru配合物(如图所示)复合光催化剂可将 转化为HCOOH。下列说法
转化为HCOOH。下列说法错误 的是
 转化为HCOOH。下列说法
转化为HCOOH。下列说法
| A.Ru配合物中第二周期元素的电负性:O>N>C |
B.吡啶(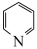 ,原子在同一平面)中C、N原子的杂化方式分别为 ,原子在同一平面)中C、N原子的杂化方式分别为 、 、 |
| C.该配合物中Ru的配位数是6 |
D. 中P的价层电子对数为4,空间结构为正四面体形 中P的价层电子对数为4,空间结构为正四面体形 |
您最近一年使用:0次
名校
3 . 某离子化合物结构如图,其中元素A为过渡金属,W、Y、Z、M、X为原子序数依次增大的五种短周期元素,且位于同周期的原子位置相邻,原子半径: ,M基态原子的所有s轨道上共有6个电子。下列说法错误的是
,M基态原子的所有s轨道上共有6个电子。下列说法错误的是
 ,M基态原子的所有s轨道上共有6个电子。下列说法错误的是
,M基态原子的所有s轨道上共有6个电子。下列说法错误的是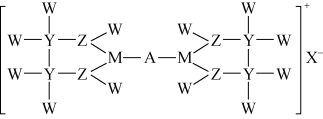
| A.化合物中除A外,其他原子均达到稀有气体的稳定结构 |
| B.W与M、Z均可形成18电子微粒,沸点前者高 |
C.化合物 的空间结构为正四面体形,可做灭火剂 的空间结构为正四面体形,可做灭火剂 |
D.电负性: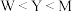 |
您最近一年使用:0次
名校
4 . X、Y、Z、J、Q是原子序数依次增大,且分布在三个短周期的主族元素,Y元素原子的核外未成对电子数在同周期中最多,Y、Z同周期,Z、J同主族.下列说法错误的是
| A.电负性:Q>J;第一电离能:Y>Z | B.最高价含氧酸的酸性:Q>J |
C. 、 、 的中心原子杂化方式相同 的中心原子杂化方式相同 | D.简单离子半径:Y>Z、J>Q |
您最近一年使用:0次
2023-06-21更新
|
584次组卷
|
5卷引用:河北省衡水市第二中学2023届高三下学期三模化学试题
河北省衡水市第二中学2023届高三下学期三模化学试题河北省泊头市第一中学2023-2024学年高三上学期开学考试化学试题(已下线)第19讲元素周期律与元素周期表(已下线)开学摸底考试卷-2024年高考化学一轮复习考点通关卷(新高考通用)(已下线)考点18 元素周期律与元素周期表(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)
5 . 某液晶分子结构如图所示,X、Y、Z、W为原子序数依次增大的短周期非金属元素,基态X原子的电子只有一种自旋取向,基态W原子核外s能级上的电子总数与p能级上的电子总数相等,Y与W的质子数之和等于Z的质子数的2倍。下列说法错误的是
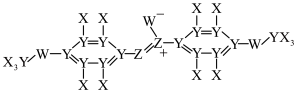
| A.电负性:W>Z>Y | B.第一电离能:Z>W>Y |
| C.常见单质分子键能:X>W>Z | D.简单氢化物沸点:W>Z>Y |
您最近一年使用:0次
2024-04-19更新
|
333次组卷
|
2卷引用:河北省重点高中2023-2024学年高三下学期5月高考模拟化学试题(二)
解题方法
6 . 一氯乙酸可用作除锈剂,其制备原理为 。下列说法错误的是
。下列说法错误的是
 。下列说法错误的是
。下列说法错误的是| A.还可能生成二氯乙酸、三氯乙酸等副产物 |
B. 中所含化学键只有σ键 中所含化学键只有σ键 |
| C.Cl-Cl键的键长比I-I键的键长短 |
D. 的酸性比 的酸性比 强 强 |
您最近一年使用:0次
名校
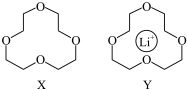
7 . 冠醚是由多个二元醇分子之间失水形成的环状醚,X是其中的一种, 因其体积大小与X的空腔大小相近而恰好能进入X的环内形成超分子Y,Y中
因其体积大小与X的空腔大小相近而恰好能进入X的环内形成超分子Y,Y中 与氧原子间能形成化学键.下列说法错误的是
与氧原子间能形成化学键.下列说法错误的是
 因其体积大小与X的空腔大小相近而恰好能进入X的环内形成超分子Y,Y中
因其体积大小与X的空腔大小相近而恰好能进入X的环内形成超分子Y,Y中 与氧原子间能形成化学键.下列说法错误的是
与氧原子间能形成化学键.下列说法错误的是
| A.X形成的晶体为分子晶体 | B.Y中 与氧原子间形成的是离子键 与氧原子间形成的是离子键 |
C. 不能与X形成超分子 不能与X形成超分子 | D.电负性:O>C>H>Li |
您最近一年使用:0次
2023-05-27更新
|
310次组卷
|
6卷引用:河北省武邑中学2023届高三5月大联考化学试题
河北省武邑中学2023届高三5月大联考化学试题湖南省郴州市九校联盟2023届高三适应考试化学试卷题(已下线)考点巩固卷06 物质结构与性质(4大考点55题)-2024年高考化学一轮复习考点通关卷(新高考通用)(已下线)第7讲 配合物与超分子湖南省邵东市第一中学2023-2024学年高三上学期第四次月考化学试题湖北省武汉市武钢三中2023-2024学年高二下学期3月月考化学试题
名校
8 . 下列陈述I与陈述II均正确,具有因果关系的是
| 选项 | 陈述I | 陈述II |
| A | 向Ag3CrO3(砖红色)悬浊液中入NaCl溶液、有白色沉淀生成 | Ksp(Ag3CrO3)>Ksp(AgCl) |
| B | 第一电离能:P<S | 同周期元素从左至右第一电离能呈现增大趋势 |
| C | 电负性F>Cl | 酸性:CF3COOH>CCl3COOH |
| D | Al2O3熔点比AlCl3高 | 工业上电解熔融Al2O3冶炼铝 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-22更新
|
262次组卷
|
3卷引用:2024届河北省高三下学期部分学校4月质量检测化学试题
9 . 甲基氯硅烷(CH3SiH2Cl)、乙二胺(NH2CH2CH2NH2)和乙二醇(HOCH2CH2OH)常用于制备硅橡胶和聚合物树脂。下列说法错误的是
| A.上述物质中硅和氮的杂化方式相同 |
| B.上述物质所含元素中,电负性的大小顺序为O>N>C>Si |
| C.乙二胺中氢键(N-H…N)的键能高于乙二醇中氢键(O-H…O)的键能 |
| D.上述物质所含元素中,第一电离能的大小顺序为N>O>C>Si |
您最近一年使用:0次
2024-03-27更新
|
258次组卷
|
2卷引用:2024届河北省张家口市高三下学期一模化学试题
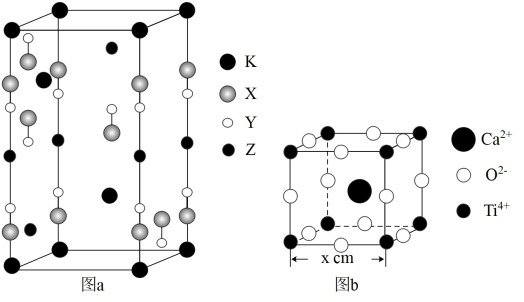
10 . 光电材料[氟代硼铍酸钾晶体(KBe2BO3F2)、CaTiO3等]是目前科学家特别关注的材料。KBe2BO3F2(晶胞结构如图a,其中氧原子已省略,图a中的原子分别位于晶胞的顶点、棱及面上)是一种可制造出深紫外固体激光器的光电材料,可由BeO、KBF4和B2O3在一定条件下制得,同时放出BF3气体;CaTiO3(晶胞结构如图b)在光、电、热等领域有着独特的性质特征。
(1)基态Ti原子的核外电子排布式为____ 。
(2)KBF4是离子化合物,BF3、BF 中B原子的杂化方式依次为
中B原子的杂化方式依次为____ 、____ 。
(3)KBe2BO3F2的组成元素中,非金属元素的电负性由强到弱的顺序为____ (填元素符号),基态原子的第一电离能:Be____ (填“>”或“<”)B。
(4)图a中,已知原子半径X>Y,X、Z分别表示____ 、____ 。(填元素符号)
(5)图b中,与Ti4+最近且距离相等的氧离子构成的几何图形为____ ,若设晶胞边长为xcm,则Ti4+与最近的 间的距离为
间的距离为____ (填含x的表达式)cm;表示该晶体的晶胞还可以有另一种画法,将Ca2+置于立方体的顶点,则Ti4+的位置是____ 。

(1)基态Ti原子的核外电子排布式为
(2)KBF4是离子化合物,BF3、BF
 中B原子的杂化方式依次为
中B原子的杂化方式依次为(3)KBe2BO3F2的组成元素中,非金属元素的电负性由强到弱的顺序为
(4)图a中,已知原子半径X>Y,X、Z分别表示
(5)图b中,与Ti4+最近且距离相等的氧离子构成的几何图形为
 间的距离为
间的距离为
您最近一年使用:0次



