名校
1 . 化合物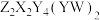 是制备
是制备 (结构如图所示)的一种原料,其中W、X、Y、Z为原子序数依次增大的短周期主族元素,W与X原子的核外电子数之和等于Y原子的价层电子数,基态Z原子的s能级与p能级填充的电子总数相等。下列说法正确的是
(结构如图所示)的一种原料,其中W、X、Y、Z为原子序数依次增大的短周期主族元素,W与X原子的核外电子数之和等于Y原子的价层电子数,基态Z原子的s能级与p能级填充的电子总数相等。下列说法正确的是
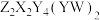 是制备
是制备 (结构如图所示)的一种原料,其中W、X、Y、Z为原子序数依次增大的短周期主族元素,W与X原子的核外电子数之和等于Y原子的价层电子数,基态Z原子的s能级与p能级填充的电子总数相等。下列说法正确的是
(结构如图所示)的一种原料,其中W、X、Y、Z为原子序数依次增大的短周期主族元素,W与X原子的核外电子数之和等于Y原子的价层电子数,基态Z原子的s能级与p能级填充的电子总数相等。下列说法正确的是
| A.元素的电负性;X>Y>Z |
| B.常见单质的熔点;Z>X>Y>W |
| C.X、Z的单质均可通过电解熔融其氯化物的方法冶炼 |
D. 中键角;Y-X-Y>W-Y-X 中键角;Y-X-Y>W-Y-X |
您最近一年使用:0次
2024-05-24更新
|
249次组卷
|
2卷引用:河北省衡水市部分示范性高中2024届高三下学期三模化学试题
2 . 物质的结构决定其性质.下列事实与解释不相符的是
选项 | 事实 | 解释 |
A | 基态Cu原子价层电子排布式为3d104s1 | 3d能级电子为全充满状态,原子能量更低 |
B | 水的热稳定性强于氨 | 水分子间形成的氢键数目与强度均大于氨 |
C | 三氟乙酸的酸性强于乙酸 | 氟为吸电子基,导致羟基中O-H键极性变大 |
D | Na2O、MgO、Al2O3离子键成分的百分数依次减小 | Na、Mg、Al的电负性依次增大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-06-01更新
|
202次组卷
|
2卷引用:河北省石家庄市2024届普通高中学校高三毕业年级教学质量检测(三)化学试卷
名校
解题方法
3 . 由金属钛、铝形成的Tebbe试剂(一种烃基钛茂)常用作有机反应的烯化试剂,其结构如图所示。下列说法错误的是
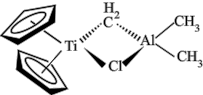
| A.Tebbe试剂为极性分子 | B.该结构中电负性最大的元素是Cl |
C.Tebbe试剂中的Al采取 杂化 杂化 | D.该结构中Al与Cl之间形成配位键 |
您最近一年使用:0次
名校
4 . 用化学知识解答问题:
(1)铜器在潮湿的空气中,表面会慢慢地生成一层铜锈(碱式碳酸铜),该反应的化学方程式为___________ 。
(2)在日常生活中常用一些铝制器皿,在清洗铝制器皿表面的污垢时,不能使用热的碱性溶液的原因时(用化学方程式解释)___________ 。
(3)发射卫星的火箭用联氨( )作燃料,以四氧化二氮作氧化剂,燃烧尾气由氮气与水蒸气组成,该反应的化学方程式为
)作燃料,以四氧化二氮作氧化剂,燃烧尾气由氮气与水蒸气组成,该反应的化学方程式为___________ 。
(4)比较甲酸、乙酸、丙酸的酸性大小,并解释原因___________
(5)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据如下表所示:
比较两元素的 、
、 可知,气态
可知,气态 再失去1个电子比气态
再失去1个电子比气态 再失去1个电子难,对此你的解释是
再失去1个电子难,对此你的解释是___________ 。
(1)铜器在潮湿的空气中,表面会慢慢地生成一层铜锈(碱式碳酸铜),该反应的化学方程式为
(2)在日常生活中常用一些铝制器皿,在清洗铝制器皿表面的污垢时,不能使用热的碱性溶液的原因时(用化学方程式解释)
(3)发射卫星的火箭用联氨(
 )作燃料,以四氧化二氮作氧化剂,燃烧尾气由氮气与水蒸气组成,该反应的化学方程式为
)作燃料,以四氧化二氮作氧化剂,燃烧尾气由氮气与水蒸气组成,该反应的化学方程式为(4)比较甲酸、乙酸、丙酸的酸性大小,并解释原因
(5)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据如下表所示:
| 元素 | Mn | Fe | |
电离能/ |  | 717 | 759 |
 | 1509 | 1561 | |
 | 3248 | 2957 | |
 、
、 可知,气态
可知,气态 再失去1个电子比气态
再失去1个电子比气态 再失去1个电子难,对此你的解释是
再失去1个电子难,对此你的解释是
您最近一年使用:0次
2023-08-19更新
|
129次组卷
|
2卷引用:河北省昌黎第一中学2023届高三下学期第五次调研考试化学试题
5 . 磷酸氯喹在细胞水平上能有效抑制新型冠状病毒的感染,其结构如图所示。回答下列问题:
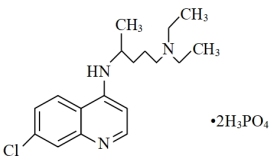
(1)C、N、O三种元素第一电离能从大到小的顺序为____ ;电负性P___ Cl(填“>”或“<”)。
(2)磷酸氯喹中N原子的杂化方式为___ ,NH3极易溶于水,且沸点比AsH3的沸点高,其原因是___ 。
(3)磷化镓与砷化镓是两种由ⅢA族元素与ⅤA族元素人工合成的Ⅲ-Ⅴ族化合物半导体材料,其晶胞结构可看作金刚石晶胞内部的碳原子被P(As)原子代替,顶点和面心的碳原子被Ga原子代替。
①基态Ga原子核外电子排布式为___ 。
②磷化镓晶体中含有的化学键类型为___ (填字母)。
A.离子键 B.配位键 C.σ键 D.π键 E.极性键 F.非极性键
③磷化镓与砷化镓具有相似的晶体结构,其中熔点较高的是___ (填化学式),原因是___ 。
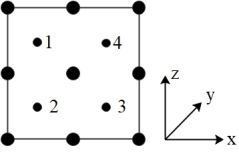
④以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。如图为沿y轴投影的磷化镓晶胞中所有原子的分布图。若原子1的原子分数坐标为(0.25,0.25,0.75),则原子3的原子分数坐标为___ ;若磷化镓的晶体密度为ρg•cm-3,阿伏加德罗常数的值为NA,则晶胞中Ga和P原子的最近距离为___ pm(用代数式表示)。

(1)C、N、O三种元素第一电离能从大到小的顺序为
(2)磷酸氯喹中N原子的杂化方式为
(3)磷化镓与砷化镓是两种由ⅢA族元素与ⅤA族元素人工合成的Ⅲ-Ⅴ族化合物半导体材料,其晶胞结构可看作金刚石晶胞内部的碳原子被P(As)原子代替,顶点和面心的碳原子被Ga原子代替。
①基态Ga原子核外电子排布式为
②磷化镓晶体中含有的化学键类型为
A.离子键 B.配位键 C.σ键 D.π键 E.极性键 F.非极性键
③磷化镓与砷化镓具有相似的晶体结构,其中熔点较高的是
④以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。如图为沿y轴投影的磷化镓晶胞中所有原子的分布图。若原子1的原子分数坐标为(0.25,0.25,0.75),则原子3的原子分数坐标为

您最近一年使用:0次
名校
解题方法
6 . 物质结构决定物质性质。下列性质差异与结构因素匹配错误的是
| 选项 | 性质差异 | 结构因素 |
| A | 沸点:正丁烷(0.5℃)高于异丁烷(11.7℃) | 范德华力 |
| B | 熔点: (399℃,易升华)低于 (399℃,易升华)低于 (714℃) (714℃) | 离子键强弱 |
| C | 酸性: 强于 强于 | 羟基极性 |
| D | 溶解性: 易溶于水, 易溶于水, 难溶于水 难溶于水 | 分子间氢键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-05-22更新
|
189次组卷
|
2卷引用:2024届河北省保定市唐县第一中学高三下学期二模化学试题
7 .  为原子序数依次增大的短周期元素,其中仅
为原子序数依次增大的短周期元素,其中仅 位于同一周期,X的s轨道电子数是p轨道电子数的2倍,
位于同一周期,X的s轨道电子数是p轨道电子数的2倍,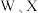 的最外层电子数之和等于Y的最外层电子数,基态Z原子有1个未成对电子。下列说法错误的是
的最外层电子数之和等于Y的最外层电子数,基态Z原子有1个未成对电子。下列说法错误的是
 为原子序数依次增大的短周期元素,其中仅
为原子序数依次增大的短周期元素,其中仅 位于同一周期,X的s轨道电子数是p轨道电子数的2倍,
位于同一周期,X的s轨道电子数是p轨道电子数的2倍,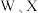 的最外层电子数之和等于Y的最外层电子数,基态Z原子有1个未成对电子。下列说法错误的是
的最外层电子数之和等于Y的最外层电子数,基态Z原子有1个未成对电子。下列说法错误的是A.电负性: |
| B.X与Z形成的化合物空间构型是三角锥形 |
| C.Y的第一电离能大于同周期相邻元素 |
| D.只有W元素处于s区 |
您最近一年使用:0次
8 . 短周期元素X、Y、Z、W的原子序数依次增大,X、W位于同主族但不相邻,基态Z原子价层电子排布式为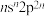 ,
, 是生活中常见的食品发泡剂。下列叙述正确的是
是生活中常见的食品发泡剂。下列叙述正确的是
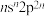 ,
, 是生活中常见的食品发泡剂。下列叙述正确的是
是生活中常见的食品发泡剂。下列叙述正确的是A.电负性: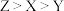 | B.第一电离能: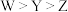 |
C.最简单氢化物的键角: | D.熔点: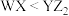 |
您最近一年使用:0次
2024-05-13更新
|
145次组卷
|
2卷引用:2024届河北省邯郸市高三下学期第四次调研检测化学试卷
名校
9 . 脱羧反应是有机化学中的重要反应,制备氰化物的脱羧反应如图所示。下列说法正确的是
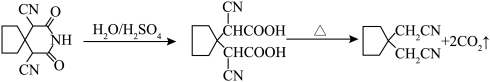
| A.电负性:S>O>N>C>H | B. 的空间填充模型为 的空间填充模型为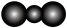 |
C.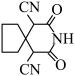 分子中有两个手性碳原子 分子中有两个手性碳原子 | D. 分子中C有2种杂化方式 分子中C有2种杂化方式 |
您最近一年使用:0次
解题方法
10 . 氟代硼铍酸钾晶体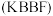 是一种非线性光学晶体材料,能够将激光转化为史无前例的176纳米波长(深紫外)激光,从而可以制造出深紫外固体激光器。回答下列问题:
是一种非线性光学晶体材料,能够将激光转化为史无前例的176纳米波长(深紫外)激光,从而可以制造出深紫外固体激光器。回答下列问题:
(1)基态K原子核外电子排布式为___________ ,在该原子中,原子轨道能量: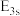
___________ (填“>”或“<”,下同)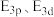
___________ 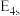 。
。
(2)上述四种元素中,第一电离能最小的是___________ (填元素符号,下同),电负性最大的是___________ 。
(3) 的空间构型为
的空间构型为___________ , 的杂化类型为
的杂化类型为___________ , 的键角比
的键角比 的键角
的键角___________ (填“大”或“小”),用价层电子对互斥理论解释原因为___________ 。
(4)已知晶体硼的熔、沸点及硬度数据和基本结构单元(由硼原子组成的正二十面体如图所示,每个三角形均为正三角形,每个顶点为一个硼原子)如下:
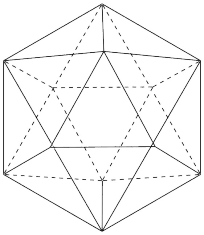
①晶体硼属于___________ 晶体,其理由是___________ 。
②每一个硼基本单元由___________ 个原子组成。
(5)已知 晶体具有
晶体具有 型结构,在
型结构,在 测出
测出 晶体密度为
晶体密度为 。
。 晶胞边长为
晶胞边长为___________  (阿伏加德罗常数用
(阿伏加德罗常数用 表示)。
表示)。
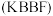 是一种非线性光学晶体材料,能够将激光转化为史无前例的176纳米波长(深紫外)激光,从而可以制造出深紫外固体激光器。回答下列问题:
是一种非线性光学晶体材料,能够将激光转化为史无前例的176纳米波长(深紫外)激光,从而可以制造出深紫外固体激光器。回答下列问题:(1)基态K原子核外电子排布式为
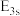
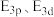
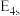 。
。(2)上述四种元素中,第一电离能最小的是
(3)
 的空间构型为
的空间构型为 的杂化类型为
的杂化类型为 的键角比
的键角比 的键角
的键角(4)已知晶体硼的熔、沸点及硬度数据和基本结构单元(由硼原子组成的正二十面体如图所示,每个三角形均为正三角形,每个顶点为一个硼原子)如下:
| 晶体 | 金刚石 | 晶体硅 | 晶体硼 |
| 熔点(K) | 3832 | 1683 | 2573 |
| 沸点(K) | 5100 | 2628 | 3823 |
| 硬度 | 10 | 7.0 | 9.6 |

①晶体硼属于
②每一个硼基本单元由
(5)已知
 晶体具有
晶体具有 型结构,在
型结构,在 测出
测出 晶体密度为
晶体密度为 。
。 晶胞边长为
晶胞边长为 (阿伏加德罗常数用
(阿伏加德罗常数用 表示)。
表示)。
您最近一年使用:0次



