1 . X、Y、Z、W是原子序数依次增大的4种短周期元素,由这4种元素组成的常见物质转化关系如图所示(反应条件略去),已知m是单质,Q是由三种元素组成的盐。下列推断错误的是
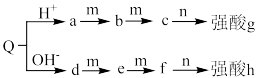

A.元素电负性: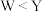 | B.Q可能是酸式盐 |
C.物质沸点: | D.b、c、e、f都是极性分子 |
您最近一年使用:0次
2024-04-02更新
|
470次组卷
|
2卷引用:2024届山东省枣庄市高三下学期模拟考试(二调)化学试题
解题方法
2 . 短周期元素X、Y、Z、W原子序数依次增大。基态X原子有两个单电子,Z的简单离子在同周期离子中半径最小,基态W原子的价电子排布式为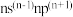 ,且Y、W同主族。
,且Y、W同主族。
下列说法错误的是
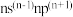 ,且Y、W同主族。
,且Y、W同主族。下列说法错误的是
| A.电负性:Y>W>X>Z | B.四种元素均位于元素周期表的p区 |
| C.简单氢化物沸点:X<Y<W | D.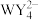 、 、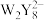 中W的化合价相同 中W的化合价相同 |
您最近一年使用:0次
2023-05-10更新
|
556次组卷
|
2卷引用:山东省枣庄市2023届高三第三次模拟考试化学试题
名校
3 . 短周期元素X、Y、Z、W位于同一周期,W元素的某种单质具有强氧化性,可用于杀菌消毒。四种元素组成的一种离子结构如图所示。下列说法错误的是
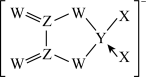
| A.电负性:Y<Z<W<X |
| B.简单氢化物的熔沸点:Z<X |
| C.Y的最高价氧化物的水化物为强酸 |
| D.阴离子中各原子均满足最外层8电子稳定结构 |
您最近一年使用:0次
2022-04-16更新
|
906次组卷
|
5卷引用:山东省枣庄市2022届高三第二次模拟化学试题
2010·山东枣庄·一模
4 . 研究物质的微观结构,有助于人们理解物质变化的本质。请回答下列问题。
(1)C、Si、N元素的电负性由大到小的顺序是___________________________ 。C60和金刚石都是碳的同素异形体,金刚石熔点高于C60熔点,原因是__________________________________________________________________________ 。
(2)A、B均为短周期金属元素。依据下表数据和已学知识,
写出B原子的电子排布式:___________________________ 。
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般地,为d0或d10排布时,无颜色;为d1~d9排布时,有颜色,如[Co(H2O) 6]2+显粉红色。据此判断,[Mn(H2O) 6]]2+_______ (填“无”或“有”)颜色。
(4)利用CO可以合成化工原料COCl2、络合物Fe(CO)5等。
①已知COCl2分子的结构式为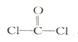 ,则 COCl2分子内含
,则 COCl2分子内含_______ (填标号)。
A.4个 键
键
B.2个 键、2个
键、2个 键
键
C.2个 键、1个
键、1个 键
键
D.3个 键、1个
键、1个 键
键
②Fe(CO)5在一定条件下发生分解反应:Fe(CO)5=Fe(s)+5CO,反应过程中,断裂的化学键只有配位键,形成的化学键是___________ 。
(1)C、Si、N元素的电负性由大到小的顺序是
(2)A、B均为短周期金属元素。依据下表数据和已学知识,
| 电离能/KJ·mol-1 | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
写出B原子的电子排布式:
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般地,为d0或d10排布时,无颜色;为d1~d9排布时,有颜色,如[Co(H2O) 6]2+显粉红色。据此判断,[Mn(H2O) 6]]2+
(4)利用CO可以合成化工原料COCl2、络合物Fe(CO)5等。
①已知COCl2分子的结构式为
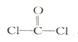 ,则 COCl2分子内含
,则 COCl2分子内含A.4个
 键
键B.2个
 键、2个
键、2个 键
键C.2个
 键、1个
键、1个 键
键D.3个
 键、1个
键、1个 键
键②Fe(CO)5在一定条件下发生分解反应:Fe(CO)5=Fe(s)+5CO,反应过程中,断裂的化学键只有配位键,形成的化学键是
您最近一年使用:0次
2013·山东枣庄·一模
解题方法
5 . 卤族元素是典型的非金属元素,包括F、Cl、Br、I等。请回答下面有关问题
(1)同主族元素的电负性大小存在一定的规律,卤族元素F、Cl、Br、I的电负性由小到大的顺序是_____ 。
(2)Br原子的M层核外电子排布式为_________ 。
(3)用价层电子对互斥理论判断BeCl2的构型为________ ,BF3分子中B-F键的键角为________ 。
(4)CCl4分子中碳原子的杂化方式为______ ,NF3分子的空间构型为_______ 。
(5)F、Mg、K三种元素形成的晶体晶胞结构如图所示,一个晶胞中 Mg元素的质量分数为________ 。

(1)同主族元素的电负性大小存在一定的规律,卤族元素F、Cl、Br、I的电负性由小到大的顺序是
(2)Br原子的M层核外电子排布式为
(3)用价层电子对互斥理论判断BeCl2的构型为
(4)CCl4分子中碳原子的杂化方式为
(5)F、Mg、K三种元素形成的晶体晶胞结构如图所示,一个晶胞中 Mg元素的质量分数为

您最近一年使用:0次



