名校
解题方法
1 . 氮族元素可以形成多种多样的化合物,回答下列问题:
(1)基态As原子的价电子的轨道表示式是______ 。
(2)叠氮酸(HN3)常用于引爆剂,可用联氨( )制取。比较联氨与双氧水分子中键角大小:
)制取。比较联氨与双氧水分子中键角大小:
______ 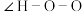 (填“>”、“=”或“<”,下同)。叠氮酸结构如图所示:
(填“>”、“=”或“<”,下同)。叠氮酸结构如图所示: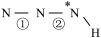 ,
, 为
为 杂化,已知参与形成π键的电子越多,键长越短,则键长;①
杂化,已知参与形成π键的电子越多,键长越短,则键长;①______ ②。
(3)乙胺( )和2-羟基乙胺(
)和2-羟基乙胺( )都可用于染料的合成,乙胺碱性更强,原因是
)都可用于染料的合成,乙胺碱性更强,原因是______ 。
(4)磷酸一氢盐受热易脱水聚合,生成环状的偏磷酸根。环状三偏磷酸根的结构如图所示,则由n个磷氧四面体连接形成的环状偏磷酸根的通式是______ 。

(5)砷与金属钠、铁、铜可形成一种绝缘体材料,其晶胞结构图钠原子沿z轴投影如图所示,已知m原子的分数坐标为 ,晶胞参数为
,晶胞参数为 ,
, 。铜周围距离最近的砷原子的个数是
。铜周围距离最近的砷原子的个数是______ ,n原子的分数坐标是______ ,若阿伏加德罗常数值为 ,该晶体密度是
,该晶体密度是______  (用含
(用含 的代数式表示)。
的代数式表示)。
(1)基态As原子的价电子的轨道表示式是
(2)叠氮酸(HN3)常用于引爆剂,可用联氨(
 )制取。比较联氨与双氧水分子中键角大小:
)制取。比较联氨与双氧水分子中键角大小:
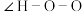 (填“>”、“=”或“<”,下同)。叠氮酸结构如图所示:
(填“>”、“=”或“<”,下同)。叠氮酸结构如图所示: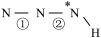 ,
, 为
为 杂化,已知参与形成π键的电子越多,键长越短,则键长;①
杂化,已知参与形成π键的电子越多,键长越短,则键长;①(3)乙胺(
 )和2-羟基乙胺(
)和2-羟基乙胺( )都可用于染料的合成,乙胺碱性更强,原因是
)都可用于染料的合成,乙胺碱性更强,原因是(4)磷酸一氢盐受热易脱水聚合,生成环状的偏磷酸根。环状三偏磷酸根的结构如图所示,则由n个磷氧四面体连接形成的环状偏磷酸根的通式是

(5)砷与金属钠、铁、铜可形成一种绝缘体材料,其晶胞结构图钠原子沿z轴投影如图所示,已知m原子的分数坐标为
 ,晶胞参数为
,晶胞参数为 ,
, 。铜周围距离最近的砷原子的个数是
。铜周围距离最近的砷原子的个数是 ,该晶体密度是
,该晶体密度是 (用含
(用含 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
2024-05-21更新
|
475次组卷
|
2卷引用:山东省潍坊市2024届高三下学期二模化学试题
解题方法
2 . X、Y、Z为短周期主族元素,化合物 是一种有机中间体,与水发生剧烈反应生成强酸HX和一种常见的温室气体
是一种有机中间体,与水发生剧烈反应生成强酸HX和一种常见的温室气体 。下列说法正确的是
。下列说法正确的是
 是一种有机中间体,与水发生剧烈反应生成强酸HX和一种常见的温室气体
是一种有机中间体,与水发生剧烈反应生成强酸HX和一种常见的温室气体 。下列说法正确的是
。下列说法正确的是A.电负性: 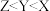 |
| B.基态Z原子和Y原子的未成对电子数相等 |
C. 的空间构型为三角锥形 的空间构型为三角锥形 |
D. 的分子中, 的分子中, 键与 键与 键个数比为2:1 键个数比为2:1 |
您最近一年使用:0次
2023-05-27更新
|
322次组卷
|
2卷引用:山东省潍坊市2023届高三下学期三模化学试题
解题方法
3 . 一种阴离子的结构如图所示,X、Y、Z、W为原子序数依次增大的短周期元素,基态W原子中有3个未成对电子,下列说法正确的是
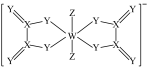
A.电负性: | B.简单氢化物的沸点: |
C.最高价氧化物对应水化物的酸性: | D.单质的氧化性: |
您最近一年使用:0次
名校
解题方法
4 . W、X、Y、Z、M是原子序数依次增大的前四周期元素,其元素性质或结构如下:
回答下列问题:
(1)写出X元素的名称_______ 。
(2)写出M元素+2价离子的价电子轨道表示式_______ 。
(3)基态Z元素原子核外电子占据的最高能层包含的原子轨道数为_______ 。
(4)W、X、Z可形成强还原性物质 ,W、X、Z三种元素电负性由大到小的顺序是
,W、X、Z三种元素电负性由大到小的顺序是_______ (用元素符号表示)。
(5)大π键可用符号 表示,m为参与形成大π键的原子数目,n为平行p轨道里的电子数,如苯分子的大
表示,m为参与形成大π键的原子数目,n为平行p轨道里的电子数,如苯分子的大 键写作
键写作 ,石墨中的大π键写作
,石墨中的大π键写作 (见下图a),
(见下图a), 被称为“无机苯”,结构与苯类似,写出
被称为“无机苯”,结构与苯类似,写出 的大π键
的大π键_______ ,某化合物XY的结构(见下图b)中也存在 的大π键,但石墨是电的良导体,XY却具有优异的电绝缘性,从电负性角度分析化合物XY不导电的可能原因
的大π键,但石墨是电的良导体,XY却具有优异的电绝缘性,从电负性角度分析化合物XY不导电的可能原因_______ 。

| 元素 | 元素性质或原子结构 |
| W | 电子只有一种自旋取向 |
| X | 核外只有一个未成对电子,且电子有三种空间运动状态 |
| Y | s轨道电子数比p轨道多一个,且第一电离能大于同周期相邻元素 |
| Z | 电负性是短周期中最小的 |
| M | +3价基态离子最高能级处于半满状态 |
(1)写出X元素的名称
(2)写出M元素+2价离子的价电子轨道表示式
(3)基态Z元素原子核外电子占据的最高能层包含的原子轨道数为
(4)W、X、Z可形成强还原性物质
 ,W、X、Z三种元素电负性由大到小的顺序是
,W、X、Z三种元素电负性由大到小的顺序是(5)大π键可用符号
 表示,m为参与形成大π键的原子数目,n为平行p轨道里的电子数,如苯分子的大
表示,m为参与形成大π键的原子数目,n为平行p轨道里的电子数,如苯分子的大 键写作
键写作 ,石墨中的大π键写作
,石墨中的大π键写作 (见下图a),
(见下图a), 被称为“无机苯”,结构与苯类似,写出
被称为“无机苯”,结构与苯类似,写出 的大π键
的大π键 的大π键,但石墨是电的良导体,XY却具有优异的电绝缘性,从电负性角度分析化合物XY不导电的可能原因
的大π键,但石墨是电的良导体,XY却具有优异的电绝缘性,从电负性角度分析化合物XY不导电的可能原因
您最近一年使用:0次
2023-02-23更新
|
643次组卷
|
2卷引用:2024届山东省潍坊市昌乐二中高三模拟预测化学试题
名校
解题方法
5 . “点击化学”研究获得2022年诺贝尔化学奖表彰,利用该原理可制得如图所示含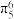 大π键的产物。已知杂化轨道中s成分越多,所形成的化学键越稳定。下列说法错误的是
大π键的产物。已知杂化轨道中s成分越多,所形成的化学键越稳定。下列说法错误的是
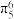 大π键的产物。已知杂化轨道中s成分越多,所形成的化学键越稳定。下列说法错误的是
大π键的产物。已知杂化轨道中s成分越多,所形成的化学键越稳定。下列说法错误的是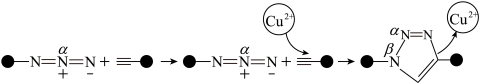
| A.铜离子降低了反应的活化能 |
| B.反应物中黑球元素的电负性强于N |
| C.产物中α、β两位置的N原子中,α位置的N原子更容易形成配位键 |
| D.反应物中氮氮键比产物中氮氮键的键长短 |
您最近一年使用:0次
2023-02-22更新
|
0次组卷
|
2卷引用:山东省潍坊市2023届高三下学期一模考试化学试题
6 . 化合物R是一种用于有机合成的催化剂,其网状结构片段如图。X、Y、Z、W为原子序数依次增大的短周期主族元素,四种元素原子序数之和为29,W的第一电离能大于同周期相邻元素。下列说法正确的是
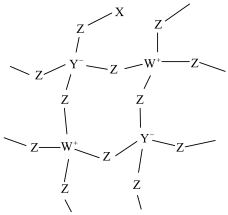

| A.电负性:W>Y>X |
B.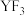 中各原子均满足8电子稳定结构 中各原子均满足8电子稳定结构 |
| C.同周期元素形成的单质中,Z的氧化性最强 |
| D.化合物R中Y、Z、W原子的杂化类型相同 |
您最近一年使用:0次
7 . 下列关于B、S、C及其化合物的结构与性质的论述错误的是
| A.C的电负性比B大,则C、B形成的二元化合物中,C显负化合价 |
B. 和 和 中B、S杂化轨道类型相同,二者均为正三角形结构 中B、S杂化轨道类型相同,二者均为正三角形结构 |
C.常温下 为液体,说明 为液体,说明 是非极性分子 是非极性分子 |
D.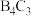 的硬度可与金刚石媲美,且熔点高,则 的硬度可与金刚石媲美,且熔点高,则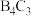 为共价晶体 为共价晶体 |
您最近一年使用:0次
名校
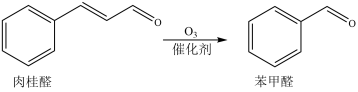
8 . 某科研团队研究用不同金属氧化物催化肉桂醛制苯甲醛(反应如下,部分产物略去)。反应时间和其它条件相同时,测得实验数据如下表。
已知:i.选择性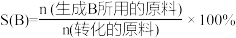
ii. 与
与 同主族。
同主族。
下列说法不正确 的是

| 催化剂 | 金属元素的电负性 | 肉桂醛转化率/% | 苯甲醛选择性/% |
 | 0.9 | 80.79 | 71.93 |
 | 1.0 | 78.27 | 60.51 |
 | 1.5 | 74.21 | 54.83 |
 | 1.6 | 76.46 | 48.57 |
 | 1.9 | 75.34 | 41.71 |
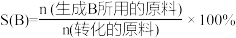
ii.
 与
与 同主族。
同主族。下列说法
| A.肉桂醛制苯甲醛的反应属于氧化反应 |
B.用 作催化剂可以获得比用 作催化剂可以获得比用 更大的主反应速率 更大的主反应速率 |
C.使用 作催化剂时,反应后副产物最多 作催化剂时,反应后副产物最多 |
| D.金属氧化物中金属元素的电负性越小,苯甲醛选择性越好 |
您最近一年使用:0次
2022-04-01更新
|
652次组卷
|
5卷引用:山东省潍坊市2022届高三下学期5月模拟考试(二)化学试题
9 . 2021年9月24日《科学》杂志发表了我国科学家的原创性重大突破,首次在实验室实现从CO2到淀粉的全合成。其合成路线如下:
CO2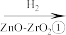 CH3OH
CH3OH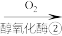
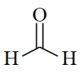
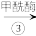
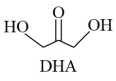
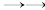
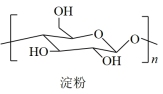
下列说法错误的是
CO2
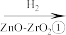 CH3OH
CH3OH



下列说法错误的是
| A.电负性:O>C>H>Zn |
| B.甲醇分子中H-C-O键角小于甲醛分子中H-C-O键角 |
| C.DHA分子间存在氢键 |
| D.Zn溶于氨水形成配合物[Zn(NH3)4](OH)2,Zn2+的配位数为6 |
您最近一年使用:0次
2022-03-04更新
|
944次组卷
|
3卷引用:山东省潍坊市2022届高三普通高等学校招生全国统一考试(一模)化学试题
山东省潍坊市2022届高三普通高等学校招生全国统一考试(一模)化学试题(已下线)回归教材重难点11 物质结构与性质-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)新疆石河子第一中学2021-2022学年高二4月月考化学试题
解题方法
10 . 某种水性钠离子电池电极材料由Na+、Fe2+、Fe3+、CN-组成,其立方晶胞嵌入和嵌出Na+过程中,Fe2+与Fe3+含量发生变化,依次变为格林绿、普鲁士蓝、普鲁士白三种物质,其过程如图所示。
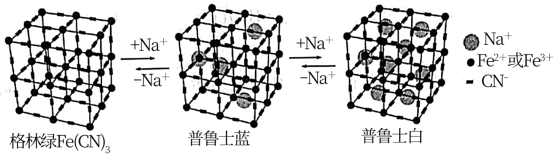
回答下列问题:
(1)基态Fe3+价电子轨道表示式是_______ 。
(2)(CN)2与卤素单质性质相似,与水反应生成HCN,请写出(CN)2的电子式_______ ,H、C、N三种元素电负性由大到小的顺序为_______ 。
(3)HCN中σ键与π键个数比为_______ 。已知沸点: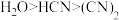 ,解释原因
,解释原因_______ 。
(4)下列微粒中,与HCN具有相同立体构型的是_______ (填字母)。
A. B.
B. C.
C. D.
D.
(5)普鲁士蓝中Fe2+与Fe3+个数比为_______ 。已知普鲁士白晶胞的晶胞参数均为apm,晶体密度为 ,设NA为阿伏加德罗常数的值,则普鲁士白(化学式为最简比值)的摩尔质量为
,设NA为阿伏加德罗常数的值,则普鲁士白(化学式为最简比值)的摩尔质量为_______  (用含a、
(用含a、 、NA的计算式表示)
、NA的计算式表示)

回答下列问题:
(1)基态Fe3+价电子轨道表示式是
(2)(CN)2与卤素单质性质相似,与水反应生成HCN,请写出(CN)2的电子式
(3)HCN中σ键与π键个数比为
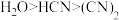 ,解释原因
,解释原因(4)下列微粒中,与HCN具有相同立体构型的是
A.
 B.
B. C.
C. D.
D.
(5)普鲁士蓝中Fe2+与Fe3+个数比为
 ,设NA为阿伏加德罗常数的值,则普鲁士白(化学式为最简比值)的摩尔质量为
,设NA为阿伏加德罗常数的值,则普鲁士白(化学式为最简比值)的摩尔质量为 (用含a、
(用含a、 、NA的计算式表示)
、NA的计算式表示)
您最近一年使用:0次



