16. 研究含氮元素物质的反应对生产、生活、科研等方面具有重要的意义.回答下列问题:
(1)已知:
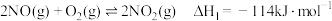
;

;
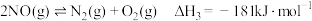
.

与

反应生成

和

的热化学方程式为
___________。
(2)

的排放主要来自于汽车尾气,包含

和

,有人提出用活性炭对

进行吸收.对于反应:

时,借助传感器测得反应在不同时间点上各物质的浓度如下:

| 0 | 10 | 20 | 30 | 40 | 50 |

| 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |

| 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
①
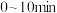
内,

的平均反应速率
 ___________
___________,当升高反应温度,该反应的平衡常数K
___________(选填“增大”“减小”或“不变”)。
②

后,只改变某一条件,反应重新达到平衡;根据上表中的数据判断改变的条件可能是
___________(填字母)。
A.加入一定量的活性炭B.通入一定量的

C.适当缩小容器的体积D.加入合适的催化剂
(3)为避免汽车尾气中的氮氧化合物对大气的污染,需给汽车安装尾气净化装置.在净化装置中

和

发生反应
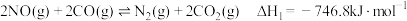
.实验测得:

,其中

分别为正、逆反应速率常数,只与温度有关;p为气体分压(分压=物质的量分数×总压).
①达到平衡后,仅升高温度,

增大的倍数
___________(选填“大于”、“小于”或“等于”)

增大的倍数。
②一定温度下在刚性密闭容器中充入

和

物质的量之比为
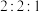
,压强为

.达平衡时压强为
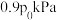
,此时
 ___________
___________
。
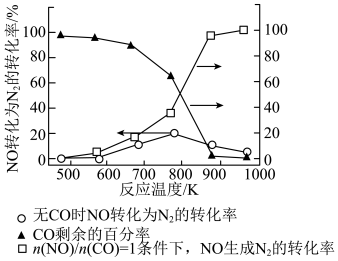
(4)某研究小组在实验室以耐高温催化剂催化

转化为

,测得

转化为

的转化率随温度变化情况如图所示.结合(1)中的反应,用平衡移动原理解释加入

后,

转化为

的转化率增大的原因:
____________________________。