名校
解题方法
1 . 物质的结构决定其性质。下列事实与解释相符的是
| 选项 | 事实 | 解释 |
| A | 一氟乙酸的 大于一溴乙酸 大于一溴乙酸 |  的电负性比 的电负性比 的大 的大 |
| B |  原子间难以形成 原子间难以形成 键 键 |  的原子半径较大,未杂化的 的原子半径较大,未杂化的 轨道很难重叠 轨道很难重叠 |
| C |  是非极性分子 是非极性分子 |  原子处在4个 原子处在4个 原子所组成的正方形中心,键的极性的向量和为零 原子所组成的正方形中心,键的极性的向量和为零 |
| D | 干冰的熔点低于 | 2个 键的键能之和小于4个 键的键能之和小于4个 键的键能之和 键的键能之和 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
2 . X、Y、Z、W是原子序数依次增大的短周期元素,X、Y可以构成 ,W的价电子排布式为
,W的价电子排布式为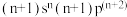 ,Z、W同主族且能构成如图所示的阴离子
,Z、W同主族且能构成如图所示的阴离子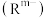 。以下说法正确的是
。以下说法正确的是

 ,W的价电子排布式为
,W的价电子排布式为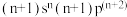 ,Z、W同主族且能构成如图所示的阴离子
,Z、W同主族且能构成如图所示的阴离子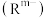 。以下说法正确的是
。以下说法正确的是
A. 中存在配位键 中存在配位键 | B. 有很好的热稳定性 有很好的热稳定性 |
| C.电负性Y>Z>W>X | D.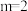 |
您最近半年使用:0次
3 . X、Y、Z、W是原子序数依次增大的4种短周期元素,由这4种元素组成的常见物质转化关系如图所示(反应条件略去),已知m是单质,Q是由三种元素组成的盐。下列推断错误的是
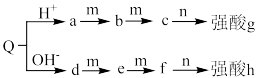

A.元素电负性: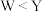 | B.Q可能是酸式盐 |
C.物质沸点: | D.b、c、e、f都是极性分子 |
您最近半年使用:0次
2024-04-02更新
|
428次组卷
|
2卷引用:2024届山东省枣庄市高三下学期模拟考试(二调)化学试题
4 . 现有属于前四周期的A、B、C、D、E、F、G七种元素,原子序数依次增大。基态A元素原子的价电子排布式为 ;C元素为最活泼的非金属元素;D元素原子核外有三个电子层,最外层电子数是核外电子总数的
;C元素为最活泼的非金属元素;D元素原子核外有三个电子层,最外层电子数是核外电子总数的 ;E元素正三价离子的3d轨道为半充满状态;F元素基态的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒。
;E元素正三价离子的3d轨道为半充满状态;F元素基态的M层全充满,N层没有成对电子,只有一个未成对电子;G元素与A元素位于同一主族,其某种氧化物有剧毒。
(1)A元素的第一电离能
(2)基态D元素原子的价电子排布式为
(3)基态C元素原子的电子排布图为
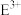 的离子符号为
的离子符号为(4)F元素位于元素周期表的
(5)G元素可能的性质是______(填字母)。
| A.其单质可作为半导体材料 | B.其电负性大于磷 |
| C.其原子半径大于锗 | D.其第一电离能小于硒 |
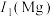
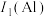 ,其原因是
,其原因是
您最近半年使用:0次
2024-03-26更新
|
68次组卷
|
2卷引用:山东省枣庄薛城实验中学等校2023-2023学年高二上学期12月大联考化学试题
解题方法
5 . 如图为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述,正确的是
| X | |||
| W | Y | R | |
| Z |
| A.W元素的第一电离能小于Y元素的第一电离能 |
| B.Y、Z的阴离子电子层结构都与R原子的相同 |
| C.p能级未成对电子最多的是W元素 |
| D.X元素是电负性最大的元素 |
您最近半年使用:0次
2024-03-26更新
|
28次组卷
|
2卷引用:山东省枣庄薛城实验中学等校2023-2023学年高二上学期12月大联考化学试题
名校
解题方法
6 . 下列关于物质结构和性质的说法正确的是
A.第2周期元素中,第一电离能介于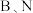 之间的有1种 之间的有1种 |
B.酸性: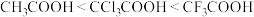 |
C. 与 与 中心原子的杂化方式相同,均为 中心原子的杂化方式相同,均为 形结构 形结构 |
D.乙二胺 的沸点比三甲胺 的沸点比三甲胺 高的原因是乙二胺存在分子间氢键,三甲胺存在分子内氢键 高的原因是乙二胺存在分子间氢键,三甲胺存在分子内氢键 |
您最近半年使用:0次
2024-03-21更新
|
514次组卷
|
3卷引用:山东省滕州市第一中学2023-2024学年高二下学期3月月考化学试题
7 . 第ⅣA族元素中 是生物分子骨架的构成元素,
是生物分子骨架的构成元素, 、
、 可用作半导体材料。下列有关说法错误的是
可用作半导体材料。下列有关说法错误的是
 是生物分子骨架的构成元素,
是生物分子骨架的构成元素, 、
、 可用作半导体材料。下列有关说法错误的是
可用作半导体材料。下列有关说法错误的是| A.三种元素原子的次外层电子排布均是全充满状态 |
B.第一电离能: |
C. 与 与 中氢元素化合价不相同 中氢元素化合价不相同 |
D.原子半径 的原因是电子层数增加对半径的影响大于核电荷数增加的影响 的原因是电子层数增加对半径的影响大于核电荷数增加的影响 |
您最近半年使用:0次
8 . 2022年诺贝尔化学奖授予美国学者卡罗琳·贝尔托齐,丹麦学者莫滕·梅尔达尔,美国学者卡尔·巴里·沙普利斯,以表彰他们“对点击化学和生物正交化学的发展”的贡献。点击化学的代表反应为铜催化的叠氮一炔基环加成反应, 、
、 、
、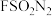 等均是点击化学中常用无机试剂。下列说法错误的是
等均是点击化学中常用无机试剂。下列说法错误的是
 、
、 、
、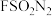 等均是点击化学中常用无机试剂。下列说法错误的是
等均是点击化学中常用无机试剂。下列说法错误的是A.基态 原子的最高能层符号为 原子的最高能层符号为 |
B.若将基态 原子的电子排布式写成 原子的电子排布式写成 ,则违反了能量最低原理 ,则违反了能量最低原理 |
C. 的电子式为 的电子式为 |
D.电负性: |
您最近半年使用:0次
9 . 一种新型漂白剂(结构如图)可用于漂白羊毛等,其中W、Y、Z为不同周期不同主族的短周期元素,Z电子只有一种自旋取向;W、Y、Z的最外层电子数之和等于X的最外层电子数,X基态原子核外有两个单电子,W、X对应的简单离子核外电子排布相同。

回答下列问题:
(1)写出元素Y在周期表中的位置是:_______ ,所属分区是:_____ 。
(2)写出元素X简单离子的核外电子排布式:________ 。
(3)元素X基态原子核外电子的运动状态有_____ 种,占据的原子轨道有____ 个。
(4)W、X、Y电负性由大到小的顺序是_______ (用元素符号表示)。
(5)试解释W的第一电离能大于 的第一电离能的原因:
的第一电离能的原因:___________ 。

回答下列问题:
(1)写出元素Y在周期表中的位置是:
(2)写出元素X简单离子的核外电子排布式:
(3)元素X基态原子核外电子的运动状态有
(4)W、X、Y电负性由大到小的顺序是
(5)试解释W的第一电离能大于
 的第一电离能的原因:
的第一电离能的原因:
您最近半年使用:0次
10 . 我国自主设计生产的长征系列运载火箭使用偏二甲肼( )作燃料,(
)作燃料,( )作氧化剂。下列相关说法正确的是
)作氧化剂。下列相关说法正确的是
 )作燃料,(
)作燃料,( )作氧化剂。下列相关说法正确的是
)作氧化剂。下列相关说法正确的是| A.N、O、C的电负性依次减小 |
B.基态N原子的轨道表示式为 |
| C.O原子有5种空间运动状态不同的电子 |
| D.C、N、O三种基态原子的第一电离能依次增大 |
您最近半年使用:0次



