名校
解题方法
1 . FeSO4·7H2O的结构如图,下列说法错误的是

| A.键角:①>② | B.H2O与Fe2+、H2O与 的作用力类型相同 的作用力类型相同 |
| C.Fe2+的配位数是6 | D.电负性:O>S>H |
您最近半年使用:0次
名校
解题方法
2 . 立方氮化硼硬度高,耐磨性好,在机械加工行业有广泛应用。制备立方氮化硼的一种方法为 ,下列说法错误的是
,下列说法错误的是
 ,下列说法错误的是
,下列说法错误的是| A.反应混合物中所有化学键均为共价键 |
| B.元素电负性大小为Cl>N>B |
C. 和BN均为共价晶体 和BN均为共价晶体 |
D.形成 时B原子先激发后杂化,其激发态价电子轨道表示式为: 时B原子先激发后杂化,其激发态价电子轨道表示式为: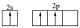 |
您最近半年使用:0次
名校
解题方法
3 . 下列化合物中碳原子的电负性最大的是
| A.乙烷 | B.乙炔 | C.乙烯 | D.甲烷 |
您最近半年使用:0次
名校
解题方法
4 . 元素周期表前四周期A、B、C、D、E五种元素,A元素的原子最外层电子排布式为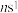 ;B元素的原子价层电子排布式为
;B元素的原子价层电子排布式为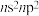 ;C元素位于第二周期且原子中p能级与s能级电子总数相等;D元素原子的M能层的p能级中有3个未成对电子;E元素的原子有5个未成对电子。
;C元素位于第二周期且原子中p能级与s能级电子总数相等;D元素原子的M能层的p能级中有3个未成对电子;E元素的原子有5个未成对电子。
(1)C基态原子的轨道表示式为___________ 。
(2)当 时,B的最简单气态氢化物的电子式为
时,B的最简单气态氢化物的电子式为________ , 分子的结构式是
分子的结构式是________ ;当 时,B与C形成的化合物与氢氧化钠溶液反应的离子方程式是
时,B与C形成的化合物与氢氧化钠溶液反应的离子方程式是________ 。
(3)若A元素的原子最外层电子排布式为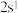 ,B元素的原子价层电子排布式为
,B元素的原子价层电子排布式为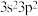 ,A、B、C、D四种元素的电负性由大到小的顺序是
,A、B、C、D四种元素的电负性由大到小的顺序是________ (用元素符号表示)。
(4)E元素原子的价层电子排布式是___________ ,在元素周期表中的位置是___________ ,其最高价氧化物的化学式是___________ 。
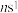 ;B元素的原子价层电子排布式为
;B元素的原子价层电子排布式为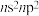 ;C元素位于第二周期且原子中p能级与s能级电子总数相等;D元素原子的M能层的p能级中有3个未成对电子;E元素的原子有5个未成对电子。
;C元素位于第二周期且原子中p能级与s能级电子总数相等;D元素原子的M能层的p能级中有3个未成对电子;E元素的原子有5个未成对电子。(1)C基态原子的轨道表示式为
(2)当
 时,B的最简单气态氢化物的电子式为
时,B的最简单气态氢化物的电子式为 分子的结构式是
分子的结构式是 时,B与C形成的化合物与氢氧化钠溶液反应的离子方程式是
时,B与C形成的化合物与氢氧化钠溶液反应的离子方程式是(3)若A元素的原子最外层电子排布式为
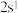 ,B元素的原子价层电子排布式为
,B元素的原子价层电子排布式为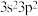 ,A、B、C、D四种元素的电负性由大到小的顺序是
,A、B、C、D四种元素的电负性由大到小的顺序是(4)E元素原子的价层电子排布式是
您最近半年使用:0次
名校
解题方法
5 . 下列有关物质结构与性质的比较正确的是
A.分子的极性: | B.酸性: |
C.键角: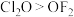 | D.基态原子未成对电子数:Mn>Cr |
您最近半年使用:0次
2023-12-16更新
|
592次组卷
|
5卷引用:山东省新泰市第一中学东校2023-2024学年高三上学期第二次月考化学试题
名校
解题方法
6 . 元素B、Al、Ga位于周期表中IIIA族。下列说法正确的是
A.原子半径: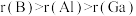 |
B.第一电离能: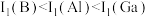 |
C.BN、 、 、 均为共价晶体 均为共价晶体 |
| D.可在周期表中元素Al附近寻找既能和酸又能和碱反应的金属 |
您最近半年使用:0次
2023-12-04更新
|
268次组卷
|
3卷引用:山东省泰安市宁阳四中2023-2024学年高二上学期期末化学模拟试卷
7 . 有机物种类繁多,应用广泛。
(1)邻氨基吡啶(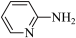 )的铜配合物在有机不对称合成中起催化诱导效应。邻氨基吡啶中所有元素的电负性由大到小的顺序为
)的铜配合物在有机不对称合成中起催化诱导效应。邻氨基吡啶中所有元素的电负性由大到小的顺序为_______ (填元素符号)。 能溶于水的原因是
能溶于水的原因是_______ 。
(2)鸟嘌呤和吡咯的结构如下图所示。
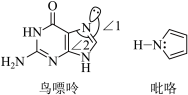
①鸟嘌呤中N原子的杂化方式为_______ ,夹角∠1_______ ∠2(填“>”或“<”)。
②分子中的大 键可以用符号
键可以用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数,吡咯中的大
键的电子数,吡咯中的大 键可表示为
键可表示为_______ 。
(3)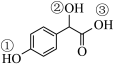 分子中3个-OH的电离能力由强到弱的顺序是
分子中3个-OH的电离能力由强到弱的顺序是_______ (用①、②、③表示)。
(4)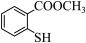 与
与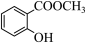 相比,前者的水溶性更
相比,前者的水溶性更_______ (填“大”或“小”)。—SH与—OH性质相似,写出与NaOH溶液反应的化学方程式_______ 。
(1)邻氨基吡啶(
 )的铜配合物在有机不对称合成中起催化诱导效应。邻氨基吡啶中所有元素的电负性由大到小的顺序为
)的铜配合物在有机不对称合成中起催化诱导效应。邻氨基吡啶中所有元素的电负性由大到小的顺序为 能溶于水的原因是
能溶于水的原因是(2)鸟嘌呤和吡咯的结构如下图所示。

①鸟嘌呤中N原子的杂化方式为
②分子中的大
 键可以用符号
键可以用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数,吡咯中的大
键的电子数,吡咯中的大 键可表示为
键可表示为(3)
 分子中3个-OH的电离能力由强到弱的顺序是
分子中3个-OH的电离能力由强到弱的顺序是(4)
 与
与 相比,前者的水溶性更
相比,前者的水溶性更
您最近半年使用:0次
2023-07-11更新
|
323次组卷
|
2卷引用:山东省泰安市2022-2023学年高二下学期期末考试化学试题
名校
解题方法
8 . 氯化铜是共价化合物,通常用作有机和无机反应催化剂、媒染剂等。 溶液与乙二胺(
溶液与乙二胺( )可形成配离子
)可形成配离子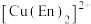 (En是乙二胺的简写),如图所示,下列说法中错误的是
(En是乙二胺的简写),如图所示,下列说法中错误的是
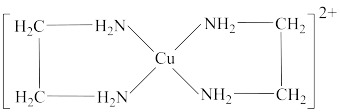
 溶液与乙二胺(
溶液与乙二胺( )可形成配离子
)可形成配离子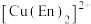 (En是乙二胺的简写),如图所示,下列说法中错误的是
(En是乙二胺的简写),如图所示,下列说法中错误的是
A.基态 的未成对电子数为1 的未成对电子数为1 |
B.配离子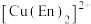 中N原子提供孤对电子 中N原子提供孤对电子 |
C.乙二胺和三甲胺 均属于胺,沸点更高的是三甲胺 均属于胺,沸点更高的是三甲胺 |
D.配离子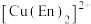 中涉及的元素的电负性由大到小的顺序为N>C>H>Cu 中涉及的元素的电负性由大到小的顺序为N>C>H>Cu |
您最近半年使用:0次
2023-05-21更新
|
427次组卷
|
3卷引用:山东省泰安市2023届高三下学期三模化学试题
9 . 某多孔储氢材料前驱体结构如图,M、W、X、Y、Z五种元素原子序数依次增大,基态Z原子的电子填充了3个能级,其中有2个未成对电子。下列说法正确的是


| A.Y的氢化物为H2Y |
| B.原子半径:M<X<Y<Z |
| C.第一电离能:W<X<Y<Z |
| D.电负性:W<X<Y<Z |
您最近半年使用:0次
2023-05-02更新
|
191次组卷
|
2卷引用:山东省泰安第一中学2023-2024学年高二上学期12月月考化学试题
10 . 依据原子结构知识回答下列问题。
(1)下列说法错误的是_______ 。
A.电负性:Si<H<C<N
B.离子半径: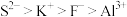
C.原子的未成对电子数: Cr>Mn>Si>Br
D.第二周期中元素原子的第一电离能介于B和N之间的元素有2种
E.前四周期元素中,基态原子中价电子数与其所在周期数相同的元素有4种
(2)基态S原子的价电子轨道表示式为_______ ,其电子占据的最高能层符号为_______ ,其价电子中两种自旋状态的电子数之比为_______ 。
(3)基态F原子核外电子的空间运动状态有_______ 种。下列属于F原子激发态的电子排布式是_______ (填标号,下同),其中能量较高的是_______ 。
A.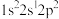 b.
b. c.
c. d.
d.
(4)Cr元素位于元素周期表_______ 区。Cr与Mn相比,第二电离能与第一电离能差值更大的是_______ ,原因是_______ 。
(1)下列说法错误的是
A.电负性:Si<H<C<N
B.离子半径:
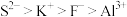
C.原子的未成对电子数: Cr>Mn>Si>Br
D.第二周期中元素原子的第一电离能介于B和N之间的元素有2种
E.前四周期元素中,基态原子中价电子数与其所在周期数相同的元素有4种
(2)基态S原子的价电子轨道表示式为
(3)基态F原子核外电子的空间运动状态有
A.
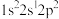 b.
b. c.
c. d.
d.
(4)Cr元素位于元素周期表
您最近半年使用:0次
2023-02-11更新
|
409次组卷
|
2卷引用:山东省泰安市新泰第一中学老校区2023-2024学年高二上学期第三次月考化学试题



