名校
解题方法
1 . 硫酸亚铁铵[ ]在定量分析中常用来标定重铬酸钾或高锰酸钾溶液,还用于医药和电镀等方面。下列说法正确的是
]在定量分析中常用来标定重铬酸钾或高锰酸钾溶液,还用于医药和电镀等方面。下列说法正确的是
 ]在定量分析中常用来标定重铬酸钾或高锰酸钾溶液,还用于医药和电镀等方面。下列说法正确的是
]在定量分析中常用来标定重铬酸钾或高锰酸钾溶液,还用于医药和电镀等方面。下列说法正确的是A.第二电离能大小: | B.电负性大小: |
C.半径大小: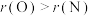 | D.简单气态氢化物稳定性: |
您最近半年使用:0次
2 . M、X、Y、Z四种短周期主族元素,M为金属元素,X、Y和Z为非金属元素,原子序数Z<X<M<Y。M在常压下可生成 :
: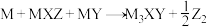 ,其中
,其中 为无色无味气体,反应消耗
为无色无味气体,反应消耗 的同时可获得标准状况下
的同时可获得标准状况下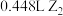 ,
, 可表示成
可表示成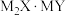 形式。下列说法正确的是
形式。下列说法正确的是
 :
: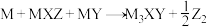 ,其中
,其中 为无色无味气体,反应消耗
为无色无味气体,反应消耗 的同时可获得标准状况下
的同时可获得标准状况下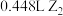 ,
, 可表示成
可表示成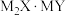 形式。下列说法正确的是
形式。下列说法正确的是| A.基态M原子核外电子空间运动状态有6种 |
| B.电负性:X<Y |
C.Z与X能组合成非极性分子 |
D. 与水反应能得到含有离子键和极性共价键的产物 与水反应能得到含有离子键和极性共价键的产物 |
您最近半年使用:0次
名校
解题方法
3 . 铁的配合物在生产、生活中有重要应用,某种铁的配合物结构如图所示,下列说法正确的是
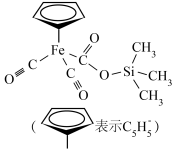

| A.基态硅原子最高能级轨道形状为球形 |
| B.该配合物中元素的电负性最大的是氧 |
| C.该配合物中碳原子的杂化方式有3种 |
| D.基态铁原子核外电子有26种空间运动状态 |
您最近半年使用:0次
2023-05-03更新
|
176次组卷
|
2卷引用:山东省青岛市西海岸新区2022-2023学年高一下学期期中考试化学试题
4 . 短周期元素W、X、Y、Z原子序数依次增大,其中基态W原子核外电子只有一种运动状态,X、Y位于同一周期,基态X原子核外s能级电子数是p能级电子数的4倍。四种元素能形成如图所示结构的化合物M是一种优良的漂白剂、杀菌剂。下列说法错误的是
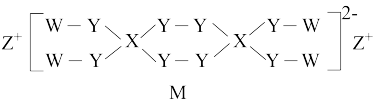

A.M阴离子中的各原子均满足 稳定结构 稳定结构 | B.M因含有 价的Y元素而具有强氧化性 价的Y元素而具有强氧化性 |
C.电负性由大到小的顺序为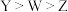 | D.工业上常通过电解Z的氯化物水溶液制备Z单质 |
您最近半年使用:0次
解题方法
5 . 化合物A (结构如下图)由原子序数依次增大的X、Y、Z、W短周期元素组成,常用来做金属矿物的浮选剂。已知Z与W位于不同周期。下列说法正确的是


| A.四种元素中X的电负性最小 |
| B.最简单气态氢化物的稳定性:Z<Y |
| C.W位于周期表的第二周期VIA族 |
| D.四种元素可组成既含离子键又含共价键的化合物 |
您最近半年使用:0次
2023-02-14更新
|
313次组卷
|
2卷引用:河北省唐山市2022-2023学年高二上学期期末考试化学试题
6 . 甲醛检测试剂盒常用来检测室内空气中甲醛,其原理是甲醛与MBTH反应生成物质A,物质A再发生一系列反应,最终生成蓝绿色化合物,有关转化如图。下列说法正确的是


| A.上述有机物涉及的元素中氮元素的电负性最强 |
| B.甲醛分子结构为平面三角形 |
| C.物质A中的C、N、S一定位于同一个平面内 |
| D.1molMBTH中σ键的数目为22NA |
您最近半年使用:0次
7 . 下列说法正确的是
| A.AlCl3固体是金属元素与非金属元素形成的共价化合物,形成了共价晶体 |
| B.电负性越大,元素的非金属性越强,第一电离能也越大 |
| C.在N2中有1个σ键和2个π键 |
| D.乙醇分子与水分子间存在范德华力和氢键 |
您最近半年使用:0次
8 . 五种短周期元素X、Y、Z、L、M的某些性质如下表所示,下列判断错误的是
| 元素 | X | Y | Z | L | M |
| 最低化合价 | -4 | -2 | -1 | -2 | 0 |
| 电负性 | 2.5 | 2.5 | 3.0 | 3.5 | 1.0 |
| A.基态X原子的核外电子共占据3个原子轨道 |
| B.Z在周期表中的位置为第2周期第VIIA族 |
| C.借助电负性数值预测:YLZ2加入水中可生成YL2 |
| D.元素L、M可形成离子化合物 |
您最近半年使用:0次
2022-01-22更新
|
199次组卷
|
2卷引用:山东省滨州市2021-2022学年高二上学期期末考试化学试题
2021高三·全国·专题练习
9 . 对于基态Cr原子,下列叙述正确的是
| A.轨道处于半充满时体系总能量低,核外电子排布应为[Ar]3d54s1 |
| B.4s电子能量较高,总是在比3d电子离核更远的地方运动 |
| C.电负性比钾高,原子对键合电子的吸引力比钾大 |
您最近半年使用:0次



