1 . 下列元素或化合物的性质变化顺序不正确的是
A.第一电离能: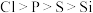 |
B.电负性: |
C.价层电子对互斥理论中, 键电子对数计入中心原子的价层电子对数 键电子对数计入中心原子的价层电子对数 |
| D.第四周期元素中,锰原子价电子层中未成对电子数最多 |
您最近半年使用:0次
名校
解题方法
2 . 物质的结构决定其性质。下列事实与解释相符的是
| 选项 | 事实 | 解释 |
| A | 一氟乙酸的 大于一溴乙酸 大于一溴乙酸 |  的电负性比 的电负性比 的大 的大 |
| B |  原子间难以形成 原子间难以形成 键 键 |  的原子半径较大,未杂化的 的原子半径较大,未杂化的 轨道很难重叠 轨道很难重叠 |
| C |  是非极性分子 是非极性分子 |  原子处在4个 原子处在4个 原子所组成的正方形中心,键的极性的向量和为零 原子所组成的正方形中心,键的极性的向量和为零 |
| D | 干冰的熔点低于 | 2个 键的键能之和小于4个 键的键能之和小于4个 键的键能之和 键的键能之和 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
3 . SiCl4与N-甲基咪唑(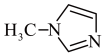 )反应可以得到M2+,其结构如图所示:
)反应可以得到M2+,其结构如图所示:
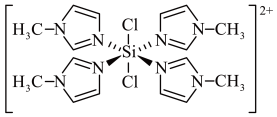
| A.N-甲基咪唑分子中氮原子的杂化轨道类型为sp2和sp3 |
| B.H、C、N的电负性由大到小的顺序为N>C>H |
| C.1个M2+中含有54个σ键(包括配键) |
| D.中心原子硅的氧化数为+6 |
您最近半年使用:0次
名校
4 . “点击化学”研究获得2022年诺贝尔化学奖,用该原理可制得如图含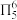 大
大 键的产物。已知杂化轨道中s成分越多,所形成的化学键越稳定。下列说法错误为是
键的产物。已知杂化轨道中s成分越多,所形成的化学键越稳定。下列说法错误为是
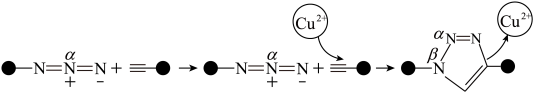
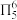 大
大 键的产物。已知杂化轨道中s成分越多,所形成的化学键越稳定。下列说法错误为是
键的产物。已知杂化轨道中s成分越多,所形成的化学键越稳定。下列说法错误为是
| A.铜离子增大了反应的活化能 |
| B.反应物中黑球元素的电负性强于N |
C.产物中 、 、 两位置中的N原子中, 两位置中的N原子中, 位置的N原子更容易形成配位键 位置的N原子更容易形成配位键 |
| D.反应物中氮氮键比产物中氮氮键的键长短 |
您最近半年使用:0次
解题方法
5 . 如图为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述,正确的是
| X | |||
| W | Y | R | |
| Z |
| A.W元素的第一电离能小于Y元素的第一电离能 |
| B.Y、Z的阴离子电子层结构都与R原子的相同 |
| C.p能级未成对电子最多的是W元素 |
| D.X元素是电负性最大的元素 |
您最近半年使用:0次
2024-03-26更新
|
25次组卷
|
2卷引用:山东省枣庄薛城实验中学等校2023-2023学年高二上学期12月大联考化学试题
名校
6 . 超分子笼PPC-2封装钌(Ru)纳米颗粒形成一种高效催化剂。PPC-2是由A、B、C三个组件拼装而成的正八面体超分子笼,结构示意如图。下列说法不正确的是
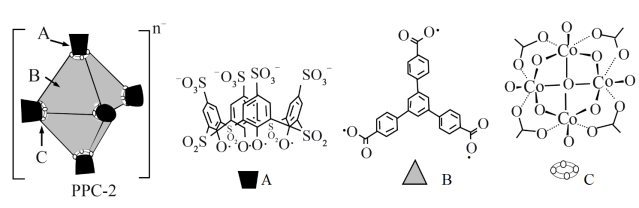

| A.组件A中所含四种元素的电负性由小到大的顺序为H<C<S<O |
B.组件B中碳原子的杂化类型均为 杂化 杂化 |
| C.组件C中Co原子位于相邻O原子构成的四面体空隙中 |
| D.每个组件C带一个单位负电荷,综合各组件所带电荷,计算PPC-2中n=30 |
您最近半年使用:0次
7 . 以下有关元素性质的说法不正确的是
| A.具有下列电子排布式的原子:①1s22s22p63s23p2 ②1s22s22p3 ③1s22s22p2 ④1s22s22p63s23p4,原子半径最大的是④ |
| B.具有下列价电子排布式的原子:①3s23p1 ②3s23p2 ③3s23p3 ④3s23p4,第一电离能最大的是③ |
| C.①Na、K、Rb ②N、P、S ③Na、P、Cl,元素的电负性随原子序数增大而增大的是③ |
| D.某主族元素气态基态离子的逐级电离能数据(单位:kJ·mol-1)分别为738、1451、7733、10540、13630、17995、21703……它与氯气反应时,生成的阳离子是X3+ |
您最近半年使用:0次
名校
解题方法
8 . 现有四种元素的基态原子的核外电子排布式如下:
①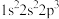 ;②
;② ;③
;③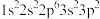 ;④
;④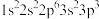 。下列说法错误的是
。下列说法错误的是
①
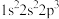 ;②
;② ;③
;③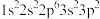 ;④
;④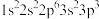 。下列说法错误的是
。下列说法错误的是| A.电负性:②>①>④>③ | B.原子半径:③>④>①>② |
| C.简单气态氢化物的稳定性:①>②>③>④ | D.第一电离能:②>①>④>③ |
您最近半年使用:0次
9 . 某种新型储氢材料的晶胞如图,八面体中心M为铁元素金属离子,顶点均为 配体;四面体中心为硼原子,顶点均为氢原子,下列说法正确的是
配体;四面体中心为硼原子,顶点均为氢原子,下列说法正确的是
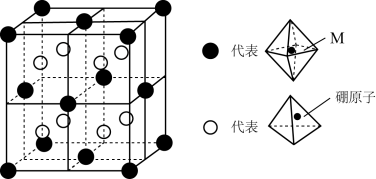
 配体;四面体中心为硼原子,顶点均为氢原子,下列说法正确的是
配体;四面体中心为硼原子,顶点均为氢原子,下列说法正确的是
A.黑球微粒的化学式为 | B.白球微粒中存在配位键,硼原子提供空轨道 |
C.晶体中 分子间可能存在氢键作用 分子间可能存在氢键作用 | D.晶体中所含元素的电负性大小顺序为N>B>H>Fe |
您最近半年使用:0次
名校
解题方法
10 . 下列实验操作、现象与结论均正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 向盛有2mL0.5mol/LNaOH溶液中先滴加2滴0.1mol/LMgCl2溶液,再滴加2滴0.1mol/LFeCl3溶液 | 先出现白色沉淀,后沉淀变为红褐色 | 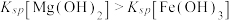 |
| B | 向盛有少量Mg(OH)2沉淀的试管中加入适量饱和CH3COONH4溶液,振荡 | 白色沉淀溶解 |  结合了OH-,促使Mg(OH)2溶解平衡正移 结合了OH-,促使Mg(OH)2溶解平衡正移 |
| C | 用玻璃棒蘸取NaHCO3溶液点在pH试纸上 | 试纸变红 |  的电离程度大于水解程度 的电离程度大于水解程度 |
| D | 比较电负性:室温下,用pH计测定0.1mol·L-1的CF3COOH、CCl3COOH两种溶液的pH | CF3COOH溶液的pH较小 | F元素的电负性大于Cl元素 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次



