名校
解题方法
1 . A、B、C、D、E、F、G是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如表所示,请用化学用语回答下列问题。
(1)元素F简单离子的价电子排布式为___________ ;写出元素G在周期表中的位置___________ 。
(2)B与氢元素形成的简单气态氢化物的空间构型为___________ ,C与氢元素形成的简单气态氢化物的VSEPR模型为___________ 。
(3)C、D、E三种元素的简单离子半径由大到小的顺序为___________ (用元素符号表示)。
(4)已知元素A、B形成的 分子中所有原子都满足8电子稳定结构,则
分子中所有原子都满足8电子稳定结构,则 中σ键与π键之比为
中σ键与π键之比为___________ 。
(5)短周期元素M与D同族,已知元素M、F的电负性分别为1.5和3.0,预测它们形成的化合物是___________ 化合物(填“离子”或“共价”);M的最高价氧化物对应的水化物与NaOH溶液反应的化学方程式为___________ 。
(6)FC—常用作消毒剂,单质砷(As)在碱性溶液中可被FC—氧化为AsO ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
| A | 原子核外有6种不同运动状态的电子 |
| C | 基态原子中s电子总数与p电子总数相等 |
| D | 电离能数据(单位: ):738、1451、7733、10540、13630…… ):738、1451、7733、10540、13630…… |
| E | 基态原子最外层电子排布式为: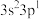 |
| F | 基态原子的最外层p轨道上2个电子的自旋状态与其他电子的自旋状态相反 |
| G | 其中一种氧化物是有磁性的黑色固体 |
(2)B与氢元素形成的简单气态氢化物的空间构型为
(3)C、D、E三种元素的简单离子半径由大到小的顺序为
(4)已知元素A、B形成的
 分子中所有原子都满足8电子稳定结构,则
分子中所有原子都满足8电子稳定结构,则 中σ键与π键之比为
中σ键与π键之比为(5)短周期元素M与D同族,已知元素M、F的电负性分别为1.5和3.0,预测它们形成的化合物是
(6)FC—常用作消毒剂,单质砷(As)在碱性溶液中可被FC—氧化为AsO
 ,该反应的离子方程式为
,该反应的离子方程式为
您最近一年使用:0次
名校
2 . 下列叙述正确的是
| A.CO2与SiO2分别熔化,克服的粒子间作用力相同 |
| B.KCN和K2S分别与FeCl3溶液反应,反应的类型相同 |
C. 和O3分别净水,净水的原理相同 和O3分别净水,净水的原理相同 |
| D.CuO和Cu2O分别与稀硝酸反应,生成的产物相同 |
您最近一年使用:0次
解题方法
3 . 分银渣是电解铜的阳极泥提取贵金属后的尾渣,含有铅(PbSO4)、钡(BaSO4)、锡(SnO2)以及金(Au)、银(Ag)等有价金属,具有较高的综合利用价值。一种分银渣的提取流程如下:
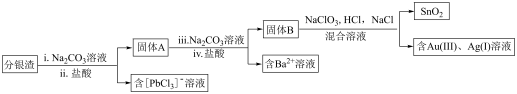
已知:
I.SnO2不溶于水、醇、稀酸和碱液;
Ⅱ.部分难溶电解质的溶度积(25℃)如表。
(1)PbSO4中Pb元素的价层电子排布式为___________________ ,[PbCl3]-离子的空间结构为_________________ 。
(2)步骤i反应后Pb(Ⅱ)的存在形式是________________ (填化学式)。
(3)ⅲ操作中用饱和Na2CO3溶液(1.6mol·L-1)浸泡固体A并煮沸,充分反应后过滤,若固体A中含0.2molBaSO4,要将其全部转化为BaCO3,至少需要加入________________ L饱和Na2CO3溶液(保留一位小数)。
(4)固体B经混合溶液同步浸出Au、Ag生成H[AuCl4]和Na2[AgCl3],Ag发生反应的化学方程式为________________ 。
(5)测定SnO2样品的纯度:称取mgSnO2样品(杂质不影响滴定结果),将样品灰化后以过氧化钠熔融,将熔融物酸溶后,再用还原铁粉将SnO2转化为Sn2+,加入指示剂,用KIO3标准溶液进行滴定,滴定反应离子方程式为: ,
,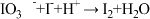 (均未配平)。
(均未配平)。
①该滴定实验中所加指示剂为_______________ ,滴定终点的现象为_______________ 。
②若终点时消耗0.0100mol·L-1KIO3标准溶液VmL,则测得SnO2纯度为_______________ (列出表达式即可)。

已知:
I.SnO2不溶于水、醇、稀酸和碱液;
Ⅱ.部分难溶电解质的溶度积(25℃)如表。
| 物质 | PbSO4 | PbCO3 | PbCl2 | BaSO4 | BaCO3 |
| Ksp | 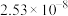 | 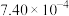 | 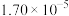 |  | 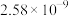 |
(1)PbSO4中Pb元素的价层电子排布式为
(2)步骤i反应后Pb(Ⅱ)的存在形式是
(3)ⅲ操作中用饱和Na2CO3溶液(1.6mol·L-1)浸泡固体A并煮沸,充分反应后过滤,若固体A中含0.2molBaSO4,要将其全部转化为BaCO3,至少需要加入
(4)固体B经混合溶液同步浸出Au、Ag生成H[AuCl4]和Na2[AgCl3],Ag发生反应的化学方程式为
(5)测定SnO2样品的纯度:称取mgSnO2样品(杂质不影响滴定结果),将样品灰化后以过氧化钠熔融,将熔融物酸溶后,再用还原铁粉将SnO2转化为Sn2+,加入指示剂,用KIO3标准溶液进行滴定,滴定反应离子方程式为:
 ,
,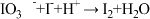 (均未配平)。
(均未配平)。①该滴定实验中所加指示剂为
②若终点时消耗0.0100mol·L-1KIO3标准溶液VmL,则测得SnO2纯度为
您最近一年使用:0次
名校
解题方法
4 . 下列化学用语或图示表达正确的是
A.HClO的电子式为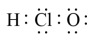 |
B.基态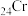 原子的价层电子轨道表示式为 原子的价层电子轨道表示式为 |
C.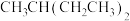 的名称为2—乙基丁烷 的名称为2—乙基丁烷 |
D. 分子的VSEPR模型为 分子的VSEPR模型为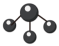 |
您最近一年使用:0次
2024-04-04更新
|
1133次组卷
|
5卷引用:重庆市名校联盟2023-2024学年高三下学期全真模拟考试化学试题
重庆市名校联盟2023-2024学年高三下学期全真模拟考试化学试题北京市第八中学2023-2024学年高三下学期零模化学试题(已下线)题型2 有关化学用语的正误判断(25题)-2024年高考化学常考点必杀300题(新高考通用)北京师范大学附属中学2023-2024学年高三下学期统练 化学试题山东省惠民县2023-2024学年高二下学期期中考试化学试题
5 . 工业上以菱锰矿(主要成分为MnCO3,含杂质CaCO3、FeCO3、NiCO3)为原料制取金属锰的工艺流程如下:
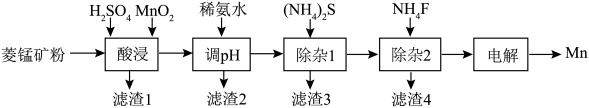
已知常温下,溶度积常数(Ksp)如下表:
(1)基态Mn2+的价层电子轨道表示式为___________ , 的空间结构为
的空间结构为___________ 。
(2)“酸浸”时,为了加快反应速率,可采取的措施有___________ (答两条),该过程一般选择硫酸而不用盐酸的原因是___________ 。
(3)“酸浸”过程中,MnO2发生的主要反应的离子方程式为___________ 。
(4)常温下,加稀氨水时调pH约为4,则滤渣2的主要成分是___________ 。
(5)“除杂1”时加入适量的(NH4)2S,除去的主要离子为___________ ,过滤后得到的滤液中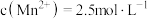 ,则其
,则其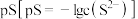 的范围是
的范围是___________ 。

已知常温下,溶度积常数(Ksp)如下表:
 |  |  |  |  |  |
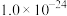 | 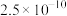 | 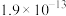 |  | 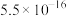 | 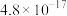 |
(1)基态Mn2+的价层电子轨道表示式为
 的空间结构为
的空间结构为(2)“酸浸”时,为了加快反应速率,可采取的措施有
(3)“酸浸”过程中,MnO2发生的主要反应的离子方程式为
(4)常温下,加稀氨水时调pH约为4,则滤渣2的主要成分是
(5)“除杂1”时加入适量的(NH4)2S,除去的主要离子为
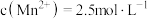 ,则其
,则其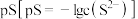 的范围是
的范围是
您最近一年使用:0次
解题方法
6 . 微颗粒的氧化锌作为一种纳米材料开始在相关领域发挥作用,利用锌焙砂 主要成分为
主要成分为 ,含
,含 及铅、铜、镉的氧化物
及铅、铜、镉的氧化物 生产高纯氧化锌的工业流程如图所示,回答下列问题:
生产高纯氧化锌的工业流程如图所示,回答下列问题:

已知: 微溶于水而生成亚砷酸
微溶于水而生成亚砷酸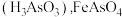 和
和 难溶于水。
难溶于水。
(1)基态 原子核外价层电子轨道表达式为
原子核外价层电子轨道表达式为______ , 中
中 的化合价为
的化合价为______ 。
(2)“浸出”过程中 足量,则生成的主要配离子的化学式为
足量,则生成的主要配离子的化学式为______ ;增大浸出率可采取的措施是______  写出两条
写出两条 。
。
(3)“除砷”过程中, 作氧化剂
作氧化剂 溶液呈酸性
溶液呈酸性 ,发生反应的离子方程式为
,发生反应的离子方程式为______ 。
(4)“除重金属”过程中加入 后
后 在溶液中的残留浓度为
在溶液中的残留浓度为 ,此时
,此时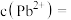
______ 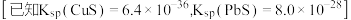 。
。
(5)“沉锌”前锌元素以 存在,写出“沉锌”的化学方程式
存在,写出“沉锌”的化学方程式______ 。
(6)流程中可循环利用的物质有 、
、______ 、______  填化学式
填化学式 。
。
 主要成分为
主要成分为 ,含
,含 及铅、铜、镉的氧化物
及铅、铜、镉的氧化物 生产高纯氧化锌的工业流程如图所示,回答下列问题:
生产高纯氧化锌的工业流程如图所示,回答下列问题:
已知:
 微溶于水而生成亚砷酸
微溶于水而生成亚砷酸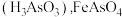 和
和 难溶于水。
难溶于水。(1)基态
 原子核外价层电子轨道表达式为
原子核外价层电子轨道表达式为 中
中 的化合价为
的化合价为(2)“浸出”过程中
 足量,则生成的主要配离子的化学式为
足量,则生成的主要配离子的化学式为 写出两条
写出两条 。
。(3)“除砷”过程中,
 作氧化剂
作氧化剂 溶液呈酸性
溶液呈酸性 ,发生反应的离子方程式为
,发生反应的离子方程式为(4)“除重金属”过程中加入
 后
后 在溶液中的残留浓度为
在溶液中的残留浓度为 ,此时
,此时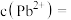
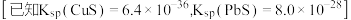 。
。(5)“沉锌”前锌元素以
 存在,写出“沉锌”的化学方程式
存在,写出“沉锌”的化学方程式(6)流程中可循环利用的物质有
 、
、 填化学式
填化学式 。
。
您最近一年使用:0次
名校
7 . 下列化学用语表示正确的是
A.基态 的价电子轨道表示式: 的价电子轨道表示式: |
B. 的空间填充模型: 的空间填充模型: |
C.3,4-二甲基-1,3-戊二烯的键线式: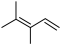 |
D. 的VSEPR模型: 的VSEPR模型: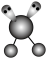 |
您最近一年使用:0次
2024-04-02更新
|
415次组卷
|
4卷引用:重庆市第八中学2023-2024学年高二下学期第一次月考化学试卷
名校
解题方法
8 . 下列化学用语或图示表达正确的是
A.HCl的电子式: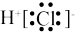 | B.基态碳原子的轨道表示式: |
C.中子数为7的氮原子: | D. 的VSEPR模型: 的VSEPR模型: |
您最近一年使用:0次
2024-04-01更新
|
430次组卷
|
5卷引用:重庆市松树桥中学校2023-2024学年高二下学期期中考试化学试题
解题方法
9 . 离子液体在化工领域具有广泛的应用前景。一种离子液体的结构如图所示,下列有关说法不正确的是
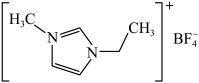
A.电负性: |
B.第一电离能: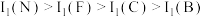 |
| C.该化合物的离子键弱,熔点低 |
D.该化合物中N原子发生 和 和 杂化 杂化 |
您最近一年使用:0次
名校
解题方法
10 . W、X、Y、Z、R、Q是前四周期元素,Q是第四周期中未成对电子数最多的元素。W、X、Y、R、Z原子半径依次增大,X元素无正价,X与R相邻,Y与Z相邻,W、Y、Z、Q均不在同一周期,四者最外层电子数之和为14。下列说法正确的是
| A.Y与W或X均能形成三角锥形分子 |
| B.简单离子半径:R>Z>X>Y |
| C.R元素氧化物的水化物均为强酸 |
| D.可用铝热反应冶炼Q的单质 |
您最近一年使用:0次



