名校
1 . 化合物甲(化学式可表示为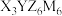 )是德国化学家L。 Leopold Gmelin于1882年发现的一种配合物,可用于颜料、钢铁等行业。X、Y、Z、M为前4周期主族或副族元素,四种元素原子的电子数总和为58;X、Y同周期,Z、M同周期相邻。基态X最高能层的原子轨道为球形,且只填充了1个电子;基态Y的价电子排布中有4个单电子。下列说法不正确的是
)是德国化学家L。 Leopold Gmelin于1882年发现的一种配合物,可用于颜料、钢铁等行业。X、Y、Z、M为前4周期主族或副族元素,四种元素原子的电子数总和为58;X、Y同周期,Z、M同周期相邻。基态X最高能层的原子轨道为球形,且只填充了1个电子;基态Y的价电子排布中有4个单电子。下列说法不正确的是
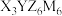 )是德国化学家L。 Leopold Gmelin于1882年发现的一种配合物,可用于颜料、钢铁等行业。X、Y、Z、M为前4周期主族或副族元素,四种元素原子的电子数总和为58;X、Y同周期,Z、M同周期相邻。基态X最高能层的原子轨道为球形,且只填充了1个电子;基态Y的价电子排布中有4个单电子。下列说法不正确的是
)是德国化学家L。 Leopold Gmelin于1882年发现的一种配合物,可用于颜料、钢铁等行业。X、Y、Z、M为前4周期主族或副族元素,四种元素原子的电子数总和为58;X、Y同周期,Z、M同周期相邻。基态X最高能层的原子轨道为球形,且只填充了1个电子;基态Y的价电子排布中有4个单电子。下列说法不正确的是A.第一电离能: |
| B.化合物甲中除含配位键,还含离子键、非极性键 |
C.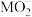 的VSEPR模型为三角形 的VSEPR模型为三角形 |
D.化合物甲的溶液可用于检验 |
您最近一年使用:0次
2024-04-27更新
|
87次组卷
|
2卷引用:重庆市部分学校2024年高三下学期考前最后一卷化学试题
名校
解题方法
2 . 某科研人员提出HCHO与 在羟基磷灰石(HAP)表面催化氧化生成
在羟基磷灰石(HAP)表面催化氧化生成 ,
, 的历程,该历程示意图如图(图中只画出了HAP的部分结构)所示。下列说法正确的是
的历程,该历程示意图如图(图中只画出了HAP的部分结构)所示。下列说法正确的是
 在羟基磷灰石(HAP)表面催化氧化生成
在羟基磷灰石(HAP)表面催化氧化生成 ,
, 的历程,该历程示意图如图(图中只画出了HAP的部分结构)所示。下列说法正确的是
的历程,该历程示意图如图(图中只画出了HAP的部分结构)所示。下列说法正确的是
A.HAP降低了该反应的焓变( ) ) |
| B.反应过程中,发生了非极性键的断裂和生成 |
C.HCHO在反应过程中,无 键发生断裂 键发生断裂 |
D. 和 和 的中心原子上所含孤电子对数不同 的中心原子上所含孤电子对数不同 |
您最近一年使用:0次
2024-04-26更新
|
381次组卷
|
5卷引用:重庆市渝西中学2023-2024学年高二下学期4月月考化学试题
名校
解题方法
3 . 氨硼烷(NH3BH3)在一定条件下与水反应: ,
, 的结构如图所示,下列说法正确的是
的结构如图所示,下列说法正确的是
 ,
, 的结构如图所示,下列说法正确的是
的结构如图所示,下列说法正确的是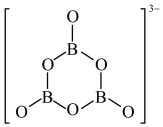
| A.NH3BH3分子中存在配位键,B原子提供孤电子对 |
| B.1molNH3BH3发生反应时转移3mole- |
| C.反应产物中只含有离子键、配位键和非极性共价键 |
| D.反应过程中B原子的杂化方式由sp2变为sp3 |
您最近一年使用:0次
2024-04-26更新
|
150次组卷
|
2卷引用:重庆市渝西中学2023-2024学年高二下学期4月月考化学试题
名校
解题方法
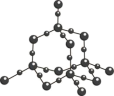
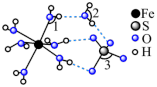
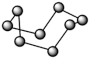
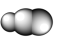
4 . 观察下列模型并结合信息,判断有关说法错误的是
| 石英 | FeSO4·7H2O | S8分子 | HCN |
|
|
|
|
| A.石英属于共价晶体,且两原子个数比为2:1 |
| B.FeSO4·7H2O结构中键角1、2、3由大到小的顺序:3>1>2 |
| C.固态硫S8中S原子为sp2杂化 |
D.HCN的结构式为 |
您最近一年使用:0次
名校
5 . 我国科技工作者用钾离子促进电催化合成尿素 可能的反应机理如图。与其他步骤相比,碳氮键的形成过程活化能更高。下列说法正确的是
可能的反应机理如图。与其他步骤相比,碳氮键的形成过程活化能更高。下列说法正确的是
 可能的反应机理如图。与其他步骤相比,碳氮键的形成过程活化能更高。下列说法正确的是
可能的反应机理如图。与其他步骤相比,碳氮键的形成过程活化能更高。下列说法正确的是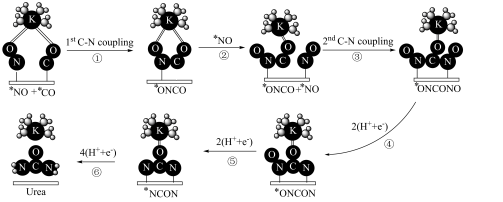
A.尿素中氮原子采取 杂化 杂化 | B.步骤①和③的反应速率较其他步骤快 |
| C.步骤⑥发生的是氧化反应 | D.以上过程中涉及极性键的形成和断裂 |
您最近一年使用:0次
名校
6 . 下列关于物质结构和性质的说法正确的是
A.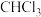 的球棍模型为 的球棍模型为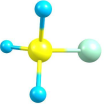 |
B.二氯化二硫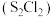 的电子式为 的电子式为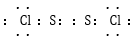 |
C. 的 的 模型与空间结构名称均为正四面体形 模型与空间结构名称均为正四面体形 |
D.酸性: |
您最近一年使用:0次
7 . 一种合金催化剂催化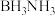 水解释氢的反应机理如图所示。下列说法正确的是
水解释氢的反应机理如图所示。下列说法正确的是
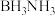 水解释氢的反应机理如图所示。下列说法正确的是
水解释氢的反应机理如图所示。下列说法正确的是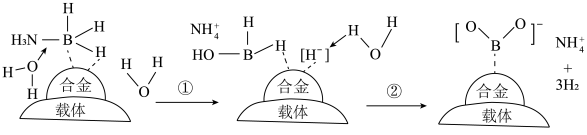
| A.使用催化剂增大反应的活化能和反应速率 |
| B.反应过程中B原子杂化方式不变 |
| C.反应过程中无配位键断裂 |
D.若将 换成 换成 ,则有HD和 ,则有HD和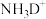 生成 生成 |
您最近一年使用:0次
8 . 氮、磷、砷等元素的单质及其化合物在生产生活中应用广泛。回答下列问题:
(1) 是一种优良的等离子蚀刻气体,在芯片制造、高能激光器方面有广泛应用,
是一种优良的等离子蚀刻气体,在芯片制造、高能激光器方面有广泛应用, 分子的空间构型为
分子的空间构型为________ .
(2)超高导热绝缘耐高温纳米氮化铝在绝缘材料中应用广泛,氮化铝晶体与金刚石类似,每个铝原子与_______ 个氮原子相连,氮化铝晶体属于__________ 晶体。
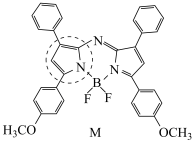
(3)M是氮杂氟硼二吡咯类物质,常用作光敏剂,其结构如图。 键,则虚线框中氮元素采用杂化方式为
键,则虚线框中氮元素采用杂化方式为_______ ,M中存在的微粒间作用力有_______ (填标号)。
A.共价键 B.离子键 C.氢键 D.配位键
(4) 是一种重要的半导体材料,晶胞结构如图1;将
是一种重要的半导体材料,晶胞结构如图1;将 掺杂到
掺杂到 的晶体中得到稀磁性半导体材料,如图2。
的晶体中得到稀磁性半导体材料,如图2。 ,则B原子的分数坐标为
,则B原子的分数坐标为_______ ;若 晶体密度为
晶体密度为 ,设
,设 为阿伏加德罗常数的值,则晶胞中两个
为阿伏加德罗常数的值,则晶胞中两个 原子间的最小距离为
原子间的最小距离为_________  (列出计算式即可);稀磁性半导体材料中
(列出计算式即可);稀磁性半导体材料中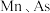 的原子个数比为
的原子个数比为_________ 。
(1)
 是一种优良的等离子蚀刻气体,在芯片制造、高能激光器方面有广泛应用,
是一种优良的等离子蚀刻气体,在芯片制造、高能激光器方面有广泛应用, 分子的空间构型为
分子的空间构型为(2)超高导热绝缘耐高温纳米氮化铝在绝缘材料中应用广泛,氮化铝晶体与金刚石类似,每个铝原子与
(3)M是氮杂氟硼二吡咯类物质,常用作光敏剂,其结构如图。
 键,则虚线框中氮元素采用杂化方式为
键,则虚线框中氮元素采用杂化方式为A.共价键 B.离子键 C.氢键 D.配位键
(4)
 是一种重要的半导体材料,晶胞结构如图1;将
是一种重要的半导体材料,晶胞结构如图1;将 掺杂到
掺杂到 的晶体中得到稀磁性半导体材料,如图2。
的晶体中得到稀磁性半导体材料,如图2。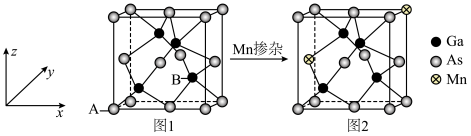
 ,则B原子的分数坐标为
,则B原子的分数坐标为 晶体密度为
晶体密度为 ,设
,设 为阿伏加德罗常数的值,则晶胞中两个
为阿伏加德罗常数的值,则晶胞中两个 原子间的最小距离为
原子间的最小距离为 (列出计算式即可);稀磁性半导体材料中
(列出计算式即可);稀磁性半导体材料中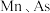 的原子个数比为
的原子个数比为
您最近一年使用:0次
名校
9 . 柠檬烯的结构式如图所示,下列说法正确的是
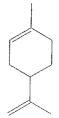
A.柠檬烯的分子式为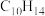 |
B. 柠檬烯最多能与 柠檬烯最多能与 发生加成反应 发生加成反应 |
C.柠檬烯分子中碳原子的杂化方式有 、 、 、 、 |
| D.柠檬烯分子的所有碳原子都可以位于同一平面内 |
您最近一年使用:0次
名校
解题方法
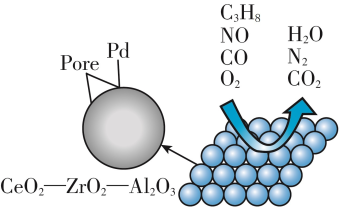
10 . 为解决汽车尾气达标排放,催化剂及其载体的选择和改良是关键。目前我国研制的稀土催化剂具有很好的催化转化效果,催化过程图如下。__________ 。
(2)CO、NO均能够与血红蛋白(Hb)中Fe2+形成稳定的配合物使血红蛋白失去携氧能力,因而具有毒性。
已知:CO进入血液后有如下平衡:CO+Hb·O2 O2+Hb·CO
O2+Hb·CO
①C、N、O三种元素,第一电离能由大到小的顺序为________ ,简单氢化物的沸点由大到小的顺序为_____ (用氢化物化学式表示)。
②在CO、NO结构中,C、N、O原子均含有孤电子对,与Fe2+配位时,配位原子均不是O原子,理由是:_______________ 。
③高压氧舱可用于治疗CO中毒,结合平衡移动原理解释其原因:____________ 。
(3)为节省贵金属并降低成本,常用某些复合型物质作催化剂。一种复合型物质的晶胞结构如图所示。________ 。
②已知阿伏加德罗常数的值为NA,该晶体的密度为ρg/cm3。其晶胞为立方体结构,则晶胞的边长为________ cm。
(2)CO、NO均能够与血红蛋白(Hb)中Fe2+形成稳定的配合物使血红蛋白失去携氧能力,因而具有毒性。
已知:CO进入血液后有如下平衡:CO+Hb·O2
 O2+Hb·CO
O2+Hb·CO①C、N、O三种元素,第一电离能由大到小的顺序为
②在CO、NO结构中,C、N、O原子均含有孤电子对,与Fe2+配位时,配位原子均不是O原子,理由是:
③高压氧舱可用于治疗CO中毒,结合平衡移动原理解释其原因:
(3)为节省贵金属并降低成本,常用某些复合型物质作催化剂。一种复合型物质的晶胞结构如图所示。

②已知阿伏加德罗常数的值为NA,该晶体的密度为ρg/cm3。其晶胞为立方体结构,则晶胞的边长为
您最近一年使用:0次