名校
解题方法
1 . 下列关于化学用语的说法错误的是
A.在 中只有 中只有 键无 键无 键 键 |
B. 电子云轮廓图为 电子云轮廓图为 |
C.若基态Cr原子的价层电子轨道表示式为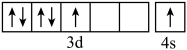 ,则其不满足洪特规则 ,则其不满足洪特规则 |
D. 的VSEPR构型为 的VSEPR构型为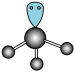 |
您最近一年使用:0次
名校
2 . 下列说法不正确的是
A.分子的极性: |
B. 与 与 中心原子的杂化方式相同 中心原子的杂化方式相同 |
C.酸性: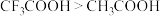 |
D. 中含配位键 中含配位键 |
您最近一年使用:0次
3 . 下列实验操作、现象和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 加热 固体,并将产生的气体通入 固体,并将产生的气体通入 溶液 溶液 | 溶液产生白色沉淀 |  固体受热分解生成了 固体受热分解生成了 和 和 |
| B | 向5mL 溶液中滴加氨水至沉淀溶解,再加入10mL 溶液中滴加氨水至沉淀溶解,再加入10mL ,过滤 ,过滤 | 析出深蓝色固体 | 氨水与 反应生成了 反应生成了 |
| C | 向盛有1mL乙酸乙酯的试管中加入3mL稀 溶液 溶液 | 试管中液体先分层,振荡后酯层消失 | 乙酸乙酯在酸性条件下可以彻底水解 |
| D | 将少量卤代乙烷加入NaOH的乙醇溶液中并水浴加热,反应后加入 酸化,滴入 酸化,滴入 溶液 溶液 | 溶液中出现淡黄色沉淀 | 卤代乙烷中含有溴原子 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 .  在水溶液中可与
在水溶液中可与  反应生成
反应生成 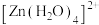 和
和 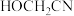 下列说法错误的
下列说法错误的
 在水溶液中可与
在水溶液中可与  反应生成
反应生成 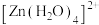 和
和 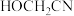 下列说法错误的
下列说法错误的A. 中键角 中键角 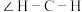 小于 小于 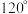 |
B.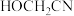 的沸点低于 的沸点低于  |
C. 与 与 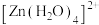 的中心离子的配位数均为4 的中心离子的配位数均为4 |
D.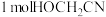 分子中含有的σ键与π键的物质的量之比为 分子中含有的σ键与π键的物质的量之比为  |
您最近一年使用:0次
名校
解题方法
5 . 已知反应 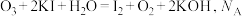 为阿伏加德罗常数的值,若生成
为阿伏加德罗常数的值,若生成  (标况),下列说法错误的是
(标况),下列说法错误的是
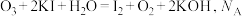 为阿伏加德罗常数的值,若生成
为阿伏加德罗常数的值,若生成  (标况),下列说法错误的是
(标况),下列说法错误的是A.转移的电子数目为  | B. 的 的 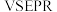 模型为 模型为 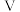 形 形 |
C.参与反应的  含有孤电子对数为 含有孤电子对数为 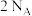 | D.生成的还原产物质量为  |
您最近一年使用:0次
名校
6 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.配合物 的熔点为 的熔点为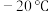 ,沸点为103℃, ,沸点为103℃,   键的数目为 键的数目为 |
B.醋酸溶液中溶解 醋酸钠固体后,醋酸根离子数目不可能为 醋酸钠固体后,醋酸根离子数目不可能为 |
C.铅蓄电池充电时,当正极增加9.6g时,转移的电子数 |
D.标准状况下,  和 和  在光照下充分反应后分子数为 在光照下充分反应后分子数为 |
您最近一年使用:0次
7 . 某多孔储氢材料前驱体结构如图,M、W、X、Y、Z为原子序数依次增大的五种短周期主族非金属元素,Z是地壳中含量最多的元素。下列说法正确的是
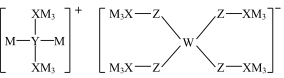
| A.基态原子的第一电离能:W<X<Y<Z |
| B.基态原子未成对电子数:W<X<Z<Y |
C.1 mol该化合物中含有配位键的数目为 |
| D.W基态原子的电子的空间运动状态有5种 |
您最近一年使用:0次
2023-11-01更新
|
546次组卷
|
5卷引用:重庆市荣昌中学校2023-2024学年高三下学期开学考试化学试题
解题方法
8 . 钛、铬、铁、镍、铜、硼等元素及其化合物在工业上有重要用途。
(1)钛铁合金是铁系储氢合金的代表,该合金具有放氢温度低、价格适中等优点。
①Ti的基态原子价电子排布式为___________ 。
②Fe的基态原子共有___________ 种不同能级的电子。
③ 也是一种储氢材料,可由
也是一种储氢材料,可由 和
和 反应制得。
反应制得。 由
由 和
和 构成,
构成, 的立体结构是
的立体结构是___________ 。
(2)制备 的反应为
的反应为 。
。
①上述化学方程式中非金属元素电负性由大到小的顺序是___________ (用元素符号表示)。
②分子中所有原子均满足8电子构型, 的电子式为
的电子式为___________ ,分子中 键和
键和 键的个数比为
键的个数比为___________ ,中心原子的杂化方式为___________ 。
(3)NiO、FeO的晶体结构均与氯化钠的晶体结构相同,其中 和
和 的离子半径分别为
的离子半径分别为 和
和 。则熔点:NiO
。则熔点:NiO___________ FeO(填“>”、“<”或“=”)。
(4)某铜镍合金的立方晶胞结构如图所示。
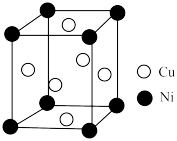
①该晶体的化学式为___________ 。
②已知该晶胞的摩尔质量为 ,密度为
,密度为 。设
。设 为阿伏加德罗常数的值,则该晶胞的棱长是
为阿伏加德罗常数的值,则该晶胞的棱长是___________ cm。(用含M、d、 的代数式表示)
的代数式表示)
(1)钛铁合金是铁系储氢合金的代表,该合金具有放氢温度低、价格适中等优点。
①Ti的基态原子价电子排布式为
②Fe的基态原子共有
③
 也是一种储氢材料,可由
也是一种储氢材料,可由 和
和 反应制得。
反应制得。 由
由 和
和 构成,
构成, 的立体结构是
的立体结构是(2)制备
 的反应为
的反应为 。
。①上述化学方程式中非金属元素电负性由大到小的顺序是
②分子中所有原子均满足8电子构型,
 的电子式为
的电子式为 键和
键和 键的个数比为
键的个数比为(3)NiO、FeO的晶体结构均与氯化钠的晶体结构相同,其中
 和
和 的离子半径分别为
的离子半径分别为 和
和 。则熔点:NiO
。则熔点:NiO(4)某铜镍合金的立方晶胞结构如图所示。

①该晶体的化学式为
②已知该晶胞的摩尔质量为
 ,密度为
,密度为 。设
。设 为阿伏加德罗常数的值,则该晶胞的棱长是
为阿伏加德罗常数的值,则该晶胞的棱长是 的代数式表示)
的代数式表示)
您最近一年使用:0次
9 . 某有机化合物的结构式如图所示,其组成元素Z、X、Y、Q、M、W为原子序数依次增大的短周期主族元素,Y原子核外有3个未成对电子,Q的最外层电子数是内层电子数的3倍,M的最高化合价为最低化合价绝对值的3倍。下列说法正确的是
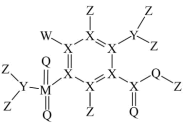

| A.最简单氢化物的沸点高低顺序为Y>X>Q |
| B.MQW2和XQW2空间构型为三角锥形 |
| C.第一电离能由小到大的顺序为X<Q<Y |
| D.Y、Q、M的简单离子半径的大小关系为Y<Q<M |
您最近一年使用:0次
名校
10 . NA为阿伏加德罗常数的值,下列说法正确的是
| A.0.1mol羟基所含的电子的数目为0.7NA |
B.1mol环戊二烯(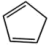 )中含有键的数目是11NA,键的数目为2NA )中含有键的数目是11NA,键的数目为2NA |
| C.1molK3[Fe(CN)6]中配位键的数目为9NA |
D.0.1mol·L−1CH3COOH溶液中CH3COOH和 数目之和为0.1NA 数目之和为0.1NA |
您最近一年使用:0次



