名校
解题方法
1 . 铋的化合物在电催化和光催化领域都有广泛应用。一种以氧化铋渣(主要成分是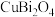 、
、 、
、 和
和 等)为原料,制取高纯
等)为原料,制取高纯 的工业流程如图所示:
的工业流程如图所示:
回答下列问题:
(1)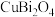 中的Cu的化合价为+2,则Bi的化合价是
中的Cu的化合价为+2,则Bi的化合价是_______ ,Bi与N同族,Bi原子处于基态时电子占据最高能级的电子云轮廓图为_______ 形。
(2)“沉铋”时加入NaOH溶液, 转化为BiOCl沉淀的离子方程式是
转化为BiOCl沉淀的离子方程式是_______ 。
(3)“洗涤”滤饼时先用水洗,再用稀硫酸洗涤(已知:BiOCl不溶于稀硫酸),用稀硫酸洗涤的目的是为了除去滤饼中的_______ (填化学式)杂质。
(4)“转化”过程中BiOCl转化为 沉淀,当溶液中
沉淀,当溶液中 浓度为
浓度为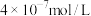 时溶液的pH为
时溶液的pH为_______ 。(该温度下,已知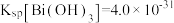 )
)
(5)硫代乙酰胺(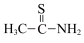 )中碳原子的杂化方式分别为
)中碳原子的杂化方式分别为_______ 。
(6)钼酸铋( )可用于光催化水的分解,其晶胞结构(不含氧原子)如图所示,晶胞参数为
)可用于光催化水的分解,其晶胞结构(不含氧原子)如图所示,晶胞参数为 ,晶胞棱边夹角均为90°。
,晶胞棱边夹角均为90°。 ,则原子2的分数坐标为
,则原子2的分数坐标为_______ 。
②设阿伏加德罗常数的值为 ,
, 的相对分子质量为
的相对分子质量为 ,则
,则 晶体的密度为
晶体的密度为_______  。
。
 、
、 、
、 和
和 等)为原料,制取高纯
等)为原料,制取高纯 的工业流程如图所示:
的工业流程如图所示: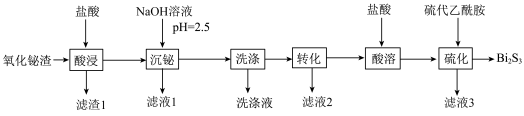
| 离子 |  |  |  |
| 开始沉淀的pH | 1.5 | 3.6 | 4.5 |
| 沉淀完全的pH | 3.2 | 4.7 | 6.7 |
(1)
 中的Cu的化合价为+2,则Bi的化合价是
中的Cu的化合价为+2,则Bi的化合价是(2)“沉铋”时加入NaOH溶液,
 转化为BiOCl沉淀的离子方程式是
转化为BiOCl沉淀的离子方程式是(3)“洗涤”滤饼时先用水洗,再用稀硫酸洗涤(已知:BiOCl不溶于稀硫酸),用稀硫酸洗涤的目的是为了除去滤饼中的
(4)“转化”过程中BiOCl转化为
 沉淀,当溶液中
沉淀,当溶液中 浓度为
浓度为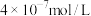 时溶液的pH为
时溶液的pH为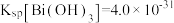 )
)(5)硫代乙酰胺(
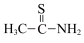 )中碳原子的杂化方式分别为
)中碳原子的杂化方式分别为(6)钼酸铋(
 )可用于光催化水的分解,其晶胞结构(不含氧原子)如图所示,晶胞参数为
)可用于光催化水的分解,其晶胞结构(不含氧原子)如图所示,晶胞参数为 ,晶胞棱边夹角均为90°。
,晶胞棱边夹角均为90°。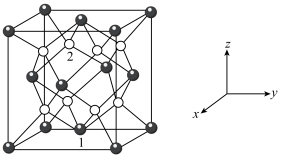
 ,则原子2的分数坐标为
,则原子2的分数坐标为②设阿伏加德罗常数的值为
 ,
, 的相对分子质量为
的相对分子质量为 ,则
,则 晶体的密度为
晶体的密度为 。
。
您最近一年使用:0次
名校
2 . 微观的世界多姿多彩,下列说法正确的是
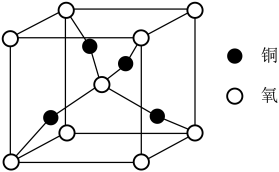
| A.上图为铜和氧形成的一种晶体,该氧化物为CuO |
| B.氧元素位于周期表的s区 |
C. 分子中,氮原子存在孤电子对 分子中,氮原子存在孤电子对 |
| D.四氨合铜离子中存在离子键 |
您最近一年使用:0次
名校
解题方法
3 . 下列有关说法表达正确的是
A.基态Cu原子的价层电子排布式: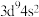 |
| B.基态Si原子中,有两个未成对电子 |
C.第二周期元素中,电负性: |
D. 与 与 均为直线型分子 均为直线型分子 |
您最近一年使用:0次
名校
解题方法
4 . 按要求回答下列问题:
(1)A.乙烷 B.乙烯 C.乙炔 D.苯是有机化学中的代表物质,其中:
①既有 键又有
键又有 键的是
键的是_______ (填序号,下同)。
②碳碳键的键长由大到小排序是:_______ 。
③上述分子中所有原子均在同一平面是:_______ 。
(2)含硫元素的微粒有很多,例如 、
、 、
、 、
、 、
、 ,其中
,其中 的分子结构如下图所示,像一顶皇冠,请回答下列问题:
的分子结构如下图所示,像一顶皇冠,请回答下列问题: 中含有的
中含有的 键数目是
键数目是_______ 。
② 中S原子的杂化轨道类型是
中S原子的杂化轨道类型是_______ , 的空间结构是
的空间结构是_______ 。
③ 分子的VSEPR模型是
分子的VSEPR模型是_______ , 是
是_______ (填“极性”或“非极性”)分子。
④沸点:
_______  (填“
(填“ ”、“
”、“ ”或“
”或“ ”),原因是
”),原因是_______ 。
(1)A.乙烷 B.乙烯 C.乙炔 D.苯是有机化学中的代表物质,其中:
①既有
 键又有
键又有 键的是
键的是②碳碳键的键长由大到小排序是:
③上述分子中所有原子均在同一平面是:
(2)含硫元素的微粒有很多,例如
 、
、 、
、 、
、 、
、 ,其中
,其中 的分子结构如下图所示,像一顶皇冠,请回答下列问题:
的分子结构如下图所示,像一顶皇冠,请回答下列问题: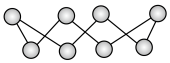
 中含有的
中含有的 键数目是
键数目是②
 中S原子的杂化轨道类型是
中S原子的杂化轨道类型是 的空间结构是
的空间结构是③
 分子的VSEPR模型是
分子的VSEPR模型是 是
是④沸点:

 (填“
(填“ ”、“
”、“ ”或“
”或“ ”),原因是
”),原因是
您最近一年使用:0次
名校
解题方法
5 . 下列粒子中,与 分子的空间构型相同的是
分子的空间构型相同的是
 分子的空间构型相同的是
分子的空间构型相同的是A. | B. | C. | D. |
您最近一年使用:0次
名校
6 . 硫代硫酸钠(Na2S2O3)是硫酸钠中一个氧原子被硫原子取代的产物。硫代硫酸钠晶体(Na2S2O3·5H2O,M=248g⋅mol−1)易溶于水,难溶于乙醇,在酸性环境中易分解。
Ⅰ.制备a2S2O3·5H2O
方法一:亚硫酸钠法。反应原理:S+Na2SO3=Na2S2O3
实验步骤:称取一定量的Na2SO3固体于烧杯中,溶于煮沸过的蒸馏水。另取过量的硫粉,加入少量乙醇充分搅拌后,加到上述Na2SO3溶液中。水浴加热,微沸,反应后趁热过滤。滤液蒸发浓缩、冷却结晶析出Na2S2O3·5H2O晶体。
(1) 中心硫原子的杂化方式为
中心硫原子的杂化方式为___________ 。
(2)使用煮沸过的蒸馏水配制Na2SO3溶液的目的是___________ 。
方法二:硫化碱法。装置如图所示。
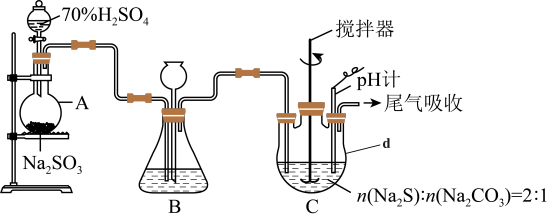
(3)①仪器d的名称为___________ 。
②装置A中发生反应的化学方程式为___________ 。
③装置C中,将Na2S和Na2CO3以2:1的物质的量之比配成溶液再通入SO2,便可制得Na2S2O3和CO2.该反应的化学方程式为___________ 。
④实验过程中,为了保证Na2S2O3·5H2O的产量,实验中通入的SO2不能过量,原因是_________ 。
Ⅱ.Na2S2O3的应用
(4)设计以下实验测定粗产品中Na2S2O3·5H2O的含量:
步骤1:准确称取8.0000g样品溶于水,配成100mL溶液。
步骤2:准确称取0.294gK2Cr2O7固体于碘量瓶中,加入20mL蒸馏水溶解,再加入10mL2mol⋅L−1H2SO4和20mL10%KI溶液使铬元素完全转化为Cr3+,加水稀释至100mL。
步骤3:向碘量瓶中加入1mL某溶液作指示剂,用待测Na2S2O3溶液滴定碘量瓶中溶液至滴定终点,消耗Na2S2O3溶液20.00mL。(已知:I2+2 =2I−+
=2I−+ )
)
①步骤3中向碘量瓶中加入的指示剂是___________ 。
②由计算可得Na2S2O3·5H2O的纯度为___________ 。
Ⅰ.制备a2S2O3·5H2O
方法一:亚硫酸钠法。反应原理:S+Na2SO3=Na2S2O3
实验步骤:称取一定量的Na2SO3固体于烧杯中,溶于煮沸过的蒸馏水。另取过量的硫粉,加入少量乙醇充分搅拌后,加到上述Na2SO3溶液中。水浴加热,微沸,反应后趁热过滤。滤液蒸发浓缩、冷却结晶析出Na2S2O3·5H2O晶体。
(1)
 中心硫原子的杂化方式为
中心硫原子的杂化方式为(2)使用煮沸过的蒸馏水配制Na2SO3溶液的目的是
方法二:硫化碱法。装置如图所示。

(3)①仪器d的名称为
②装置A中发生反应的化学方程式为
③装置C中,将Na2S和Na2CO3以2:1的物质的量之比配成溶液再通入SO2,便可制得Na2S2O3和CO2.该反应的化学方程式为
④实验过程中,为了保证Na2S2O3·5H2O的产量,实验中通入的SO2不能过量,原因是
Ⅱ.Na2S2O3的应用
(4)设计以下实验测定粗产品中Na2S2O3·5H2O的含量:
步骤1:准确称取8.0000g样品溶于水,配成100mL溶液。
步骤2:准确称取0.294gK2Cr2O7固体于碘量瓶中,加入20mL蒸馏水溶解,再加入10mL2mol⋅L−1H2SO4和20mL10%KI溶液使铬元素完全转化为Cr3+,加水稀释至100mL。
步骤3:向碘量瓶中加入1mL某溶液作指示剂,用待测Na2S2O3溶液滴定碘量瓶中溶液至滴定终点,消耗Na2S2O3溶液20.00mL。(已知:I2+2
 =2I−+
=2I−+ )
)①步骤3中向碘量瓶中加入的指示剂是
②由计算可得Na2S2O3·5H2O的纯度为
您最近一年使用:0次
名校
解题方法
7 . 下列方程式与所给事实不相符的是
A.硫酸铜溶液中加少量氨水:Cu2++2NH3·H2O=Cu(OH)2↓+2 |
B.氢气燃烧热为285.8kJ/mol:H2(g)+ O2(g)=H2O(l) ΔH=−285.8kJ/mol O2(g)=H2O(l) ΔH=−285.8kJ/mol |
| C.用KSCN溶液检验Fe3+:Fe3++3SCN−=Fe(SCN)3↓ |
| D.加热CuCl2溶液,溶液变成黄绿色:[Cu(H2O)4]2++4Cl−⇌[CuCl4]2−+4H2O ΔH>0 |
您最近一年使用:0次
单选题
|
适中(0.65)
|
名校
解题方法
8 . BODIPY类荧光染料母体结构(如图所示)由X、Y、Z、M、N五种原子序数依次增大的第一和第二周期主族元素组成。其中,X是宇宙中含量最多的元素,Y、N可形成平面三角形分子YN3,N元素只有两种化合价。下列说法错误的是
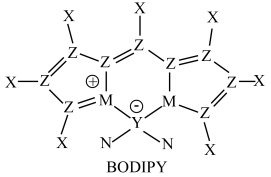

| A.基态原子未成对电子数:Y<Z<M |
| B.该母体结构中含sp2杂化和sp3杂化的原子 |
| C.Y和M组成的化合物是一种新型陶瓷 |
| D.X与M形成的简单化合物的水溶液呈酸性 |
您最近一年使用:0次
2023-12-28更新
|
259次组卷
|
3卷引用:重庆市巴蜀中学校2023-2024学年高三上学期11月期中化学试题
单选题
|
适中(0.65)
|
9 . 下列实验操作及现象与对应结论匹配的是
| 选项 | 实验操作及现象 | 结论 |
| A | 取一定量Na2SO3样品,溶解后加入BaCl2溶液,产生白色沉淀。加入浓HNO3,仍有沉淀。 | 此样品中含有SO |
| B | 相同温度下,分别测定相同浓度的NaNO2和CH3COONa溶液pH,NaNO2溶液的pH约为8,CH3COONa溶液的pH约为9 | 相同温度下,Ka(HNO2)<Ka(CH3COOH) |
| C | 向硫酸铜溶液中滴加浓盐酸至过量,溶液由蓝色变为绿色。 | [Cu(H2O)4]2+转化为[CuCl4]2- |
| D | 将Zn(OH)2固体粉末加入过量NaOH溶液中,充分搅拌,溶解得到无色溶液。 | Zn(OH)2既体现碱性又体现酸性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-28更新
|
195次组卷
|
3卷引用:重庆市巴蜀中学校2023-2024学年高三上学期11月期中化学试题
10 . Beckmann重排被广泛应用于有机合成中,下列反应就是Beckmann重排的实例之一、下列说法错误的是


| A.X 中碳原子采用 sp2、sp3杂化 |
| B.X 和 Y 互为同分异构体 |
| C.若硝基中原子均共平面,则Y中最多17个原子共平面 |
| D.Y 中的官能团有酰胺基、硝基、碳溴键 |
您最近一年使用:0次



