名校
解题方法
1 . 法匹拉韦是治疗新冠肺炎的一种药物,其结构简式如图所示。下列说法正确的是
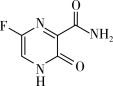

| A.该分子中C原子均为sp2杂化 |
| B.该分子中C—N键的键能大于C—F键的键能 |
| C.该分子中σ键与π键数目之比为7:2 |
| D.该分子中存在手性碳原子 |
您最近一年使用:0次
14-15高三上·上海嘉定·期末
名校
解题方法
2 . 有关化学键和晶体的说法中正确的是
| A.离子键的本质是静电作用,阴阳离子电荷越大、离子半径越小,静电作用越强 |
| B.共价键的本质是共用电子对,因此必须由成键的两原子各提供一个电子形成 |
| C.分子晶体的基本微粒是分子,分子晶体熔沸点由分子内部共价键强弱决定 |
| D.原子晶体由于是空间网状结构,因此只能由碳、硅两元素构成 |
您最近一年使用:0次
解题方法
3 . 下列说法正确的是( )
| A.键角越大,该分子越稳定 |
| B.共价键的键能越大,共价键越牢固,含有该键的分子越稳定 |
| C.CH4、CCl4中键长相等,键角不同 |
| D.C===C键的键能是C—C键的2倍 |
您最近一年使用:0次
2018-04-23更新
|
236次组卷
|
3卷引用:山东省单县五中2017-2018学年高二下学期第一次月考化学试题
4 . 探究共价晶体熔点高低的比较判断。
(1)晶体的熔点的高低取决于共价键的_______ 和_______ 。键长越_______ ,键能越_______ ,共价键越_______ ,物质的熔点越_______ 。
(2)若没有告知键长或键能数据时,可比较_______ 的大小。一般原子半径越_______ ,键长越短,键能越大,晶体的熔点就越_______ 。如比较金刚石、碳化硅、晶体硅的熔点高低。原子半径:C<Si,则键长:C-C<C-Si<Si-Si,故键能:C-C>C-Si>Si-Si,熔点:金刚石>碳化硅>晶体硅。
(1)晶体的熔点的高低取决于共价键的
(2)若没有告知键长或键能数据时,可比较
您最近一年使用:0次
5 . 氰气化学式为(CN)2,结构式为 N≡C—C≡N,性质与卤素相似,叙述正确的是( )
A.在一定条件下可发生加成反应  |
| B.分子中N≡C键的键长大于C—C键的键长 |
| C.分子中含有2个σ键和4个π键 |
| D.不能与氢氧化钠溶液发生反应 |
您最近一年使用:0次
2016-04-12更新
|
362次组卷
|
13卷引用:2015-2016学年四川成都七中高二上12月月考化学试卷
2015-2016学年四川成都七中高二上12月月考化学试卷2015-2016学年湖北省宜昌金东方高级中学高二上学期期末化学试卷2015-2016学年陕西西藏民族学院附中高二4月月考化学卷2015-2016学年河北省定州中学高二下期中化学试卷安徽省安庆市五校联盟2017-2018学年高二上学期期中联考化学试题【全国市级联考】四川省乐山市2017-2018学年高二上学期期末化学试题福建省莆田第一中学2019-2020学年高二下学期期中考试化学试题安徽省六安中学2019-2020学年高二下学期期末考试化学试题(已下线)山西省原平市范亭中学2018-2019学年高二4月月考化学试题山西省晋中市新一双语学校2020-2021学年高二下学期3月月考化学试题福建省福清西山学校高中部2020-2021学年高二下学期期中考试化学试题内蒙古赤峰市2020-2021学年高二下学期期末考试化学(A)试题新疆阿克苏市实验中学2022-2023学年高二下学期第三次月考化学试题
名校
6 . 如图为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是
| X | |||
| W | Y | R | |
| Z |
| A.W、R元素单质分子内的化学键都是非极性键 |
| B.X、Z元素都能够形成双原子分子 |
| C.键能:W-H>Y-H,键的极性:Y-H>W-H |
| D.键长:X-H<W-H,键能:X-H>W-H |
您最近一年使用:0次
名校
解题方法
7 . 下列各选项中的两个量,前者一定大于后者的是
| A.基态Al原子和基态N原子的未成对电子数 |
| B.BF3的键角和NF3的键角 |
| C.C=C键的键长和C-C键的键长 |
| D.H-I的键能和H-F的键能 |
您最近一年使用:0次
名校
8 . 下列说法中正确的是

 杂化轨道是由同一个原子中能量最近的s轨道和p轨道混合起来形成的一组能量相同的新轨道
杂化轨道是由同一个原子中能量最近的s轨道和p轨道混合起来形成的一组能量相同的新轨道
 同一周期从左到右,元素的第一电离能、电负性都是越来越大
同一周期从左到右,元素的第一电离能、电负性都是越来越大
 分子中键能越大,表示分子拥有的能量越高
分子中键能越大,表示分子拥有的能量越高
 所有的配合物都存在配位键
所有的配合物都存在配位键
 所有含极性键的分子都是极性分子
所有含极性键的分子都是极性分子
 熔融状态下能导电的化合物一定是离子化合物
熔融状态下能导电的化合物一定是离子化合物
 所有的原子晶体都不导电
所有的原子晶体都不导电


 杂化轨道是由同一个原子中能量最近的s轨道和p轨道混合起来形成的一组能量相同的新轨道
杂化轨道是由同一个原子中能量最近的s轨道和p轨道混合起来形成的一组能量相同的新轨道 同一周期从左到右,元素的第一电离能、电负性都是越来越大
同一周期从左到右,元素的第一电离能、电负性都是越来越大 分子中键能越大,表示分子拥有的能量越高
分子中键能越大,表示分子拥有的能量越高 所有的配合物都存在配位键
所有的配合物都存在配位键 所有含极性键的分子都是极性分子
所有含极性键的分子都是极性分子 熔融状态下能导电的化合物一定是离子化合物
熔融状态下能导电的化合物一定是离子化合物 所有的原子晶体都不导电
所有的原子晶体都不导电A.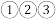 | B. | C.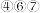 | D.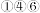 |
您最近一年使用:0次
2018-07-20更新
|
207次组卷
|
3卷引用:2015-2016学年四川省新津中学高二上学期12月月考化学试卷
名校
解题方法
9 . [化学-选修3:物质结构与性质]
(1)丙酮(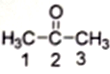 )分子中2号碳原子的杂化方式为
)分子中2号碳原子的杂化方式为__________ ;
(2)写出镍原子的电子排布式_____________ ;
(3)H2O分子的键角比NH3分子的键角小,原因是_____________________________________ ;
(4)N、P、As属于同族元素,它们的简单氢化物沸点由大到小的顺序为_________________ (用化学式表示),其原因是 ____________________________________ ;
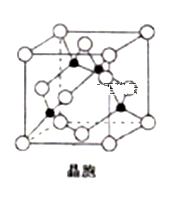
(5)由铜与氯形成的一种化合物的晶胞结构如图所示(黑点代表铜原子)。
①将晶胞内的4个黑点相互连接所形成的立体构型是______________ ;
②晶体中与一个氯原子距离最近的氯原子有___________ 个;
③已知该晶体的密度为ρg.cm-3,阿伏伽德罗常数的值为NA,则该晶体中铜原子和氯原子之间的最短距离为____________ pm(列出计算式即可);
(1)丙酮(
 )分子中2号碳原子的杂化方式为
)分子中2号碳原子的杂化方式为(2)写出镍原子的电子排布式
(3)H2O分子的键角比NH3分子的键角小,原因是
(4)N、P、As属于同族元素,它们的简单氢化物沸点由大到小的顺序为

(5)由铜与氯形成的一种化合物的晶胞结构如图所示(黑点代表铜原子)。
①将晶胞内的4个黑点相互连接所形成的立体构型是
②晶体中与一个氯原子距离最近的氯原子有
③已知该晶体的密度为ρg.cm-3,阿伏伽德罗常数的值为NA,则该晶体中铜原子和氯原子之间的最短距离为
您最近一年使用:0次
2018-12-17更新
|
193次组卷
|
2卷引用:宁夏回族自治区银川市长庆高级中学2019届高三上学期第四次月考理科综合化学试题
13-14高二下·宁夏银川·期末
名校
10 . 下列判断正确的是
| A.根据同周期元素的第一电离能变化趋势,推出Al的第一电离能比Mg大 |
| B.根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正价都是+7 |
| C.晶体中一定存在化学键 |
| D.正四面体分子中键角可能是109°28′或60° |
您最近一年使用:0次
2016-12-09更新
|
285次组卷
|
9卷引用:2013-2014宁夏银川一中高二下学期期末考试化学试卷
(已下线)2013-2014宁夏银川一中高二下学期期末考试化学试卷2014-2015吉林省吉林市第五十五中学高二下学期期中考试化学试卷2015-2016学年贵州省思南中学高二下期中化学试卷苏教版高二化学选修三单元测试题:2.2 元素性质的递变规律2020届高三化学二轮物质结构题型专攻——元素性质的递变规律【选择基础专练】(已下线)模块同步卷12 综合检测卷(提升卷)-《灯塔金卷系列》2020-2021学年高二化学模块同步卷(人教版选修3)宁夏青铜峡市高级中学2020-2021学年高二下学期第一次月考化学试题宁夏中卫市中宁县第一中学2021-2022学年高三上学期第一次月考化学试题四川省内江市威远中学校2022-2023学年高二上学期第一次月考化学试题



