解题方法
1 . 请按要求完成填空:
(1)完成下表中的空白:
(2)配合物[Cu(NH3)4]SO4的中心离子是___________ 、配体是___________ 、配位原子是___________ 、配位数是___________ 。
(1)完成下表中的空白:
| 粒子 | 中心原子孤电子对数 | 中心原子的杂化轨道类型 | VSEPR模型 | 空间结构 |
| CO2 | ① | ② | ③ | ④ |
SO | ⑤ | ⑥ | ⑦ | ⑧ |
您最近一年使用:0次
解题方法
2 . 下列关于物质的结构或性质以及解释均正确的是
| 选项 | 物质的结构或性质 | 解释 |
| A | 键角:NH3>BF3 | NH3中N的孤电子对数比BF3中B的孤电子对数多 |
| B | 酸性:CF3COOH>CCl3COOH | F的电负性大于Cl的电负性,使CF3COOH中羧基上的氢更易电离 |
| C | 熔点:碳化硅>金刚石 | C﹣Si键能大于C﹣C键能 |
| D | 稳定性:H2O>CH4 | H2O分子之间除了范德华力以外还存在氢键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
3 . 硅烷广泛应用在现代高科技领域。
制备硅烷的反应为 。
。
(1)①基态硅原子的价层电子轨道表示式为___________ 。
② 中,硅的化合价为+4价。硅显正化合价的原因是
中,硅的化合价为+4价。硅显正化合价的原因是___________ 。
③下列说法正确的是___________ (填字母)。
a. 的稳定性比
的稳定性比 的差
的差
b. 中4个
中4个 的键长相同,
的键长相同, 的键角为
的键角为
c. 中硅原子以4个
中硅原子以4个 杂化轨道分别与4个氢原子的
杂化轨道分别与4个氢原子的 轨道重叠,形成4个
轨道重叠,形成4个 键
键
④ 的沸点(-86℃)高于
的沸点(-86℃)高于 的沸点(-112℃),原因是
的沸点(-112℃),原因是___________ 。
(2) 的晶胞结构如图所示,晶胞的体积为
的晶胞结构如图所示,晶胞的体积为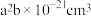 。
。 的
的 模型名称为
模型名称为___________ 。
②用 表示阿伏伽德罗常数的值。
表示阿伏伽德罗常数的值。 晶体密度为
晶体密度为___________  (用含
(用含 、
、 、
、 的代数式表示)。
的代数式表示)。
制备硅烷的反应为
 。
。(1)①基态硅原子的价层电子轨道表示式为
②
 中,硅的化合价为+4价。硅显正化合价的原因是
中,硅的化合价为+4价。硅显正化合价的原因是③下列说法正确的是
a.
 的稳定性比
的稳定性比 的差
的差b.
 中4个
中4个 的键长相同,
的键长相同, 的键角为
的键角为
c.
 中硅原子以4个
中硅原子以4个 杂化轨道分别与4个氢原子的
杂化轨道分别与4个氢原子的 轨道重叠,形成4个
轨道重叠,形成4个 键
键④
 的沸点(-86℃)高于
的沸点(-86℃)高于 的沸点(-112℃),原因是
的沸点(-112℃),原因是(2)
 的晶胞结构如图所示,晶胞的体积为
的晶胞结构如图所示,晶胞的体积为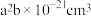 。
。
 的
的 模型名称为
模型名称为②用
 表示阿伏伽德罗常数的值。
表示阿伏伽德罗常数的值。 晶体密度为
晶体密度为 (用含
(用含 、
、 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
名校
4 . NH3具有易液化、含氢密度高、应用广泛等优点,NH3的合成及应用一直是科学研究的重要课题。
(1)以H2、N2合成NH3,Fe是常用的催化剂。
①基态Fe原子的电子排布式为_____ 。
②我国科学家开发出Fe-LiH等双中心催化剂,在合成NH3中显示出高催化活性。第一电离能(I1):I1(H)>I1(Li)>I1(Na),原因是_____ 。
(2)化学工业科学家侯德榜利用下列反应最终制得了高质量的纯碱。
NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
①1体积水可溶解1体积CO2,1体积水可溶解约700体积NH3,NH3极易溶于水的原因是_____ 。
②NaHCO3分解得Na2CO3., 空间结构为
空间结构为_____ 。
(3)NH3、NH3BH3(氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
①NH3的中心原子的杂化轨道类型为_____ 。
②比较熔点:NH3BH3_____ CH3CH3(填“>”或“<”)。
(4)NF3的结构与NH3类似,但是性质差异较大。
①NF3的空间结构名称为_____ 。
②NH3BH3具有碱性(可与H+结合)而NF3没有碱性。原因是_____ 。
(1)以H2、N2合成NH3,Fe是常用的催化剂。
①基态Fe原子的电子排布式为
②我国科学家开发出Fe-LiH等双中心催化剂,在合成NH3中显示出高催化活性。第一电离能(I1):I1(H)>I1(Li)>I1(Na),原因是
(2)化学工业科学家侯德榜利用下列反应最终制得了高质量的纯碱。
NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
①1体积水可溶解1体积CO2,1体积水可溶解约700体积NH3,NH3极易溶于水的原因是
②NaHCO3分解得Na2CO3.,
 空间结构为
空间结构为(3)NH3、NH3BH3(氨硼烷)储氢量高,是具有广泛应用前景的储氢材料。
| 元素 | H | B | N | F |
| 电负性 | 2.1 | 2.0 | 3.0 | 4.0 |
②比较熔点:NH3BH3
(4)NF3的结构与NH3类似,但是性质差异较大。
①NF3的空间结构名称为
②NH3BH3具有碱性(可与H+结合)而NF3没有碱性。原因是
您最近一年使用:0次
2024-03-03更新
|
281次组卷
|
2卷引用:北京市第十九中学2021-2022学年高二下学期期中考试化学试题
名校
解题方法
5 . 下列化学用语或图示表达不正确 的是
A.氮分子的电子式: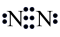 | B.Br的原子结构示意图: |
C.SO3的VSEPR模型: | D.基态24Cr的简化电子排布式:[Ar]3d54s1 |
您最近一年使用:0次
名校
解题方法
6 . 下列判断不正确的是
| A.电负性:P<S<Cl | B.沸点:Cl2<Br2<I2 |
| C.微粒半径:Li+<O2-<Na+ | D.键角:BF3>CH4>H2O |
您最近一年使用:0次
2023-12-25更新
|
180次组卷
|
2卷引用:北京市大兴区2022-2023学年大兴一中高二上学期期中考试(1+3学部)
名校
解题方法
7 . 下列各种物质中,都是由极性键构成的非极性分子的是
| A.NH3和CH4 | B.CO2和CCl4 | C.CH3Cl和BF3 | D.SO3和PCl3 |
您最近一年使用:0次
名校
解题方法
8 . 利用光催化技术可将太阳能转化为化学能。
(1)光催化可实现 的净化
的净化
①比较N、O元素第一电离能:N___________ O(填“>”或“小于”)。
②光催化还原 可得到
可得到 ,从结构角度分析
,从结构角度分析 性质稳定的原因
性质稳定的原因___________ 。
③光催化氧化 最终产物为硝酸盐,
最终产物为硝酸盐, 的空间结构是
的空间结构是___________ 形。
(2)光催化 和
和 合成甲醇是
合成甲醇是 转化利用最有前景的途径之一。比较甲醇分子中H-C-H与C-O-H的键角大小并解释原因
转化利用最有前景的途径之一。比较甲醇分子中H-C-H与C-O-H的键角大小并解释原因___________ 。
(3)光催化可降解苯酚( )。在紫外光的作用下催化剂表面有
)。在紫外光的作用下催化剂表面有 (羟基自由基)生成,
(羟基自由基)生成, 可将苯酚氧化为
可将苯酚氧化为 和
和 ,该反应的方程式为
,该反应的方程式为___________ 。
(4)某含钛的复合型物质可作光催化剂,晶胞结构如图所示,边长均为 。
。
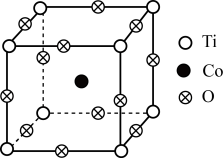
①基态钛原子的价层电子轨道表示式为___________ 。
②晶体中每个钛原子周围与其距离最近且相等的氧原子的个数是___________ 。
③ 表示阿伏加德罗常数的值,则该晶体的密度为
表示阿伏加德罗常数的值,则该晶体的密度为___________  。
。
(1)光催化可实现
 的净化
的净化①比较N、O元素第一电离能:N
②光催化还原
 可得到
可得到 ,从结构角度分析
,从结构角度分析 性质稳定的原因
性质稳定的原因③光催化氧化
 最终产物为硝酸盐,
最终产物为硝酸盐, 的空间结构是
的空间结构是(2)光催化
 和
和 合成甲醇是
合成甲醇是 转化利用最有前景的途径之一。比较甲醇分子中H-C-H与C-O-H的键角大小并解释原因
转化利用最有前景的途径之一。比较甲醇分子中H-C-H与C-O-H的键角大小并解释原因(3)光催化可降解苯酚(
 )。在紫外光的作用下催化剂表面有
)。在紫外光的作用下催化剂表面有 (羟基自由基)生成,
(羟基自由基)生成, 可将苯酚氧化为
可将苯酚氧化为 和
和 ,该反应的方程式为
,该反应的方程式为(4)某含钛的复合型物质可作光催化剂,晶胞结构如图所示,边长均为
 。
。
①基态钛原子的价层电子轨道表示式为
②晶体中每个钛原子周围与其距离最近且相等的氧原子的个数是
③
 表示阿伏加德罗常数的值,则该晶体的密度为
表示阿伏加德罗常数的值,则该晶体的密度为 。
。
您最近一年使用:0次
解题方法
9 . 黄铜矿(主要成分为CuFeS2)可用于冶炼Cu2O,主要物质转化过程如下:

(1)Cu2S与O2共热制备Cu2O的反应中,化合价升高的元素是___________ 。
(2)为减少SO2对环境的污染,在高温时可以用CaO将其转化为CaSO4,反应的化学方程式为___________ 。
(3) SO2中心原子的杂化方式是___________ ,用价层电子对互斥理论解释SO2的空间结构不同于CO2的原因:___________ 。
(4)下图中,表示Cu2O晶胞的是___________ (填“图1”或“图2”)。

(5)Cu2O与Cu2S都可视为离子晶体,且结构相似,但Cu2O的熔点比Cu2S的高约100℃,原因是___________ 。
(6) CuFeS2的晶胞如图3所示。
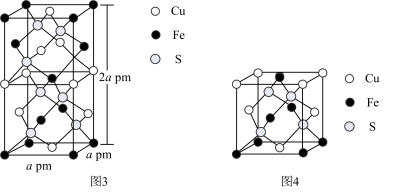
①图4所示结构单元不能 作为CuFeS2晶胞的原因是___________ 。
②从图3可以看出,每个CuFeS2晶胞中含有的Cu原子个数为___________ 。
③已知:CuFeS2晶体的密度是4.30g/cm3,阿伏伽德罗常数的值为NA。CuFeS2晶胞中底边边长a=___________ pm(用计算式表示;1cm=1010pm;CuFeS2的摩尔质量为184g/mol)。

(1)Cu2S与O2共热制备Cu2O的反应中,化合价升高的元素是
(2)为减少SO2对环境的污染,在高温时可以用CaO将其转化为CaSO4,反应的化学方程式为
(3) SO2中心原子的杂化方式是
(4)下图中,表示Cu2O晶胞的是

(5)Cu2O与Cu2S都可视为离子晶体,且结构相似,但Cu2O的熔点比Cu2S的高约100℃,原因是
(6) CuFeS2的晶胞如图3所示。

①图4所示结构单元
②从图3可以看出,每个CuFeS2晶胞中含有的Cu原子个数为
③已知:CuFeS2晶体的密度是4.30g/cm3,阿伏伽德罗常数的值为NA。CuFeS2晶胞中底边边长a=
您最近一年使用:0次
10 . 下列化学用语或图示表达正确的是
A. 的电子式为 的电子式为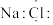 | B. 的VSEPR模型为 的VSEPR模型为 |
C.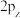 电子云图为 电子云图为 | D.基态 原子的价层电子轨道表示式为 原子的价层电子轨道表示式为 |
您最近一年使用:0次
2023-06-28更新
|
7451次组卷
|
16卷引用:北京师范大学第二附属中学2023-2024学年高三上学期期中考试化学试题
北京师范大学第二附属中学2023-2024学年高三上学期期中考试化学试题2023年高考北京卷化学真题(已下线)2023年北京卷高考真题变式题(选择题1-5)北京市第一七一中学2023-2024学年高三上学期10月考化学试题北京师范大学第二附属中学2023-2024学年高二上学期12月月考化学试题 北京师范大学附属中学2023-2024学年高二上学期期末考试化学试卷北京市第五十五中学2023-2024学年高二下学期(等级考)3月调研化学试卷(已下线)第21讲分子结构与性质江西省吉安市宁冈中学2023-2024学年高三上学期开学考试化学试题(已下线)专题02 化学用语及其应用-2023年高考化学真题题源解密(新高考专用)新疆疏附县第一中学2023-2024学年高三上学期开学摸底测试化学试题(已下线)题型01 物质的组成与分类 传统文化 化学用语-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)广东省珠海市第三中学2023-2024学年高二下学期3月月考化学试卷海南省文昌中学2023-2024学年高二下学期第一次月考化学试题上海市华东师范大学第二附属中学(紫竹校区)2023-2024学年高三下学期三模考试 化学试题福建省福建师范大学附属中学2023-2024学年高三上学期开学考化学试题



