名校
解题方法
1 . 铁、铜及其化合物在生产生活中有着广泛应用。回答下列问题:
(1)基态 原子核外电子的运动状态有
原子核外电子的运动状态有___________ 种;
 易被氧化为
易被氧化为 ,画出
,画出 的结构示意图
的结构示意图___________ 。
(2) 是检验
是检验 的特征试剂,
的特征试剂, 中心离子配位数是
中心离子配位数是___________ ;1mol 中含有
中含有___________ mol 键,能够证明
键,能够证明 不能电离的试剂是
不能电离的试剂是___________ (填化学式)。
(3) 可形成配合物
可形成配合物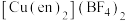 ,其中
,其中 代表
代表 分子。该配合物
分子。该配合物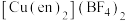 中配位离子所带电荷数为
中配位离子所带电荷数为___________ ,VSEPR模型为四面体的非金属原子共有___________ 个。 单晶的晶胞,其中原子坐标参数A为
单晶的晶胞,其中原子坐标参数A为 ;B为
;B为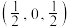 ;C为
;C为 。则D原子的坐标参数为
。则D原子的坐标参数为___________ 。
(1)基态
 原子核外电子的运动状态有
原子核外电子的运动状态有 易被氧化为
易被氧化为 ,画出
,画出 的结构示意图
的结构示意图(2)
 是检验
是检验 的特征试剂,
的特征试剂, 中心离子配位数是
中心离子配位数是 中含有
中含有 键,能够证明
键,能够证明 不能电离的试剂是
不能电离的试剂是(3)
 可形成配合物
可形成配合物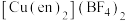 ,其中
,其中 代表
代表 分子。该配合物
分子。该配合物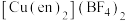 中配位离子所带电荷数为
中配位离子所带电荷数为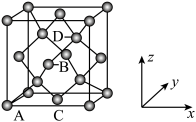
 单晶的晶胞,其中原子坐标参数A为
单晶的晶胞,其中原子坐标参数A为 ;B为
;B为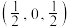 ;C为
;C为 。则D原子的坐标参数为
。则D原子的坐标参数为
您最近一年使用:0次
名校
2 . 第IIB族元素(Zn、Cd、Hg)和第VIA族元素(S、Se、Te)组成的某些二元化合物常用作半导体材料,应用十分广泛。
(1)基态Se原子价电子排布式为_______ ,有_______ 种空间运动状态。
(2)碲酸(H6TeO6)是白色固体,经X射线衍射研究证明在碲酸分子内的6个羟基排列在碲原子的周围成八面体结构,碲酸中碲原子的价层电子对数为_______ 。
(3)CdTe可用作太阳能电池的吸收层,研究从太阳能电池的碲化镉吸收层(主要含CdTe、CdS)中回收碲具有重要的意义。某回收工艺的流程如图:

①碲化镉吸收层中的CdTe参与反应的化学方程式为_______ ,该反应需要控制温度为50℃的原因为_______ ;滤渣1含有的一种单质是_______ 。
②常温下,向含Cd2+、Te4+滤液中加入NaOH溶液调节pH,当pH=10时,溶液中c(Cd2+)=_______ 。(已知Ksp[Cd(OH)2]=5.3×10-15)。
(1)基态Se原子价电子排布式为
(2)碲酸(H6TeO6)是白色固体,经X射线衍射研究证明在碲酸分子内的6个羟基排列在碲原子的周围成八面体结构,碲酸中碲原子的价层电子对数为
(3)CdTe可用作太阳能电池的吸收层,研究从太阳能电池的碲化镉吸收层(主要含CdTe、CdS)中回收碲具有重要的意义。某回收工艺的流程如图:

①碲化镉吸收层中的CdTe参与反应的化学方程式为
②常温下,向含Cd2+、Te4+滤液中加入NaOH溶液调节pH,当pH=10时,溶液中c(Cd2+)=
您最近一年使用:0次
名校
3 . 回答下列问题:
(1)根据价层电子对互斥模型, 分子中心原子孤电子对数是
分子中心原子孤电子对数是_______ , 分子的空间构型是
分子的空间构型是_______ 。
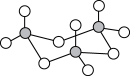
(2)气态三氧化硫以单分子形式存在,属于_______ 分子(填“极性”、“非极性”),固体三氧化硫中存在如图所示的三聚分子,该分子中S原子的杂化轨道类型为_______ 。
(3) 中心原子的价层电子对数为
中心原子的价层电子对数为_______ ,写出一个与 VEEPR模型相同的离子
VEEPR模型相同的离子_______ 。
(4)下列表述中,不能证明氯的非金属性比硫强的是_______ 。
A.气态氢化物的稳定性:
B.两元素的电负性: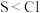
C.高价含氧酸的酸性: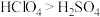
D.常温时,硫单质为固态,氯单质为气态
E.两者间可发生反应: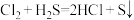
(1)根据价层电子对互斥模型,
 分子中心原子孤电子对数是
分子中心原子孤电子对数是 分子的空间构型是
分子的空间构型是(2)气态三氧化硫以单分子形式存在,属于

(3)
 中心原子的价层电子对数为
中心原子的价层电子对数为 VEEPR模型相同的离子
VEEPR模型相同的离子(4)下列表述中,不能证明氯的非金属性比硫强的是
A.气态氢化物的稳定性:

B.两元素的电负性:
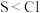
C.高价含氧酸的酸性:
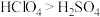
D.常温时,硫单质为固态,氯单质为气态
E.两者间可发生反应:
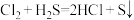
您最近一年使用:0次
名校
解题方法
4 . 根据物质结构的基本理论,原子之间通过原子轨道的重叠方式,以不同类型的化学键结合,形成具有不同空间结构的分子或离子,按照已学的物质结构知识填写下列空白。
(1)在 分子中,硼原子的电子排布式为
分子中,硼原子的电子排布式为___________ ,F-B-F的键角是___________ 。
(2) 可与
可与 形成
形成 ,
, 中氧原子采用
中氧原子采用___________ 杂化, 的空间立体构型为
的空间立体构型为___________ 。
(3)第ⅥA族元素(O、S、Se、Te),基态Se原子价电子排布式为_______ ,有___________ 个未成对电子;碲酸 是白色固体,经X射线研究证明在碲酸分子内的6个羟基排列在碲原子周围成八面体结构,碲酸中碲原子的价层电子对数为
是白色固体,经X射线研究证明在碲酸分子内的6个羟基排列在碲原子周围成八面体结构,碲酸中碲原子的价层电子对数为___________ 。
(1)在
 分子中,硼原子的电子排布式为
分子中,硼原子的电子排布式为(2)
 可与
可与 形成
形成 ,
, 中氧原子采用
中氧原子采用 的空间立体构型为
的空间立体构型为(3)第ⅥA族元素(O、S、Se、Te),基态Se原子价电子排布式为
 是白色固体,经X射线研究证明在碲酸分子内的6个羟基排列在碲原子周围成八面体结构,碲酸中碲原子的价层电子对数为
是白色固体,经X射线研究证明在碲酸分子内的6个羟基排列在碲原子周围成八面体结构,碲酸中碲原子的价层电子对数为
您最近一年使用:0次
名校
5 . 根据已学《物质结构与性质》的有关知识,回答下列问题:
(1)如图所示是元素周期表中第一、第二周期10种元素的某些性质的一组数据(所列数据的单位相同),除带“…”的四种元素外,其余元素都给出了该种元素的全部该类数据。
有些元素的逐级电离能中个别地方增大的比例(倍数)特别大,形成“突跃”,由此可以证明原子结构中_______________________ 的结论。根据这个规律,你认为氧元素8个电离能数据中出现“突跃”的数据应该是第________ 个。
(2)在①苯 ②CH3OH ③HCHO ④CS2 ⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有_____ (填序号),易溶于水的有_____ (填序号),理由是:____________ 。
(3)N≡N键的键能为946kJ·mol-1,N—N键的键能为193kJ·mol-1,则一个π键的平均键能为__________ ,说明N2中________ 键更稳定(填“σ”或“π”)。
(4)向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续滴加氨水,难溶物溶解,得到深蓝色的透明溶液,写出有关化学反应的离子方程式___________ 、____________ 。
(1)如图所示是元素周期表中第一、第二周期10种元素的某些性质的一组数据(所列数据的单位相同),除带“…”的四种元素外,其余元素都给出了该种元素的全部该类数据。
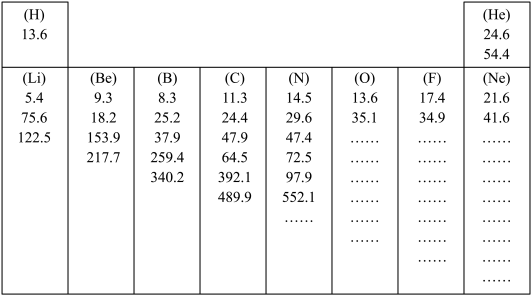
有些元素的逐级电离能中个别地方增大的比例(倍数)特别大,形成“突跃”,由此可以证明原子结构中
(2)在①苯 ②CH3OH ③HCHO ④CS2 ⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有
(3)N≡N键的键能为946kJ·mol-1,N—N键的键能为193kJ·mol-1,则一个π键的平均键能为
(4)向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续滴加氨水,难溶物溶解,得到深蓝色的透明溶液,写出有关化学反应的离子方程式
您最近一年使用:0次
名校
解题方法
6 . 下列关于N、O、F及其相关微粒的说法错误的是
A. 、OF2、NF3的键角大小顺序为 、OF2、NF3的键角大小顺序为 >NF3>OF2 >NF3>OF2 |
| B.基态N3-、O2-、F-核外电子空间运动状态均为5种 |
| C.N、O、F三种元素形成的单质分子均为非极性分子 |
D. 、 、 的VSEPR模型相同,均为平面三角形 的VSEPR模型相同,均为平面三角形 |
您最近一年使用:0次
昨日更新
|
87次组卷
|
3卷引用:江西省部分重点中学2024届高三下学期第二次联考化学试题
名校
解题方法
7 . 某化合物具漂白性,主要用于染色工艺,其结构如图所示,其中W、X、Y、M、Z是原子序数依次递增的短周期主族元素,且Y和 同主族,下列说法错误的是
同主族,下列说法错误的是
 同主族,下列说法错误的是
同主族,下列说法错误的是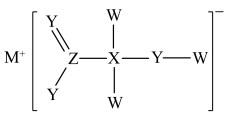
A.电负性: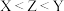 | B. 和 和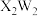 均为极性分子 均为极性分子 |
| C.MW与水反应后的溶液呈碱性 | D. 利 利 的VSEPR模型名称均为平面三角形 的VSEPR模型名称均为平面三角形 |
您最近一年使用:0次
7日内更新
|
166次组卷
|
2卷引用:湖北省武汉市2024届高三毕业生四月调研考试(二模)化学试题
名校
解题方法
8 . 由原子序数依次增大的短周期元素X、Y、Z、W、R组成的一种离子液体(其阳离子中五元环上5个原子共面),其结构如图。Z的最简单氢化物易液化,可用作制冷剂。W的氢化物的水溶液能腐蚀玻璃,Z、R为同一主族元素。下列说法错误的是
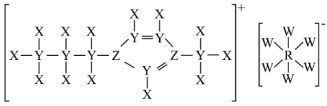
| A.电负性:W>Z>Y |
| B.该离子液体中的Z原子的杂化方式均为sp2 |
C.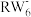 空间结构为正八面体形 空间结构为正八面体形 |
| D.最简单氢化物的沸点:Z<R |
您最近一年使用:0次
解题方法
9 . 已知NaBiO3制MnO 的离子方程式为5NaBiO3+2Mn2++14H+=2MnO
的离子方程式为5NaBiO3+2Mn2++14H+=2MnO +5Na++5Bi3++7H2O,下列说法错误的是
+5Na++5Bi3++7H2O,下列说法错误的是
 的离子方程式为5NaBiO3+2Mn2++14H+=2MnO
的离子方程式为5NaBiO3+2Mn2++14H+=2MnO +5Na++5Bi3++7H2O,下列说法错误的是
+5Na++5Bi3++7H2O,下列说法错误的是| A.上述反应需要在硫酸酸化的环境中进行 |
B.H2O的VSEPR模型为: |
| C.基态Bi3+的价电子排布式为6s2 |
D.用浓盐酸溶解NaBiO3的离子方程式为BiO +2Cl-+6H+=Cl2↑+Bi3++3H2O +2Cl-+6H+=Cl2↑+Bi3++3H2O |
您最近一年使用:0次
解题方法
10 . NCl3和SiCl4均可发生水解反应,其中NCl3的水解机理示意图如下:
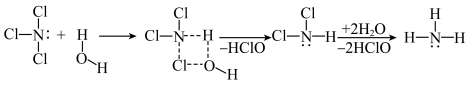
| A.NCl3和SiCl4的水解反应机理不相同 | B.NCl3中键角小于NH3中键角 |
| C.NHCl2和NH3均能与H2O形成氢键 | D.NCl3和SiCl4中心原子的杂化方式不同 |
您最近一年使用:0次



