名校
解题方法
1 . 化合物H是制备药物洛索洛芬钠的关键中间体,其一种合成路线如图:
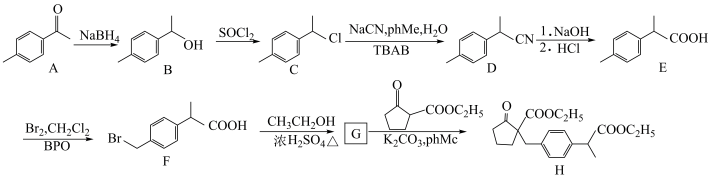
(1)A的分子式________ ﹔B→C的反应类型________ 。
(2)B的含氧官能团名称________ ;D中氮(N)的杂化方式_______ 。
(3)G的结构简式_______ 。
(4)F→G反应中乙醇可能发生的副反应方程式_______ 。
(5)F的一种同分异构体同时满足下列条件,写出任意一种该同分异构体的结构简式_______ 。
①分子中含有苯环;
②不能与Na2CO3反应生成CO2;
③含有手性碳原子。

(1)A的分子式
(2)B的含氧官能团名称
(3)G的结构简式
(4)F→G反应中乙醇可能发生的副反应方程式
(5)F的一种同分异构体同时满足下列条件,写出任意一种该同分异构体的结构简式
①分子中含有苯环;
②不能与Na2CO3反应生成CO2;
③含有手性碳原子。
您最近一年使用:0次
名校
解题方法
2 . 下列对分子性质的解释中,不正确的是


| A.在氨水中,大部分NH3与H2O以氢键(用“⋯”表示)结合形成NH3·H2O分子,则NH3·H2O的结构式如图1 |
B. 和 和 的中心原子杂化方式不同,前者是 的中心原子杂化方式不同,前者是 后者是 后者是 |
C. 、 、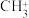 、 、 的空间构型相同 的空间构型相同 |
D.由如图2可知酸性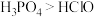 ,因为 ,因为 分子中有1个非羟基氧原子 分子中有1个非羟基氧原子 |
您最近一年使用:0次
3 . 有机化合物F是一种镇痛药,它的合成路线如下:
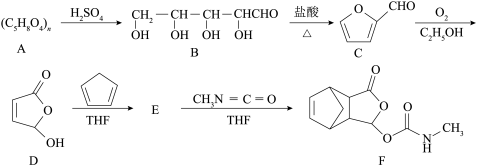
(1)B分子中含氧官能团的名称为_______ 。
(2)D分子中采取sp2杂化的碳原子数目是_______ 。
(3)已知E+CH3N=C=O → F为加成反应,中间体E的结构式为_______ 。
(4)F的同分异构体同时满足下列条件,写出一种该同分异构体的结构简式:_______ 。
I.核磁共振氢谱有3个峰,苯环上的一取代物有2种;
II.能发生水解反应,酸性条件下水解产物之一能与FeCl3溶液发生显色反应。
(5)请以2—戊烯和 CH2=CHCHO为原料制备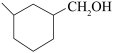 ,写出制备的合成路线流程图
,写出制备的合成路线流程图_______ 。(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)

(1)B分子中含氧官能团的名称为
(2)D分子中采取sp2杂化的碳原子数目是
(3)已知E+CH3N=C=O → F为加成反应,中间体E的结构式为
(4)F的同分异构体同时满足下列条件,写出一种该同分异构体的结构简式:
I.核磁共振氢谱有3个峰,苯环上的一取代物有2种;
II.能发生水解反应,酸性条件下水解产物之一能与FeCl3溶液发生显色反应。
(5)请以2—戊烯和 CH2=CHCHO为原料制备
 ,写出制备的合成路线流程图
,写出制备的合成路线流程图
您最近一年使用:0次
名校
4 . 锂离子电池让电动汽车飞速发展,有利于实现节能减排。LiCoO2、LiFePO4、Li4Ti5O12常用作电池的电极材料,LiPF6、LiAsF6常用作锂离子聚合物电池的载体材料。
(1)在周期表中,与Li的化学性质最相似的邻族元素是_______ ,LiCoO2中基态Co原子核外电子的空间运动状态有_______ 种。
(2)含氧酸的通式可写为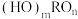 ,,根据含氧酸的结构规律,下列酸中酸性与H3PO4相近的有_______(填字母)。
,,根据含氧酸的结构规律,下列酸中酸性与H3PO4相近的有_______(填字母)。
(3)电池工作时,Li+计可在电解质LiPF6或LiAsF6中发生迁移,相同条件下,Li+在_______ (填“LiPF6”或“LiAsF6”)中迁移较快,原因是_______ 。
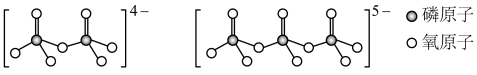
(4)LiFePO4中P的_______ 杂化轨道与O的2p轨道形成 键。LiFePO4属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如下图所示,这类磷酸根离子的化学式可用通式表示为
键。LiFePO4属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如下图所示,这类磷酸根离子的化学式可用通式表示为_______ (用n代表P原子数)。
(5)Li4Ti5O12中Ti元素的化合物TiO2是一种重要的瓷器釉料。研究表明,在TiO2中通过氮掺杂反应可生成TiO2-aNb,能使TiO2对可见光具有活性,掺杂过程如图所示。
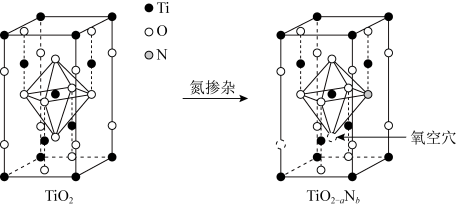
则TiO2-aNb晶体中a=_______ ,b=_______ 。
(1)在周期表中,与Li的化学性质最相似的邻族元素是
(2)含氧酸的通式可写为
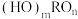 ,,根据含氧酸的结构规律,下列酸中酸性与H3PO4相近的有_______(填字母)。
,,根据含氧酸的结构规律,下列酸中酸性与H3PO4相近的有_______(填字母)。| A.HClO | B.H2SO4 | C.HNO2 | D.HNO3 |
(4)LiFePO4中P的
 键。LiFePO4属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如下图所示,这类磷酸根离子的化学式可用通式表示为
键。LiFePO4属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如下图所示,这类磷酸根离子的化学式可用通式表示为
(5)Li4Ti5O12中Ti元素的化合物TiO2是一种重要的瓷器釉料。研究表明,在TiO2中通过氮掺杂反应可生成TiO2-aNb,能使TiO2对可见光具有活性,掺杂过程如图所示。

则TiO2-aNb晶体中a=
您最近一年使用:0次
名校
解题方法
5 . 材料是人类文明进步的阶梯,第IIIA、IVA、VA族元素是组成特殊材料的重要元素。请回答下列问题:
(1)根据价层电子对互斥理论, 、
、 、
、 中,中心原子价层电子对数不同于其他两种粒子的是
中,中心原子价层电子对数不同于其他两种粒子的是_______ ,已知 与
与 互为等电子体,推算HCN分子中σ键与π键的数目比为
互为等电子体,推算HCN分子中σ键与π键的数目比为_______ 。
(2)M与Ga位于同周期, 的一种配合物组成为
的一种配合物组成为 。
。
①下列有关 、
、 的说法正确的是
的说法正确的是_______ (填字母)。
a.分子空间构型相同 b.中心原子杂化类型相同 c.键角大小相同
② 配体是
配体是_______ 。
③配合物T与 组成元素相同,中心离子的配位数相同。1moT溶于水,加入足量
组成元素相同,中心离子的配位数相同。1moT溶于水,加入足量 溶液只生成2molAgCl沉淀,则T的化学式为
溶液只生成2molAgCl沉淀,则T的化学式为_______ 。
(3)磷化硼(BP)是受高度关注的耐磨材料,可作为金属农面的保护层,其结构与金刚石类似,晶胞结构如图所示,磷化硼晶胞沿z轴在平面的投影图中,B原子构成的几何形状是_______ 。
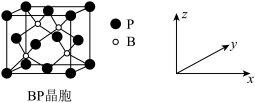
(4)已知晶胞中B与P原子最短距离为a pm,则磷化硼晶体的密度是_______  (仅列式不计算)。
(仅列式不计算)。
(1)根据价层电子对互斥理论,
 、
、 、
、 中,中心原子价层电子对数不同于其他两种粒子的是
中,中心原子价层电子对数不同于其他两种粒子的是 与
与 互为等电子体,推算HCN分子中σ键与π键的数目比为
互为等电子体,推算HCN分子中σ键与π键的数目比为(2)M与Ga位于同周期,
 的一种配合物组成为
的一种配合物组成为 。
。①下列有关
 、
、 的说法正确的是
的说法正确的是a.分子空间构型相同 b.中心原子杂化类型相同 c.键角大小相同
②
 配体是
配体是③配合物T与
 组成元素相同,中心离子的配位数相同。1moT溶于水,加入足量
组成元素相同,中心离子的配位数相同。1moT溶于水,加入足量 溶液只生成2molAgCl沉淀,则T的化学式为
溶液只生成2molAgCl沉淀,则T的化学式为(3)磷化硼(BP)是受高度关注的耐磨材料,可作为金属农面的保护层,其结构与金刚石类似,晶胞结构如图所示,磷化硼晶胞沿z轴在平面的投影图中,B原子构成的几何形状是

(4)已知晶胞中B与P原子最短距离为a pm,则磷化硼晶体的密度是
 (仅列式不计算)。
(仅列式不计算)。
您最近一年使用:0次
2022-12-27更新
|
197次组卷
|
2卷引用:福建省福州市福建师范大学附属中学2021-2022学年高二下学期期中考试化学试题
名校
解题方法
6 . 研究发现,在CO2低压合成甲醇反应(CO2+3H2=CH3OH+H2O)中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
(1) 基态原子电子排布式为
基态原子电子排布式为_______ 。元素 与O中,第一电离能较大的是
与O中,第一电离能较大的是_______ ,基态原子核外未成对电子数较多的是_______ 。
(2)CO2和CH3OH分子中C原子的杂化形式分别为_______ 和_______ 。
(3)在CO2低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为_______ ,原因是_______ 。
(4)硝酸锰是制备上述反应催化剂的原料,Mn(NO3)2中的化学键除了σ键外,还存在_______ 。
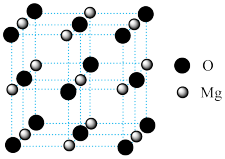
(5)MgO具有NaCl型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得MgO的晶胞参数为a=0.420nm,则r(O2-)为_______  。该晶体的密度为
。该晶体的密度为_______  (列出计算式,NA为阿伏加德罗常数的值)。
(列出计算式,NA为阿伏加德罗常数的值)。
(1)
 基态原子电子排布式为
基态原子电子排布式为 与O中,第一电离能较大的是
与O中,第一电离能较大的是(2)CO2和CH3OH分子中C原子的杂化形式分别为
(3)在CO2低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为
(4)硝酸锰是制备上述反应催化剂的原料,Mn(NO3)2中的化学键除了σ键外,还存在
(5)MgO具有NaCl型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得MgO的晶胞参数为a=0.420nm,则r(O2-)为
 。该晶体的密度为
。该晶体的密度为 (列出计算式,NA为阿伏加德罗常数的值)。
(列出计算式,NA为阿伏加德罗常数的值)。
您最近一年使用:0次
名校
解题方法
7 . 氮、氧、磷、砷及其化合物在工农业生产等方面有着重要应用。请按要求回答下列问题。
(1)基态砷原子价电子排布图不能写为 ,是因为该排布方式违背了
,是因为该排布方式违背了__________ 这一原理。
(2)元素第一电离能N______ O(填“>”或“<”或“=”,下同),电负性P______  。
。
(3)肼 可用作火箭燃料等,它的沸点远高于乙烯的原因是:
可用作火箭燃料等,它的沸点远高于乙烯的原因是:__________ 。
(4)尿素( )中碳原子杂化类型
)中碳原子杂化类型__________ ; 离子的立体构型(即空间构型)为
离子的立体构型(即空间构型)为__________ 。
(5) 的熔点为1238℃可作半导体材料;而
的熔点为1238℃可作半导体材料;而 的熔点为77.9℃。
的熔点为77.9℃。
①预测 的晶体类型为
的晶体类型为__________ 。
② 晶胞结构如图所示,晶胞边长为
晶胞结构如图所示,晶胞边长为 。则晶胞中每个
。则晶胞中每个 原子周围有
原子周围有__________ 个紧邻等距的 原子;该晶体的密度为
原子;该晶体的密度为__________  (列出计算式)。
(列出计算式)。

(1)基态砷原子价电子排布图不能写为
 ,是因为该排布方式违背了
,是因为该排布方式违背了(2)元素第一电离能N
 。
。(3)肼
 可用作火箭燃料等,它的沸点远高于乙烯的原因是:
可用作火箭燃料等,它的沸点远高于乙烯的原因是:(4)尿素(
 )中碳原子杂化类型
)中碳原子杂化类型 离子的立体构型(即空间构型)为
离子的立体构型(即空间构型)为(5)
 的熔点为1238℃可作半导体材料;而
的熔点为1238℃可作半导体材料;而 的熔点为77.9℃。
的熔点为77.9℃。①预测
 的晶体类型为
的晶体类型为②
 晶胞结构如图所示,晶胞边长为
晶胞结构如图所示,晶胞边长为 。则晶胞中每个
。则晶胞中每个 原子周围有
原子周围有 原子;该晶体的密度为
原子;该晶体的密度为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
2022-11-20更新
|
1002次组卷
|
6卷引用:天津市河北区2022-2023学年高三上学期期中质量检测化学试题
天津市河北区2022-2023学年高三上学期期中质量检测化学试题(已下线)北京市海淀区2022届高三一模(结构与性质)(已下线)2022年天津市普通高中学业水平等级性考试化学试题变式题(结构与性质)(已下线)期中模拟预测卷03(测试范围:选择性必修2+选择性必修3第1-2章)-2022-2023学年高二化学下学期期中期末考点大串讲(人教版2019)宁夏青铜峡市宁朔中学2022-2023学年高二下学期期中考试化学试题吉林省吉林松花江中学2022-2023学年高二上学期1月期末考试化学试题
名校
解题方法
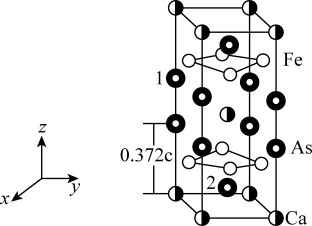
8 . 最近合成的一种铁基超导材料 ,在低温高压下能显示出独特的电子性质,晶胞结构如图所示,回答下列问题:
,在低温高压下能显示出独特的电子性质,晶胞结构如图所示,回答下列问题:
(1)Fe的基态原子共有_______ 种不同能级的电子。
(2) 的沸点(1935℃)高于
的沸点(1935℃)高于 的沸点(130.2℃)原因是
的沸点(130.2℃)原因是_______ 。
(3)Fe可以与CO、NO、 等多种微粒形成配合物。
等多种微粒形成配合物。
①C、N、O的第一电离能由大到小的顺序为_______ 。
②写出 的一种等电子体分子
的一种等电子体分子_______ 。
(4) 溶液中含有的微粒内部及微粒间作用力除共价键外还有
溶液中含有的微粒内部及微粒间作用力除共价键外还有_______ ,溶质阴离子的中心原子杂化轨道类型为_______ 。
(5)该材料的化学式为_______ ,已知:体心的Ca原子与顶点的Ca原子有着相同的化学环境(化学环境受周围粒子的数目与距离所影响),该晶胞的晶胞参数为a pm、a pm、c pm,晶胞中As原子1分数坐标为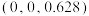 ,则As原子2的分数坐标为
,则As原子2的分数坐标为_______ 。
 ,在低温高压下能显示出独特的电子性质,晶胞结构如图所示,回答下列问题:
,在低温高压下能显示出独特的电子性质,晶胞结构如图所示,回答下列问题:
(1)Fe的基态原子共有
(2)
 的沸点(1935℃)高于
的沸点(1935℃)高于 的沸点(130.2℃)原因是
的沸点(130.2℃)原因是(3)Fe可以与CO、NO、
 等多种微粒形成配合物。
等多种微粒形成配合物。①C、N、O的第一电离能由大到小的顺序为
②写出
 的一种等电子体分子
的一种等电子体分子(4)
 溶液中含有的微粒内部及微粒间作用力除共价键外还有
溶液中含有的微粒内部及微粒间作用力除共价键外还有(5)该材料的化学式为
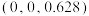 ,则As原子2的分数坐标为
,则As原子2的分数坐标为
您最近一年使用:0次
2022-11-13更新
|
104次组卷
|
2卷引用:福建省宁德市2022-2023学年高三上学期期中区域性学业质量检测化学试题
名校
解题方法
9 . Ⅰ.在下列物质中:①HCl②NH3③Na2O2④C2H4⑤NaOH⑥Ar⑦H2O2
(1)既存在离子键又存在极性键的是_______ (填序号,下同)。
(2)不存在化学键的是_______ 。
(3)既存在极性键又存在非极性键的极性分子是_______ 。
(4)NH3分子的空间构型为_______ ,与该分子互为等电子体的阳离子为_______ (填化学式,只写一种即可)。
Ⅱ.原子序数小于36的X、Y、Z、W、J、G六种元素,原子序数依次增大,其中X元素的原子在所有原子中半径最小,Y元素原子核外有三种不同的能级且各个能级所填充的电子数相同,W元素原子最外层电子数是内层电子数的3倍,J元素原子核外的3p能级有两个电子,G元素原子核外有6个未成对电子(用元素符号或化学式表示)。
(5)写出G元素的基态原子的价电子排布式_______ ;Y2X2分子中σ键与π键数目之比为_______ 。
(6)Y、Z、W三种元素第一电离能由大到小的顺序为_______ (用元素符号表示)。
(7)ZX3在水中的溶解度较大,可能的原因有_______ 、_______ 。(写出两个即可)
(8)判断J与W形成的化合物JW2是晶体还是非晶体,最科学的办法是_______ ;XYZ分子中Y原子轨道的杂化类型为_______ 。
(9)G元素有δ、γ、α三种同素异形体,晶胞结构如图所示。三种晶体的晶胞中所含有的G原子数之比为_______ 。

(1)既存在离子键又存在极性键的是
(2)不存在化学键的是
(3)既存在极性键又存在非极性键的极性分子是
(4)NH3分子的空间构型为
Ⅱ.原子序数小于36的X、Y、Z、W、J、G六种元素,原子序数依次增大,其中X元素的原子在所有原子中半径最小,Y元素原子核外有三种不同的能级且各个能级所填充的电子数相同,W元素原子最外层电子数是内层电子数的3倍,J元素原子核外的3p能级有两个电子,G元素原子核外有6个未成对电子(用元素符号或化学式表示)。
(5)写出G元素的基态原子的价电子排布式
(6)Y、Z、W三种元素第一电离能由大到小的顺序为
(7)ZX3在水中的溶解度较大,可能的原因有
(8)判断J与W形成的化合物JW2是晶体还是非晶体,最科学的办法是
(9)G元素有δ、γ、α三种同素异形体,晶胞结构如图所示。三种晶体的晶胞中所含有的G原子数之比为

您最近一年使用:0次
名校
10 . 含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种原子序数为48的Cd2+配合物的结构如图所示,则下列说法正确的是
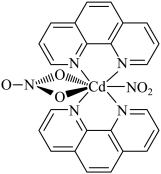

| A.该螯合物中N的杂化方式有2种 |
| B.1mol该配合物中通过螯合作用形成的配位键有6mol |
| C.Cd属于d区元素 |
| D.Cd的价电子排布式为4d85s2 |
您最近一年使用:0次
2022-11-07更新
|
918次组卷
|
3卷引用:四川省内江市第六中学2022-2023学年高二上学期期中考试化学试题



