解题方法
1 . 碳是一种很常见的元素,它能形成多种物质。
(1)碳与铁可以形成合金。
①基态碳原子的价电子排布图(即价电子轨道表示式)为___________ ;基态铁原子核外共有___________ 种不同空间运动状态的电子。
②从结构角度分析, 较
较 稳定的原因是
稳定的原因是___________ 。
(2)碳与其他元素一起能形成多种酸或酸根。
① 的空间构型是
的空间构型是___________ 。
②类卤素 分子中σ键与π键的数目比
分子中σ键与π键的数目比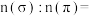
___________ 。 对应的酸有两种,理论上硫氰酸(
对应的酸有两种,理论上硫氰酸( )的沸点低于异硫氰酸(
)的沸点低于异硫氰酸(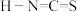 )的沸点,其原因是
)的沸点,其原因是___________ 。
(3)碳也可以形成多种有机化合物。
①有机物尿素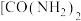 。尿素中C、N、O第一电离能大小顺序为
。尿素中C、N、O第一电离能大小顺序为___________ 。
②吡咯(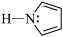 )结构中N原子的杂化轨道类型为
)结构中N原子的杂化轨道类型为___________ ;分子中的大π键可以用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为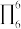 ),则吡咯中的大π键应表示为
),则吡咯中的大π键应表示为___________ 。
(4)碳还能形成多种同素异形体,如石墨、金刚石等。
①石墨具有平面层状结构,同一层中的原子构成许许多多的正六边形,它与熔融的K单质相互作用,形成某种青铜色的物质(其中的元素K用“●”表示),原子分布如图甲所示,该物质的化学式为___________ 。
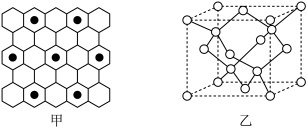
(图中的○表示碳形成的正四面体结构 )
)
②2017年,中外科学家团队共同合成了碳的一种新型同素异形体:T-碳。T-碳的结构是将立方金刚石中的每个碳原子用一个由4个碳原子组成的正四面体结构单元取代,可形成碳的一种新型三维立方晶体结构——T-碳(如图乙)。已知T-碳密度为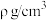 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则T-碳的晶胞参数
,则T-碳的晶胞参数
___________ pm(写出表达式即可)。
(1)碳与铁可以形成合金。
①基态碳原子的价电子排布图(即价电子轨道表示式)为
②从结构角度分析,
 较
较 稳定的原因是
稳定的原因是(2)碳与其他元素一起能形成多种酸或酸根。
①
 的空间构型是
的空间构型是②类卤素
 分子中σ键与π键的数目比
分子中σ键与π键的数目比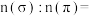
 对应的酸有两种,理论上硫氰酸(
对应的酸有两种,理论上硫氰酸( )的沸点低于异硫氰酸(
)的沸点低于异硫氰酸(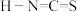 )的沸点,其原因是
)的沸点,其原因是(3)碳也可以形成多种有机化合物。
①有机物尿素
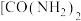 。尿素中C、N、O第一电离能大小顺序为
。尿素中C、N、O第一电离能大小顺序为②吡咯(
 )结构中N原子的杂化轨道类型为
)结构中N原子的杂化轨道类型为 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为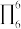 ),则吡咯中的大π键应表示为
),则吡咯中的大π键应表示为(4)碳还能形成多种同素异形体,如石墨、金刚石等。
①石墨具有平面层状结构,同一层中的原子构成许许多多的正六边形,它与熔融的K单质相互作用,形成某种青铜色的物质(其中的元素K用“●”表示),原子分布如图甲所示,该物质的化学式为

(图中的○表示碳形成的正四面体结构
 )
)②2017年,中外科学家团队共同合成了碳的一种新型同素异形体:T-碳。T-碳的结构是将立方金刚石中的每个碳原子用一个由4个碳原子组成的正四面体结构单元取代,可形成碳的一种新型三维立方晶体结构——T-碳(如图乙)。已知T-碳密度为
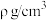 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则T-碳的晶胞参数
,则T-碳的晶胞参数
您最近一年使用:0次
解题方法
2 . “中国紫”——硅酸铜钡( ),其合成原料为
),其合成原料为 、孔雀石[
、孔雀石[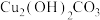 ]和砂子(
]和砂子( )。回答下列问题:
)。回答下列问题:
(1)基态Ba原子的价电子排布式为_______ 。
(2) 常用作光导纤维,在生产和生活中有广泛的用途。
常用作光导纤维,在生产和生活中有广泛的用途。
① 属于
属于_______ 晶体,在 晶体中,硅原子的杂化类型为
晶体中,硅原子的杂化类型为_______ , 的空间构型为
的空间构型为_______ 。
②1mol 晶体中,Si-O键的数目为
晶体中,Si-O键的数目为_______ 。
(3)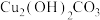 不溶于水,但可溶于浓氨水,反应的化学方程式为
不溶于水,但可溶于浓氨水,反应的化学方程式为
 。
。
①氨水中存在的化学键有_______ (填标号)。
A.极性键 B.非极性键 C.氢键 D.σ键 E.π键
② 中配体是
中配体是_______ ,所含元素中电负性最小的非金属元素是_______ (填元素符号)。
(4) 的熔点比
的熔点比 的
的_______ (填“高”或“低”),原因是_______ 。
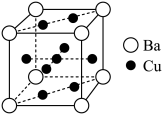
(5)Cu和Ba形成的某种合金的晶胞结构如图所示,设 为阿伏加德罗常数的值,晶胞参数为a nm,则该晶体的密度
为阿伏加德罗常数的值,晶胞参数为a nm,则该晶体的密度
_______ (列出计算式) 。
。
 ),其合成原料为
),其合成原料为 、孔雀石[
、孔雀石[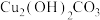 ]和砂子(
]和砂子( )。回答下列问题:
)。回答下列问题:(1)基态Ba原子的价电子排布式为
(2)
 常用作光导纤维,在生产和生活中有广泛的用途。
常用作光导纤维,在生产和生活中有广泛的用途。①
 属于
属于 晶体中,硅原子的杂化类型为
晶体中,硅原子的杂化类型为 的空间构型为
的空间构型为②1mol
 晶体中,Si-O键的数目为
晶体中,Si-O键的数目为(3)
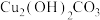 不溶于水,但可溶于浓氨水,反应的化学方程式为
不溶于水,但可溶于浓氨水,反应的化学方程式为
 。
。①氨水中存在的化学键有
A.极性键 B.非极性键 C.氢键 D.σ键 E.π键
②
 中配体是
中配体是(4)
 的熔点比
的熔点比 的
的(5)Cu和Ba形成的某种合金的晶胞结构如图所示,设
 为阿伏加德罗常数的值,晶胞参数为a nm,则该晶体的密度
为阿伏加德罗常数的值,晶胞参数为a nm,则该晶体的密度
 。
。
您最近一年使用:0次
名校
解题方法
3 . 元素周期表第IIIA族包括B、Al、Ga等元素,它们参与形成的化合物有重要研究和应用价值,回答下列问题:
(1)基态Ga原子的价电子排布式为________ ;Ga、As和Se的第一电离能由小到大的顺序是________ 。
(2)实验发现,氯化铝溶于非极性溶剂中或处于熔融状态、蒸气状态时,都以二聚态(A12C16)的形式存在。其球棍模型如图甲所示。

①该分子中A1原子采取________ 杂化。
②Al2Cl6与过量NaOH溶液反应生成Na[A1(OH)4],[A1(OH)4]-中存在的化学键有________ (序号)。
A.离子键 B.极性共价键 C.金属键 D.非极性共价键 E.配位键 F.σ键 G.氢键
(3)更高温度下Al2Cl6二聚体离解成A1Cl3,BF3是AlCl3的一种等电子体,根据价层电子对互斥理论判断BF3的分子构型为________ ;写出BF3的一种带负电荷的等电子体粒子:________ 。
(4)GaN是第三代半导体材料的研究热点,在干燥的NH3气流中焙烧磨细的GaAs可制得GaN。GaN熔点约为1500℃,GaAs熔点为1238℃,GaN熔点高于GaAs的原因是________ 。
(5)GaN的其中一种晶胞结构如图乙所示,与金刚石的晶体结构高度相似。该晶胞中Ga原子处于N原子形成的________ (填“正四面体形”或“正八面体形”)空隙。已知GaN的密度为ρg•cm-3,Ga和N的摩尔质量分别为ag•moL-1和bg•moL-1,NA为阿伏加德罗常数,则GaN晶胞的边长为________ pm(列出表达式)。

(1)基态Ga原子的价电子排布式为
(2)实验发现,氯化铝溶于非极性溶剂中或处于熔融状态、蒸气状态时,都以二聚态(A12C16)的形式存在。其球棍模型如图甲所示。

①该分子中A1原子采取
②Al2Cl6与过量NaOH溶液反应生成Na[A1(OH)4],[A1(OH)4]-中存在的化学键有
A.离子键 B.极性共价键 C.金属键 D.非极性共价键 E.配位键 F.σ键 G.氢键
(3)更高温度下Al2Cl6二聚体离解成A1Cl3,BF3是AlCl3的一种等电子体,根据价层电子对互斥理论判断BF3的分子构型为
(4)GaN是第三代半导体材料的研究热点,在干燥的NH3气流中焙烧磨细的GaAs可制得GaN。GaN熔点约为1500℃,GaAs熔点为1238℃,GaN熔点高于GaAs的原因是
(5)GaN的其中一种晶胞结构如图乙所示,与金刚石的晶体结构高度相似。该晶胞中Ga原子处于N原子形成的

您最近一年使用:0次
解题方法
4 . 离子液体被认为是21世纪理想的绿色溶剂,是指室温或者接近室温时呈液态,而本身由阴、阳离子构成的化合物。氯代1-丁基-3-甲基咪唑离子液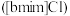 可以与
可以与 混合形成离子液体;
混合形成离子液体;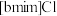 也可以转化成其他离子液体,下图是
也可以转化成其他离子液体,下图是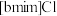 与
与 离子交换反应合成离子液体
离子交换反应合成离子液体 的流程:
的流程:

(1)请画出基态Ga原子的价电子排布图_____ ;同周期元素中基态原子未成对电子数与硼(B)原子相同的有_____ (填元素符号)。
(2)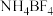 中N原子的杂化方式为
中N原子的杂化方式为_____ ,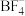 的空间构型为
的空间构型为_____ , 中几种元素电负性由大到小的顺序为
中几种元素电负性由大到小的顺序为_____ 。
(3)已知分子中的大 键可以用
键可以用 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表大
键的原子数,n代表大 键中的电子数,则
键中的电子数,则 中大
中大 键可以表示为
键可以表示为_____ 。
(4) 熔点为
熔点为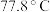 ,则
,则 的晶体类型为
的晶体类型为_____ , 和
和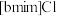 混合形成离子液体的过程中会存在以下转化:
混合形成离子液体的过程中会存在以下转化: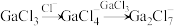 ,请画出
,请画出 的结构式
的结构式_____ 。
(5)某种 的晶胞结构如图所示,O2−以六方最密方式堆积,
的晶胞结构如图所示,O2−以六方最密方式堆积, 在其八面体空隙中(注:未全部标出,如:
在其八面体空隙中(注:未全部标出,如: 在1、2、3、4、5、6构成的八面体体心)。
在1、2、3、4、5、6构成的八面体体心)。
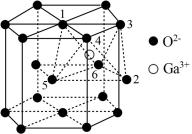
①该晶胞中O2−的配位数为_____ 。
②已知氧离子半径为acm,晶胞的高为bcm,NA代表阿伏加德罗常数的值,该晶体的密度为_____ g·cm−3(用含 和NA的代数式表示)。
和NA的代数式表示)。
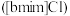 可以与
可以与 混合形成离子液体;
混合形成离子液体;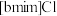 也可以转化成其他离子液体,下图是
也可以转化成其他离子液体,下图是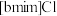 与
与 离子交换反应合成离子液体
离子交换反应合成离子液体 的流程:
的流程:
(1)请画出基态Ga原子的价电子排布图
(2)
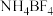 中N原子的杂化方式为
中N原子的杂化方式为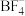 的空间构型为
的空间构型为 中几种元素电负性由大到小的顺序为
中几种元素电负性由大到小的顺序为(3)已知分子中的大
 键可以用
键可以用 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表大
键的原子数,n代表大 键中的电子数,则
键中的电子数,则 中大
中大 键可以表示为
键可以表示为(4)
 熔点为
熔点为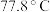 ,则
,则 的晶体类型为
的晶体类型为 和
和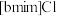 混合形成离子液体的过程中会存在以下转化:
混合形成离子液体的过程中会存在以下转化: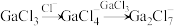 ,请画出
,请画出 的结构式
的结构式(5)某种
 的晶胞结构如图所示,O2−以六方最密方式堆积,
的晶胞结构如图所示,O2−以六方最密方式堆积, 在其八面体空隙中(注:未全部标出,如:
在其八面体空隙中(注:未全部标出,如: 在1、2、3、4、5、6构成的八面体体心)。
在1、2、3、4、5、6构成的八面体体心)。
①该晶胞中O2−的配位数为
②已知氧离子半径为acm,晶胞的高为bcm,NA代表阿伏加德罗常数的值,该晶体的密度为
 和NA的代数式表示)。
和NA的代数式表示)。
您最近一年使用:0次
名校
5 . 碳及钾元素形成的单质及其化合物有重要的应用。回答下列问题:
(1)放射性同位素 常用于测定古生物体的年龄,它可由中子轰击A原子制得:
常用于测定古生物体的年龄,它可由中子轰击A原子制得: 。则基态A原子的价电子排布式为
。则基态A原子的价电子排布式为_____ ;第四周期副族元素基态原子中,与A含有相同未成对电子数相同的元素有_____ (填元素符号)。
(2)碳元素可与氮等其他元素形成许多胺类物质,其中烟碱和多巴胺的结构如下:

烟碱中N原子的杂化方式为_____ ;多巴胺的沸点比烟碱高,其原因为_____ 。
(3) 可用于超微量Cu(Ⅱ)的测定。
可用于超微量Cu(Ⅱ)的测定。 中阴离子空间构型是
中阴离子空间构型是_____ ,与其互为等电子体的一种分子为_____ 。
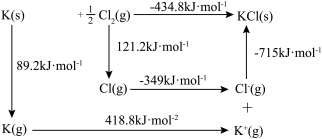
(4)KCl可用作氮肥的生产,其晶体的晶格能可通过下图热化学循环计算得到。则K原子的第一电离能为_____  ,Cl—Cl键键能为
,Cl—Cl键键能为_____  。
。
(5)石墨层间插入碱金属K可形成一系列夹层化合物,其导电性和磁性发生很大的变化。某种夹层化合物的结构如下图所示,每隔两层插入一层钾原子,与钾层相邻的上下两层碳原子的排列方式相同。
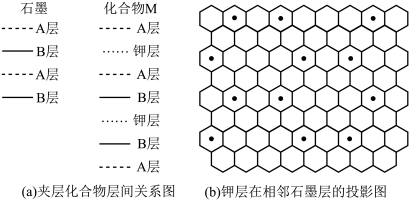
图(b)中正六边形的顶点代表碳原子,黑点代表钾原子。
①距离钾原子最近的碳原子的个数为_____ ;该夹层化合物的化学式为_____ 。
②若钾层相邻两个K之间的最近距离为dpm,则石墨层中C—C键键长为_____ pm。
(1)放射性同位素
 常用于测定古生物体的年龄,它可由中子轰击A原子制得:
常用于测定古生物体的年龄,它可由中子轰击A原子制得: 。则基态A原子的价电子排布式为
。则基态A原子的价电子排布式为(2)碳元素可与氮等其他元素形成许多胺类物质,其中烟碱和多巴胺的结构如下:

烟碱中N原子的杂化方式为
(3)
 可用于超微量Cu(Ⅱ)的测定。
可用于超微量Cu(Ⅱ)的测定。 中阴离子空间构型是
中阴离子空间构型是(4)KCl可用作氮肥的生产,其晶体的晶格能可通过下图热化学循环计算得到。则K原子的第一电离能为
 ,Cl—Cl键键能为
,Cl—Cl键键能为 。
。
(5)石墨层间插入碱金属K可形成一系列夹层化合物,其导电性和磁性发生很大的变化。某种夹层化合物的结构如下图所示,每隔两层插入一层钾原子,与钾层相邻的上下两层碳原子的排列方式相同。

图(b)中正六边形的顶点代表碳原子,黑点代表钾原子。
①距离钾原子最近的碳原子的个数为
②若钾层相邻两个K之间的最近距离为dpm,则石墨层中C—C键键长为
您最近一年使用:0次
名校
解题方法
6 . 中国科学家合成了首例缺陷诱导的晶态无机硼酸盐单一组分白光材料 ,并获得该化合物的
,并获得该化合物的 器件,该结果有望为白光发射的设计和应用提供新的有效策略。
器件,该结果有望为白光发射的设计和应用提供新的有效策略。
(1)已知 与
与 同族,基态
同族,基态 原子价层电子的运动状态有
原子价层电子的运动状态有_________ 种,基态 原子的电子排布式不能表示为
原子的电子排布式不能表示为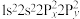 ,因为这违背了
,因为这违背了_________ (填选项)。
A.能量最低原理 B.泡利不相容原理 C.洪特规则
(2) 中硼原子的杂化轨道类型为
中硼原子的杂化轨道类型为_________ 。 中,
中, 与
与 之间不存在的化学键是
之间不存在的化学键是_________ (填选项)。
A. 键 B.
键 B.  键 C. 配位键 D. 极性键
键 C. 配位键 D. 极性键
(3)碳酸钡、碳酸镁分解得到的金属氧化物中,熔点较低的是_________ ,其原因是__________________ 。
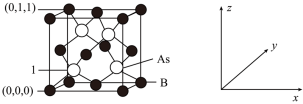
(4)超高热导率半导体材料砷化硼( )的晶胞结构如图所示,则1号砷原子的原子坐标为
)的晶胞结构如图所示,则1号砷原子的原子坐标为_________ 。已知阿伏加德罗常数的值为 ,若晶胞中
,若晶胞中 原子到
原子到 原子最近距离为
原子最近距离为 ,则该晶体的密度为
,则该晶体的密度为_________  (列出含
(列出含 、
、 的计算式即可)。
的计算式即可)。
 ,并获得该化合物的
,并获得该化合物的 器件,该结果有望为白光发射的设计和应用提供新的有效策略。
器件,该结果有望为白光发射的设计和应用提供新的有效策略。(1)已知
 与
与 同族,基态
同族,基态 原子价层电子的运动状态有
原子价层电子的运动状态有 原子的电子排布式不能表示为
原子的电子排布式不能表示为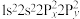 ,因为这违背了
,因为这违背了A.能量最低原理 B.泡利不相容原理 C.洪特规则
(2)
 中硼原子的杂化轨道类型为
中硼原子的杂化轨道类型为 中,
中, 与
与 之间不存在的化学键是
之间不存在的化学键是A.
 键 B.
键 B.  键 C. 配位键 D. 极性键
键 C. 配位键 D. 极性键(3)碳酸钡、碳酸镁分解得到的金属氧化物中,熔点较低的是
(4)超高热导率半导体材料砷化硼(
 )的晶胞结构如图所示,则1号砷原子的原子坐标为
)的晶胞结构如图所示,则1号砷原子的原子坐标为 ,若晶胞中
,若晶胞中 原子到
原子到 原子最近距离为
原子最近距离为 ,则该晶体的密度为
,则该晶体的密度为 (列出含
(列出含 、
、 的计算式即可)。
的计算式即可)。
您最近一年使用:0次
2022-11-13更新
|
434次组卷
|
6卷引用:山西省太原市第五中学2021-2022学年上学期高三第四次模块诊断化学试题
山西省太原市第五中学2021-2022学年上学期高三第四次模块诊断化学试题(已下线)第十一单元 物质结构与性质(B卷 真题滚动练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)(已下线)一轮巩固卷7-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(全国卷专用)广东省广州市广大附中、广外、铁一中学三校2022届高三三模联考化学试题(已下线)化学(全国乙卷单科卷)-学易金卷:2023年高考第一次模拟考试卷福建永春一中、培元中学、季延中学、石光中学2022-2023学年高三上学期期中考联考化学试题
解题方法
7 . 铁、锌、铜等过渡金属元素及其化合物在生产、生活中有着广泛应用。回答下列问题:
(1)基态Cu的核外电子排布式为___________ 。
(2)甘氨酸锌[(H2NCH2COO)2Zn]是 某种饲料添加剂,在该化合物中所涉及到的元素中,第一电离能最大的是______ ; C原子的杂化方式为:___________ 。
(3)Fe3+可与噻吩( )和吡咯(
)和吡咯( )形成配位化合物。试比较二者在水中的溶解度大小:噻吩
)形成配位化合物。试比较二者在水中的溶解度大小:噻吩___________ 吡咯(填“大于 ”或“小于”或“等于”),原因为:_____ 。
(4)硫酸亚铁铵[(NH4)2Fe(SO4)2]俗名摩尔盐,是一种重要的化工原料。固态摩尔盐的晶体类型为___________ ; 的空间构型为
的空间构型为___________ 。
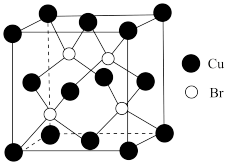
(5)某种铜的溴化物晶体结构如图所示。则该化合物的化学式为___________ ,设晶胞参数为anm,该铜的溴化物晶体的密度为___________ g·m-3。(用含a和NA的式子表示,NA为阿伏加德罗常数)
(1)基态Cu的核外电子排布式为
(2)甘氨酸锌[(H2NCH2COO)2Zn]是 某种饲料添加剂,在该化合物中所涉及到的元素中,第一电离能最大的是
(3)Fe3+可与噻吩(
 )和吡咯(
)和吡咯( )形成配位化合物。试比较二者在水中的溶解度大小:噻吩
)形成配位化合物。试比较二者在水中的溶解度大小:噻吩(4)硫酸亚铁铵[(NH4)2Fe(SO4)2]俗名摩尔盐,是一种重要的化工原料。固态摩尔盐的晶体类型为
 的空间构型为
的空间构型为(5)某种铜的溴化物晶体结构如图所示。则该化合物的化学式为

您最近一年使用:0次
名校
解题方法
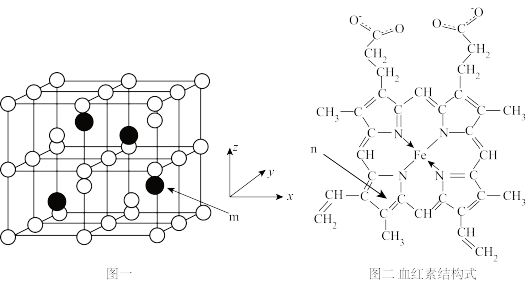
8 . 以物质的量之比3:1的Fe和Al共熔后结晶得Fe3Al晶体,晶胞结构如图一所示,该晶胞为立方晶胞,晶胞参数为a pm。血红素(如图二)是血红蛋白的活性部位,其中心元素是Fe( II)。二者是常见的含铁物质,请回答下列问题。
(1)Fe2+的价电子排布式为:_______ 。
(2)血红素分子中非金属元素电负性由大到小的顺序是_______ (用元素符号表示);这些元素形成的简单氢化物中沸点由高到低的顺序是_______ (用化学式表示);C、N、O三种元素形成一种阴离子CNO-,其结构中有_______ 个σ键,_______ 个π键。
(3)有机分子中的闭环平面结构中,成环原子的π电子数等于4n+2(n=1,2,3 )时,该环具有芳香性。n环为血红素中含N最小环,且为平面结构,则N杂化类型为
)时,该环具有芳香性。n环为血红素中含N最小环,且为平面结构,则N杂化类型为_______ ;该环_______ (填“有”、“无”)芳香性。
(4)Fe3Al晶胞中,rA1=b pm, rFe=c pm,则该晶胞的空间利用率为_______ (以含π的代数式表示)。
(5)m原子的原子分数坐标为_______ . ;晶胞内任意两个A1原子之间的距离为_______ pm。
(6)Fe3Al晶体的密度为_______ g·cm-3。

(1)Fe2+的价电子排布式为:
(2)血红素分子中非金属元素电负性由大到小的顺序是
(3)有机分子中的闭环平面结构中,成环原子的π电子数等于4n+2(n=1,2,3
 )时,该环具有芳香性。n环为血红素中含N最小环,且为平面结构,则N杂化类型为
)时,该环具有芳香性。n环为血红素中含N最小环,且为平面结构,则N杂化类型为(4)Fe3Al晶胞中,rA1=b pm, rFe=c pm,则该晶胞的空间利用率为
(5)m原子的原子分数坐标为
(6)Fe3Al晶体的密度为
您最近一年使用:0次
2022-04-29更新
|
631次组卷
|
3卷引用:江西省九江市2021届高三三模考试化学试题
解题方法
9 . 硫酸亚铁铵是一种蓝绿色的复盐,俗名为摩尔盐,化学式为(NH4)2Fe(SO4)2•6H2O。它在空气中稳定,是重要的化工原料,用途十分广泛。该物质隔绝空气加强热会发生分解,一种分解方式可表示为:(NH4)2Fe(SO4)2•6H2O=2NH3↑+FeO+2SO3↑+7H2O↑。请回答下列问题:
(1)基态铁原子的价电子排布式为___________ ,s电子的电子云形状为___________ 。
(2)摩尔盐中的组成元素N、O的电负性大小顺序是___________ 。
(3)SO2、SO3、SO 是三种常见含硫微粒。
是三种常见含硫微粒。
①SO 微粒的立体构型为
微粒的立体构型为___________ ,SO2中心原子的杂化方式为___________ 。
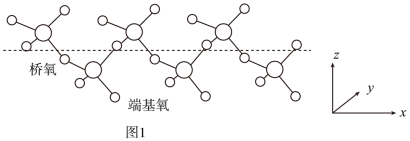
②固态SO3能以无限长链形式存在,结构如图1所示。与硫原子形成化学键更长的是___________ (填“桥氧”或“端基氧”),理由是___________ 。
(4)噻吩( )、吡咯(
)、吡咯(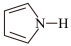 )都可与Fe3+形成配位化合物。在水中的溶解度噻吩
)都可与Fe3+形成配位化合物。在水中的溶解度噻吩___________ 吡咯(填“<”、“>”或“=”),理由是___________ 。
(5)氧化亚铁的一种晶胞与氯化钠晶胞类似,如图2所示。
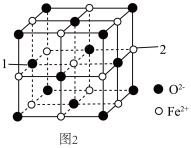
①以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图2中原子1的坐标为(0, ,
, ),则原子2的坐标为
),则原子2的坐标为___________ 。
②Fe2+处于O2﹣围成的___________ 空隙中。(填“正四面体”或“正八面体”)
③该晶体的密度为ρg•cm﹣3,用N0表示阿伏加德罗常数的值,则该晶胞边长为___________ pm。
(1)基态铁原子的价电子排布式为
(2)摩尔盐中的组成元素N、O的电负性大小顺序是
(3)SO2、SO3、SO
 是三种常见含硫微粒。
是三种常见含硫微粒。①SO
 微粒的立体构型为
微粒的立体构型为②固态SO3能以无限长链形式存在,结构如图1所示。与硫原子形成化学键更长的是

(4)噻吩(
 )、吡咯(
)、吡咯( )都可与Fe3+形成配位化合物。在水中的溶解度噻吩
)都可与Fe3+形成配位化合物。在水中的溶解度噻吩(5)氧化亚铁的一种晶胞与氯化钠晶胞类似,如图2所示。

①以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图2中原子1的坐标为(0,
 ,
, ),则原子2的坐标为
),则原子2的坐标为②Fe2+处于O2﹣围成的
③该晶体的密度为ρg•cm﹣3,用N0表示阿伏加德罗常数的值,则该晶胞边长为
您最近一年使用:0次
2022-04-15更新
|
333次组卷
|
2卷引用:新疆维吾尔自治区乌鲁木齐市2021届高三第二次质量检测理综化学试题
10 . 化学家可以通过“自组装”这一有效的工具,利用各种各样的建筑基元米构建复杂的纳米结构。可以预见的是,小型的金属簇能够作为很好的建筑模块用于复杂结构的大体积金属簇的组装。利用高电荷的白磷等电子体[Ge4]4-作为基本建筑单元,过渡金属阳离子Zn2+或Cd2+作为连接节点,成功制备了两个异金属超四面体团簇[M6Ge16]4-(M=Zn2+/Cd2-)。
(1)①基态Zn2+的价电子排布式为____ ,核外有____ 种不同运动状态的电子。
②金属Cd与Zn同族且相邻,则Cd在元素周期表中的位置是____ ,属____ 区元素。Zn和Cd中熔点更高的是____ ,原因是____ 。
(2)①[Ge4]4-中Ge采取____ 杂化,键角为____ 。
②Ge是第IVA族元素,能形成锗烷(GenH2n+2),其结构类似于烷烃。甲锗烷(GeH4)常温下是一种无色、剧毒、可自燃的气体,GeH4和同主族原子序数比它小的元素的简单气态氢化物相比,沸点由高到低的顺序是_____ 。至今没有形成n>5的长链锗烷,请结合键能说明原因_____ 。
(3)Ge是原子晶体,熔点2830℃,与金刚石一样呈现空间网状结构,晶胞如图,则晶体Ge的空间利用率为____ 。(请用含π代数式表示)


(1)①基态Zn2+的价电子排布式为
②金属Cd与Zn同族且相邻,则Cd在元素周期表中的位置是
(2)①[Ge4]4-中Ge采取
②Ge是第IVA族元素,能形成锗烷(GenH2n+2),其结构类似于烷烃。甲锗烷(GeH4)常温下是一种无色、剧毒、可自燃的气体,GeH4和同主族原子序数比它小的元素的简单气态氢化物相比,沸点由高到低的顺序是
| 化学键 | C—C | C—H | Ge—Ge | Ge—H |
| 键能(kJ/mol) | 346 | 411 | 188 | 288 |
(3)Ge是原子晶体,熔点2830℃,与金刚石一样呈现空间网状结构,晶胞如图,则晶体Ge的空间利用率为

您最近一年使用:0次



