名校
解题方法
1 . 钛的化合物如 、
、 、
、 、
、 等均有着广泛用途。
等均有着广泛用途。
(1)写出Ti的基态原子的核外电子排布式:_______ 。
(2) 熔点是-25℃,沸点136.4℃,可溶于苯或
熔点是-25℃,沸点136.4℃,可溶于苯或 ,该晶体属于
,该晶体属于_______ 晶体; 中B原子的杂化类型为
中B原子的杂化类型为_______ 。
(3)在 催化作用下,可将
催化作用下,可将 氧化成
氧化成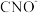 ,进而得到
,进而得到 。与
。与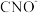 互为等电子体的分子化学式为
互为等电子体的分子化学式为_______ 。
(4) 难溶于水和稀酸,但能溶于浓硫酸,析出含有钛酰离子的晶体,钛酰离子常成为链状聚合形式的阳离子,其结构形式如图1,化学式为
难溶于水和稀酸,但能溶于浓硫酸,析出含有钛酰离子的晶体,钛酰离子常成为链状聚合形式的阳离子,其结构形式如图1,化学式为_______ 。

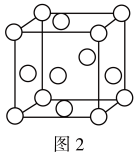
(5)金属钛内部原子的堆积方式是面心立方堆积方式,如图2,若该晶胞的密度为 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则该晶胞的边长为
,则该晶胞的边长为_______ cm。
 、
、 、
、 、
、 等均有着广泛用途。
等均有着广泛用途。(1)写出Ti的基态原子的核外电子排布式:
(2)
 熔点是-25℃,沸点136.4℃,可溶于苯或
熔点是-25℃,沸点136.4℃,可溶于苯或 ,该晶体属于
,该晶体属于 中B原子的杂化类型为
中B原子的杂化类型为(3)在
 催化作用下,可将
催化作用下,可将 氧化成
氧化成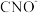 ,进而得到
,进而得到 。与
。与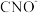 互为等电子体的分子化学式为
互为等电子体的分子化学式为(4)
 难溶于水和稀酸,但能溶于浓硫酸,析出含有钛酰离子的晶体,钛酰离子常成为链状聚合形式的阳离子,其结构形式如图1,化学式为
难溶于水和稀酸,但能溶于浓硫酸,析出含有钛酰离子的晶体,钛酰离子常成为链状聚合形式的阳离子,其结构形式如图1,化学式为
(5)金属钛内部原子的堆积方式是面心立方堆积方式,如图2,若该晶胞的密度为
 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则该晶胞的边长为
,则该晶胞的边长为
您最近一年使用:0次
名校
2 . 铜及其化合物在科学研究和工农业生产中有许多用途。回答下列问题:
(1) 溶液可以吸收合成氨中对催化剂有毒害的CO气体[醋酸根(
溶液可以吸收合成氨中对催化剂有毒害的CO气体[醋酸根( )简写成
)简写成 ],反应的化学方程式为:
],反应的化学方程式为: 。
。
①基态 的核外电子排布式为
的核外电子排布式为___________ 。
② 中C原子的杂化轨道类型为
中C原子的杂化轨道类型为___________ 。
③ 中所含非金属元素的电负性由大到小的顺序是
中所含非金属元素的电负性由大到小的顺序是___________ (用元素符号表示)。
④ 中N原子形成的H—N—H键角
中N原子形成的H—N—H键角___________ (填“大于”“小于”或“等于”)气态 中的键角,原因是
中的键角,原因是___________ 。
⑤1个 中含有的共价键数为
中含有的共价键数为___________ 。
(2)Cu—Mn—Al合金为磁性形状记忆合金材料之一,其晶胞结构如图所示:

①合金的化学式为___________ 。
②若A原子的坐标参数为(0,1,0),则B原子的坐标参数为___________ 。
③已知该合金晶体的边长为a cm,则最近的两个Al原子间的距离为___________ nm
(1)
 溶液可以吸收合成氨中对催化剂有毒害的CO气体[醋酸根(
溶液可以吸收合成氨中对催化剂有毒害的CO气体[醋酸根( )简写成
)简写成 ],反应的化学方程式为:
],反应的化学方程式为: 。
。①基态
 的核外电子排布式为
的核外电子排布式为②
 中C原子的杂化轨道类型为
中C原子的杂化轨道类型为③
 中所含非金属元素的电负性由大到小的顺序是
中所含非金属元素的电负性由大到小的顺序是④
 中N原子形成的H—N—H键角
中N原子形成的H—N—H键角 中的键角,原因是
中的键角,原因是⑤1个
 中含有的共价键数为
中含有的共价键数为(2)Cu—Mn—Al合金为磁性形状记忆合金材料之一,其晶胞结构如图所示:

①合金的化学式为
②若A原子的坐标参数为(0,1,0),则B原子的坐标参数为
③已知该合金晶体的边长为a cm,则最近的两个Al原子间的距离为
您最近一年使用:0次
解题方法
3 . 中国科学院天津工业生物技术研究所马延和研究员带领团队,采用一种类似“搭积木”的方式,在实验室中首次实现从二氧化碳到淀粉分子的全合成,开启了“向空气要面包”的新技术。下列有关说法错误的是
A.合成过程中发生 的转化,其中C原子杂化方式发生了变化 的转化,其中C原子杂化方式发生了变化 |
B.“向空气要面包”还可以指天然固氮(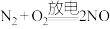 )产生硝态氮肥的过程 )产生硝态氮肥的过程 |
| C.淀粉用途广泛,如制作各种食品、酿酒、检验加碘食盐中的碘单质等 |
D.该技术可以减缓 给环境带来的负担,有利于“碳中和”“碳达峰”的实现 给环境带来的负担,有利于“碳中和”“碳达峰”的实现 |
您最近一年使用:0次
4 . 氮族元素及其化合物种类繁多,有着非常重要的用途,回答下列问题:
(1)基态 原子的电子排布式为
原子的电子排布式为
___________ 。
(2) 和
和 两种分子键角较小的是
两种分子键角较小的是___________ ,原因是:___________ 。
(3) 分子的空间构型为
分子的空间构型为___________ 。
(4) 中三种元素电负性由大到小的顺序为
中三种元素电负性由大到小的顺序为___________ ,N杂化方式是___________ , 的沸点高于
的沸点高于 的原因是
的原因是___________ 。
(5) 的立方晶胞结构如图所示:
的立方晶胞结构如图所示:

若砷化镓晶胞边长为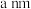 ,则该晶体密度为
,则该晶体密度为___________  (用含
(用含 的代数式表示)。
的代数式表示)。
(1)基态
 原子的电子排布式为
原子的电子排布式为
(2)
 和
和 两种分子键角较小的是
两种分子键角较小的是(3)
 分子的空间构型为
分子的空间构型为(4)
 中三种元素电负性由大到小的顺序为
中三种元素电负性由大到小的顺序为 的沸点高于
的沸点高于 的原因是
的原因是(5)
 的立方晶胞结构如图所示:
的立方晶胞结构如图所示:
若砷化镓晶胞边长为
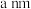 ,则该晶体密度为
,则该晶体密度为 (用含
(用含 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
名校
5 . 一种叠氮桥基配位化合物C在医药工业具有广泛的用途,其合成方法如图,下列叙述正确的是


| A.基态Br原子价电子排布式为3d104s24p5 | B.物质C中氮原子杂化形式有sp2、sp3 |
| C.CH3OH是手性分子 | D.NaN3中N 立体构型为直线形 立体构型为直线形 |
您最近一年使用:0次
2022-11-13更新
|
108次组卷
|
2卷引用:四川省绵阳南山中学2022-2023学年高二上学期期中考试化学试题
名校
解题方法
6 . 铜及其化合物在人们的日常生活中有着广泛的用途,回答下列问题:
(1)基态铜原子的价电子排布式为___________ 。
(2)在气体分析中,常用CuCl的盐酸溶液吸收并定量测定CO的含量,其化学反应如下: 2CuCl+2CO+2H2O= Cu2Cl2·2CO·2H2O,Cu2Cl2·2CO·2H2O是一种配合物。其结构简式如图1所示。

①H2O中氧原子的杂化轨道类型为___________ 。
②该配合物中,CO作配体时配位原子是C而不是O的原因是___________ 。
(3)氧化亚铜的化学式为Cu2O,为一价铜的氧化物,为鲜红色粉末状固体,常用于催化有机物的合成,其立方晶胞如图2所示:

①晶胞中白球Z表示___________ 原子(填名称)
②与O距离相等且最近的O能构成___________ ( 填空间构型)
③体心Z原子的坐标为( ,
, ,
, )。 则P与M两个位置的R原子的坐标分别是
)。 则P与M两个位置的R原子的坐标分别是_____ 、______ 。
(1)基态铜原子的价电子排布式为
(2)在气体分析中,常用CuCl的盐酸溶液吸收并定量测定CO的含量,其化学反应如下: 2CuCl+2CO+2H2O= Cu2Cl2·2CO·2H2O,Cu2Cl2·2CO·2H2O是一种配合物。其结构简式如图1所示。

①H2O中氧原子的杂化轨道类型为
②该配合物中,CO作配体时配位原子是C而不是O的原因是
(3)氧化亚铜的化学式为Cu2O,为一价铜的氧化物,为鲜红色粉末状固体,常用于催化有机物的合成,其立方晶胞如图2所示:

①晶胞中白球Z表示
②与O距离相等且最近的O能构成
③体心Z原子的坐标为(
 ,
, ,
, )。 则P与M两个位置的R原子的坐标分别是
)。 则P与M两个位置的R原子的坐标分别是
您最近一年使用:0次
7 . N、P、As及其化合物在生产生活方面都有重要的用途。回答下列问题:
(1)下列基态氮原子的轨道表示式中,仅违背泡利不相容原理的是_______(填字母)。
(2)氢氧化铜难溶于水,但可溶于浓氨水,得到深蓝色透明溶液。写出反应的离子方程式:_______ ; 在水溶液里,Cu2+比Cu+稳定,是由于水分子配体的作用。在气态时,Cu2+比Cu+活泼的原因是_______ ;
(3)C、N、O三种元素的第五电离能(I5)由大到小顺序是_______ 。
(4)离子液体具有较好的化学稳定性、较低的熔点以及对多种物质有良好的溶解性,因此被广泛应用于有机合成、分离提纯以及电化学研究中。下图为某一离子液体的结构。下列判断不正确的是_______

(5)含砷有机物“对氨基苯胂酸”的结构简式如图,1mol对氨基苯胂酸含σ键数目为_______ 。

(1)下列基态氮原子的轨道表示式中,仅违背泡利不相容原理的是_______(填字母)。
A. | B. |
C. | D. |
(3)C、N、O三种元素的第五电离能(I5)由大到小顺序是
(4)离子液体具有较好的化学稳定性、较低的熔点以及对多种物质有良好的溶解性,因此被广泛应用于有机合成、分离提纯以及电化学研究中。下图为某一离子液体的结构。下列判断不正确的是_______

| A.该离子液体能与水分子形成氢键 |
| B.该结构中不存在手性碳原子 |
| C.该结构中C原子的轨道杂化类型有3种 |
D.BF 中存在配位键,B原子的轨道杂化类型为sp3 中存在配位键,B原子的轨道杂化类型为sp3 |

您最近一年使用:0次
名校
解题方法
8 . 第VA族元素氮、磷、砷的化合物用途广泛。回答下列问题:
(1)实验中常用 检验
检验 ,
, 中
中 的配位数为
的配位数为_______ ,其中碳原子的杂化轨道类型为_______ 杂化。1mol 中含有
中含有 键的数目为
键的数目为_______ 。
(2)铁和氨在640℃可发生置换反应,产物之一的立方晶胞结构如图所示,写出该反应的化学方程式:_______ 。

(3)阿伏加德罗常数的值为 ,X射线衍实验测得该晶胞参数为anm,则晶胞的密度为
,X射线衍实验测得该晶胞参数为anm,则晶胞的密度为_______  (写出表达式即可)。
(写出表达式即可)。
(4)用铬原子代替部分铜原子,可以形成一系列铜—铬合金。其中两种铜—铬合金的晶体结构如图所示。

①晶体a中铬原子的配位数为_______ 。
②晶体b中铬原子填充在由铜原子构成的_______ (填“四面体”“六面体”或“八面体”)空隙中, 表示阿伏加德罗常数的值,铜原子半径为
表示阿伏加德罗常数的值,铜原子半径为 cm,铬原子半径为
cm,铬原子半径为 cm,则晶体b的空间利用率为
cm,则晶体b的空间利用率为_______ 。(写出表达式即可)
(1)实验中常用
 检验
检验 ,
, 中
中 的配位数为
的配位数为 中含有
中含有 键的数目为
键的数目为(2)铁和氨在640℃可发生置换反应,产物之一的立方晶胞结构如图所示,写出该反应的化学方程式:

(3)阿伏加德罗常数的值为
 ,X射线衍实验测得该晶胞参数为anm,则晶胞的密度为
,X射线衍实验测得该晶胞参数为anm,则晶胞的密度为 (写出表达式即可)。
(写出表达式即可)。(4)用铬原子代替部分铜原子,可以形成一系列铜—铬合金。其中两种铜—铬合金的晶体结构如图所示。

①晶体a中铬原子的配位数为
②晶体b中铬原子填充在由铜原子构成的
 表示阿伏加德罗常数的值,铜原子半径为
表示阿伏加德罗常数的值,铜原子半径为 cm,铬原子半径为
cm,铬原子半径为 cm,则晶体b的空间利用率为
cm,则晶体b的空间利用率为
您最近一年使用:0次
名校
解题方法
9 . 锡、铬、钴、铜等金属及其化合物在工业上有重要用途。
(1)锡合金具有优异的抗蚀性能,可以用来生产制作各种精美合金饰品。
①基态Sn原子价层电子排布为_______
②Co元素在元素周期表中的位置是_______
③Cu元素位于元素周期表的_______ 区
(2)制备CrO2Cl2的反应为K2Cr2O7 + 3CCl4 = 2KCl + 2CrO2Cl2 + 3COCl2↑
①上述方程式中非金属元素电负性由小到大的顺序为_______ (用元素符号表示)。
②COCl2分子中π键和σ键的个数比为_______ ,中心原子的杂化方式为_______ ,COCl2属于_______ 分子(填“极性”或“非极性”)。
(3)Cu−Mn−Al合金为磁性形状记忆合金材料之一,其晶胞结构如图所示:
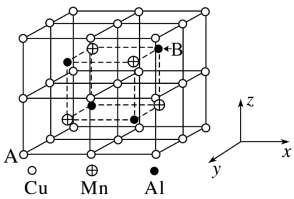
①合金的化学式为_______ 。
②A原子坐标参数为(0,1,0),则B原子坐标参数为_______ 。
③已知该合金晶体密度为ρg·cm-3,则两个Al原子间的最近距离为_______ nm (阿伏加德罗常数用NA表示,只列计算式)。
(1)锡合金具有优异的抗蚀性能,可以用来生产制作各种精美合金饰品。
①基态Sn原子价层电子排布为
②Co元素在元素周期表中的位置是
③Cu元素位于元素周期表的
(2)制备CrO2Cl2的反应为K2Cr2O7 + 3CCl4 = 2KCl + 2CrO2Cl2 + 3COCl2↑
①上述方程式中非金属元素电负性由小到大的顺序为
②COCl2分子中π键和σ键的个数比为
(3)Cu−Mn−Al合金为磁性形状记忆合金材料之一,其晶胞结构如图所示:

①合金的化学式为
②A原子坐标参数为(0,1,0),则B原子坐标参数为
③已知该合金晶体密度为ρg·cm-3,则两个Al原子间的最近距离为
您最近一年使用:0次
2022-05-16更新
|
132次组卷
|
2卷引用:甘肃省兰州第一中学2021-2022学年高二下学期期中考试化学试题
名校
解题方法
10 . 完成下列问题。
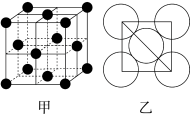
(1)金属铝的晶胞结构如图甲所示,原子之间相互位置关系的平面图如图乙所示。若已知Al的原子半径为rcm,NA代表阿伏加德罗常数的值,该晶体的密度为_______  (用含NA、r的最简式表示)。
(用含NA、r的最简式表示)。
(2)2022年北京冬季奥运会场馆建设使用了大量不锈钢材质,不锈钢属于铁碳合金,常含铬、镍等元素。
①碳的一种单质石墨是单层二维蜂窝状晶格结构的新材料(如图1),其中碳原子采取_______ 杂化,在层中每个碳原子周围等距且紧邻的碳原子个数为_______ 。

②铁合金用途广泛,某种铁镁合金储氢效率很高,其晶胞如图2所示。晶体中每个镁原子周围等距且紧邻的镁原子有_______ 个,该铁镁合金中原子个数比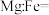
_______ ;原子坐标参数可以表示晶胞内部各原子的相对位置,其中原子坐标参数A为(0,0,0),C为( ,
, ,0),B点坐标参数为
,0),B点坐标参数为_______ 。

(1)金属铝的晶胞结构如图甲所示,原子之间相互位置关系的平面图如图乙所示。若已知Al的原子半径为rcm,NA代表阿伏加德罗常数的值,该晶体的密度为
 (用含NA、r的最简式表示)。
(用含NA、r的最简式表示)。
(2)2022年北京冬季奥运会场馆建设使用了大量不锈钢材质,不锈钢属于铁碳合金,常含铬、镍等元素。
①碳的一种单质石墨是单层二维蜂窝状晶格结构的新材料(如图1),其中碳原子采取

②铁合金用途广泛,某种铁镁合金储氢效率很高,其晶胞如图2所示。晶体中每个镁原子周围等距且紧邻的镁原子有
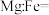
 ,
, ,0),B点坐标参数为
,0),B点坐标参数为
您最近一年使用:0次



