1 . 卤素单质及其化合物在科研和工农业生产中有着广泛的应用。回答下列问题:
(1)氟原子激发态的电子排布式有________ ,其中能量较高的是________ 。(填标号)
A. B.
B. C.
C.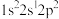 D.
D.
(2)基态Br原子的核外电子排布式为________ 。
(3) 中提供电子对形成配位键的原子是
中提供电子对形成配位键的原子是________ ,中心离子的配位数为________ 。
(4)Kr是第四周期的稀有气体元素,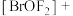 的中心原子Br的杂化轨道类型为
的中心原子Br的杂化轨道类型为________ 。
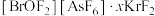 晶体中的微粒间作用力有
晶体中的微粒间作用力有________ (填标号)。
a.氢键 b.离子键 c.极性共价键 d.非极性共价键
(5)固态氟化氢中存在 形式,画出
形式,画出 的链状结构
的链状结构________ 。
(6)四氟乙烯 和聚四氟乙烯中C的杂化轨道类型分别为
和聚四氟乙烯中C的杂化轨道类型分别为________ 和________ ;聚四氟乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因________ 。
(1)氟原子激发态的电子排布式有
A.
 B.
B. C.
C.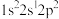 D.
D.
(2)基态Br原子的核外电子排布式为
(3)
 中提供电子对形成配位键的原子是
中提供电子对形成配位键的原子是(4)Kr是第四周期的稀有气体元素,
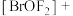 的中心原子Br的杂化轨道类型为
的中心原子Br的杂化轨道类型为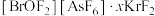 晶体中的微粒间作用力有
晶体中的微粒间作用力有a.氢键 b.离子键 c.极性共价键 d.非极性共价键
(5)固态氟化氢中存在
 形式,画出
形式,画出 的链状结构
的链状结构(6)四氟乙烯
 和聚四氟乙烯中C的杂化轨道类型分别为
和聚四氟乙烯中C的杂化轨道类型分别为
您最近一年使用:0次
2 . NA表示阿伏加德罗常数的值,配合物Na2[Fe(CN)5(NO)]可用于离子检验。下列说法不正确的是
| A.该配合物中存在离子键、配位键、极性键、非极性键 |
| B.配离子为[Fe(CN)5(NO)]2-,中心离子为Fe3+,配位数为6,配位原子为C和N |
| C.1mol该配合物中σ键数目为6NA |
| D.该配合物为离子化合物,易电离,1mol配合物电离共得到3NA个阴、阳离子 |
您最近一年使用:0次
名校
解题方法
3 . 下列离子方程式错误的是
A.向氨水中加入少量氯化银: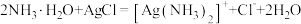 |
B.向明矾溶液中滴加氢氧化钡溶液至沉淀质量最大: |
C.用惰性电极电解硫酸铜溶液: |
D.硝酸铁溶液中通入少量二氧化硫: |
您最近一年使用:0次
名校
4 . 根据下列实验操作和现象,得出的相应结论正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 用铂丝蘸取少量某溶液进行焰色试验 | 有黄色火焰,透过蓝色钴玻璃观察到紫色火焰 | 溶液中含有钠盐和钾盐 |
B | 向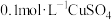 溶液中加入 溶液中加入 固体 固体 | 溶液由蓝色变为黄绿色 | 存在转化: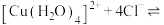 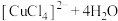 |
C | 向 溶液中滴加稀盐酸溶液 溶液中滴加稀盐酸溶液 | 有白色胶状沉淀 | 非金属性: |
D | 将铁锈溶于浓盐酸,滴入 溶液 溶液 | 紫红色褪去 | 铁锈中含有二价铁 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-05-16更新
|
158次组卷
|
2卷引用:2024届重庆市南开中学校高三下学期5月月考化学试题
名校
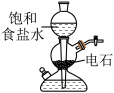
5 . 下列实验装置或操作能够达到实验目的的是
|
|
| A.实验室制乙炔 | B.验证羟基活化苯环 |
|
|
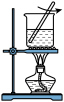
C.验证牺牲 保护 保护 | D.制备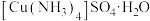 晶体 晶体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-05-16更新
|
184次组卷
|
2卷引用:2024届重庆市南开中学校高三下学期5月月考化学试题
解题方法
6 . 连二亚硫酸钠( )俗称保险粉,可用作造纸工业中的漂白剂,将部分有色物质还原为无色物质,提高纸浆白度。已知亚硫酸的结构式为
)俗称保险粉,可用作造纸工业中的漂白剂,将部分有色物质还原为无色物质,提高纸浆白度。已知亚硫酸的结构式为 ,实验室利用如下流程进行制备:
,实验室利用如下流程进行制备: ,装置如图所示。下列说法错误的是
,装置如图所示。下列说法错误的是

A.实验室利用亚硫酸钠制备 时,应选择70%的浓硫酸 时,应选择70%的浓硫酸 |
| B.单向阀的作用是只让气体通过并防倒吸 |
C.加入的NaOH不宜过多,防止生成难以分离的 |
D.尾气可用 溶液处理 溶液处理 |
您最近一年使用:0次
7 . 实验室以废铜屑(含少量Fe、不溶性杂质)为原料制取 晶体和
晶体和 晶体,其实验流程如下:
晶体,其实验流程如下:
(1)基态Cu原子核外电子排布式为______ 。
(2) 中,中心离子为
中,中心离子为_____ ,其配位数为_____ ,配体是_____ 。
(3) 中,存在的化学键有
中,存在的化学键有______ (填字母)。
a.离子键 b.非极性共价键 c.极性共价键 d.配位键 e.氢键
(4)“氧化”时,在如图所示的装置中进行。从长导管中通入氧气的作用是_______ 。保持试剂的用量不变,实验中提高反应速率的操作有______ (写一种)。该步骤首先加入一定量 的
的 溶液,再调节浓
溶液,再调节浓 的用量至
的用量至 为2.0左右时,铜粉和浓
为2.0左右时,铜粉和浓 完全反应,主要反应的化学方程式为
完全反应,主要反应的化学方程式为_______ 。硝酸过量对产品的影响为______ 。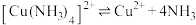 ;
; 、
、 难溶于乙醇。结合下图,
难溶于乙醇。结合下图, 在乙醇—水混合液中的溶解度随乙醇体积分数变化曲线,将加入足量氨水后所得的
在乙醇—水混合液中的溶解度随乙醇体积分数变化曲线,将加入足量氨水后所得的 溶液制备
溶液制备 晶体的实验方案补充完整:将
晶体的实验方案补充完整:将 溶液加入
溶液加入______ ,所得沉淀先用乙醇—水混合液洗涤,向最后的洗涤滤液中滴加_______ (填试剂)无沉淀生成,再将晶体用无水乙醇洗涤,放入真空干燥箱中干燥。
 晶体和
晶体和 晶体,其实验流程如下:
晶体,其实验流程如下: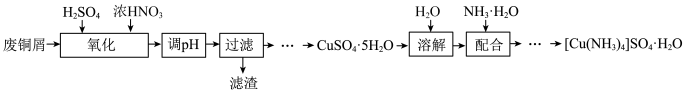
(1)基态Cu原子核外电子排布式为
(2)
 中,中心离子为
中,中心离子为(3)
 中,存在的化学键有
中,存在的化学键有a.离子键 b.非极性共价键 c.极性共价键 d.配位键 e.氢键
(4)“氧化”时,在如图所示的装置中进行。从长导管中通入氧气的作用是
 的
的 溶液,再调节浓
溶液,再调节浓 的用量至
的用量至 为2.0左右时,铜粉和浓
为2.0左右时,铜粉和浓 完全反应,主要反应的化学方程式为
完全反应,主要反应的化学方程式为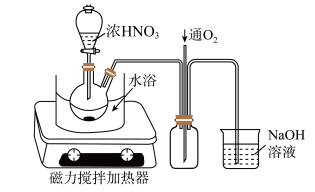
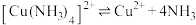 ;
; 、
、 难溶于乙醇。结合下图,
难溶于乙醇。结合下图, 在乙醇—水混合液中的溶解度随乙醇体积分数变化曲线,将加入足量氨水后所得的
在乙醇—水混合液中的溶解度随乙醇体积分数变化曲线,将加入足量氨水后所得的 溶液制备
溶液制备 晶体的实验方案补充完整:将
晶体的实验方案补充完整:将 溶液加入
溶液加入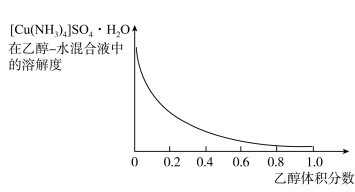
您最近一年使用:0次
解题方法
8 . 原子序数依次增大的前四周期元素X、Y、Z、W中,X和Y的价电子层中未成对电子均只有1个,并且 和
和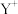 的电子数相差8;与Y位于同一周期的Z和W,它们的价电子层中的未成对电子数分别为4和2,且原子序数相差2。回答下列问题:
的电子数相差8;与Y位于同一周期的Z和W,它们的价电子层中的未成对电子数分别为4和2,且原子序数相差2。回答下列问题:
(1)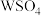 溶于氨水形成
溶于氨水形成 蓝色溶液。
蓝色溶液。
① 中
中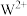 与
与 之间形成的化学键称为
之间形成的化学键称为______ ,提供孤电子对的成键原子是______ (填元素符号)。
②氨气溶于水时,大部分 与
与 以氢键(用“…”表示)结合形成
以氢键(用“…”表示)结合形成 分子。根据氨水的性质可推知
分子。根据氨水的性质可推知 的结构式为
的结构式为______ 。
③往 蓝色溶液中滴入少量氢氧化钡溶液,该反应的离子方程式为
蓝色溶液中滴入少量氢氧化钡溶液,该反应的离子方程式为____________ 。
(2) 中的化学键只有明显的共价性,蒸气状态下以双聚分子形式存在的
中的化学键只有明显的共价性,蒸气状态下以双聚分子形式存在的 的结构式为
的结构式为______ ,其中Z的配位数为______ 。
(3)反应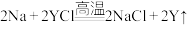 能够发生的原因为
能够发生的原因为____________ 。
 和
和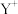 的电子数相差8;与Y位于同一周期的Z和W,它们的价电子层中的未成对电子数分别为4和2,且原子序数相差2。回答下列问题:
的电子数相差8;与Y位于同一周期的Z和W,它们的价电子层中的未成对电子数分别为4和2,且原子序数相差2。回答下列问题:(1)
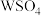 溶于氨水形成
溶于氨水形成 蓝色溶液。
蓝色溶液。①
 中
中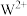 与
与 之间形成的化学键称为
之间形成的化学键称为②氨气溶于水时,大部分
 与
与 以氢键(用“…”表示)结合形成
以氢键(用“…”表示)结合形成 分子。根据氨水的性质可推知
分子。根据氨水的性质可推知 的结构式为
的结构式为③往
 蓝色溶液中滴入少量氢氧化钡溶液,该反应的离子方程式为
蓝色溶液中滴入少量氢氧化钡溶液,该反应的离子方程式为(2)
 中的化学键只有明显的共价性,蒸气状态下以双聚分子形式存在的
中的化学键只有明显的共价性,蒸气状态下以双聚分子形式存在的 的结构式为
的结构式为(3)反应
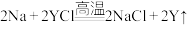 能够发生的原因为
能够发生的原因为
您最近一年使用:0次
9 . 氯化亚铜可用作有机合成的催化剂。以黄铜矿(主要成分为 ,还含杂质
,还含杂质 )为主要原料制备
)为主要原料制备 的流程如下。已知:
的流程如下。已知: 可以溶解在氯离子浓度较大的溶液中,生成
可以溶解在氯离子浓度较大的溶液中,生成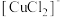 ,
,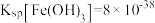 ,
,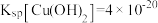 ,
, 。
。___________ (填“大于”或“小于”)锌的第二电离能,其主要原因是___________ 。
(2)“滤渣1”的主要成分为___________ 。
(3)用 溶液调节溶液的
溶液调节溶液的 的值应大于
的值应大于___________ 。
(4)“还原”过程中发生的主要反应的离子方程式为___________ ;该过程中若 的用量过多,造成的后果是
的用量过多,造成的后果是___________ 。
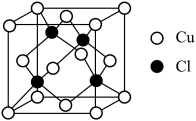
(5)氯化亚铜的立方晶胞如图所示,已知其密度为 ,
, 为阿伏加德罗常数的值,晶胞中
为阿伏加德罗常数的值,晶胞中 的配位数为
的配位数为___________ ,该晶胞参数为___________  。
。
 ,还含杂质
,还含杂质 )为主要原料制备
)为主要原料制备 的流程如下。已知:
的流程如下。已知: 可以溶解在氯离子浓度较大的溶液中,生成
可以溶解在氯离子浓度较大的溶液中,生成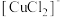 ,
,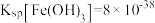 ,
,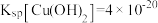 ,
, 。
。
(2)“滤渣1”的主要成分为
(3)用
 溶液调节溶液的
溶液调节溶液的 的值应大于
的值应大于(4)“还原”过程中发生的主要反应的离子方程式为
 的用量过多,造成的后果是
的用量过多,造成的后果是(5)氯化亚铜的立方晶胞如图所示,已知其密度为
 ,
, 为阿伏加德罗常数的值,晶胞中
为阿伏加德罗常数的值,晶胞中 的配位数为
的配位数为 。
。
您最近一年使用:0次
10 .  是一系列化合物,向含
是一系列化合物,向含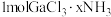 的溶液中加入足量
的溶液中加入足量 溶液,有难溶于硝酸的白色沉淀生成;过滤后,充分加热滤液,有4mol氨气逸出,且又有上述沉淀生成,两次沉淀的物质的量之比为1∶2,能准确表示
溶液,有难溶于硝酸的白色沉淀生成;过滤后,充分加热滤液,有4mol氨气逸出,且又有上述沉淀生成,两次沉淀的物质的量之比为1∶2,能准确表示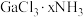 结构的化学式为
结构的化学式为_______ 。
 是一系列化合物,向含
是一系列化合物,向含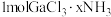 的溶液中加入足量
的溶液中加入足量 溶液,有难溶于硝酸的白色沉淀生成;过滤后,充分加热滤液,有4mol氨气逸出,且又有上述沉淀生成,两次沉淀的物质的量之比为1∶2,能准确表示
溶液,有难溶于硝酸的白色沉淀生成;过滤后,充分加热滤液,有4mol氨气逸出,且又有上述沉淀生成,两次沉淀的物质的量之比为1∶2,能准确表示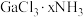 结构的化学式为
结构的化学式为
您最近一年使用:0次