1 . 工业上用Cu(NH3)4SO4和氨水的混合液浸取废铜矿渣中的单质铜,得到[Cu(NH3)2]2SO4。某小组同学欲通过实验探究其原理。
【查阅资料】
i.Cu(NH3)42+呈深蓝色,[Cu(NH3)4]2+ Cu2++4NH3;受热易分解,放出氨气。
Cu2++4NH3;受热易分解,放出氨气。
ii.Cu+在水溶液中不稳定,在溶液中只能以[Cu(NH3)2]+等络合离子的形式稳定存在;[Cu(NH3)2]+无色,易被氧气氧化为[Cu(NH3)4]2+。
【实验1】制备Cu(NH3)4SO4
向盛有2mL0.1mol•L-1CuSO4溶液的试管中滴加2mL1mol•L-1氨水,观察到溶液中立即出现浅蓝色沉淀;随后沉淀逐渐溶解,得到深蓝色溶液,经分离得到Cu(NH3)4SO4晶体。
(1)资料表明,向CuSO4溶液中滴加氨水,可能会生成浅蓝色Cu2(OH)2SO4沉淀。
①该小组同学取实验1中浅蓝色沉淀,洗涤后,_______ (补全实验操作和现象),证明沉淀中含有SO 。
。
②补全实验1中生成Cu2(OH)2SO4沉淀的离子方程式:2Cu2++_______ +SO =Cu2(OH)2SO4↓+
=Cu2(OH)2SO4↓+_______ 。
(2)甲同学设计实验证明深蓝色溶液中含Cu(NH3)4SO4;加热深蓝色溶液并检验逸出气体为氨气。你认为此方案_______ (填“可行”或“不可行”),理由是______ 。
【实验2】探究用Cu(NH3)4SO4和氨水的混合液浸取单质铜得到[Cu(NH3)2]2SO4的原理。
已知:其他条件相同时,参与原电池反应的氧化剂(或还原剂)的氧化性(或还原性)越强,检测到的电压越大。
(3)溶液A为_______ 。
(4)对比实验2-1和2-2,可以得到的结论是_______ 。
(5)实验2~4中,甲烧杯中溶液由无色变为蓝色的原因是______ 。
(6)结合上述实验分析,用Cu(NH3)4SO4和氨水的混合液浸取单质铜的过程中,Cu(NH3)4SO4和氨水的作用分别是:______ 。
【查阅资料】
i.Cu(NH3)42+呈深蓝色,[Cu(NH3)4]2+
 Cu2++4NH3;受热易分解,放出氨气。
Cu2++4NH3;受热易分解,放出氨气。ii.Cu+在水溶液中不稳定,在溶液中只能以[Cu(NH3)2]+等络合离子的形式稳定存在;[Cu(NH3)2]+无色,易被氧气氧化为[Cu(NH3)4]2+。
【实验1】制备Cu(NH3)4SO4
向盛有2mL0.1mol•L-1CuSO4溶液的试管中滴加2mL1mol•L-1氨水,观察到溶液中立即出现浅蓝色沉淀;随后沉淀逐渐溶解,得到深蓝色溶液,经分离得到Cu(NH3)4SO4晶体。
(1)资料表明,向CuSO4溶液中滴加氨水,可能会生成浅蓝色Cu2(OH)2SO4沉淀。
①该小组同学取实验1中浅蓝色沉淀,洗涤后,
 。
。②补全实验1中生成Cu2(OH)2SO4沉淀的离子方程式:2Cu2++
 =Cu2(OH)2SO4↓+
=Cu2(OH)2SO4↓+(2)甲同学设计实验证明深蓝色溶液中含Cu(NH3)4SO4;加热深蓝色溶液并检验逸出气体为氨气。你认为此方案
【实验2】探究用Cu(NH3)4SO4和氨水的混合液浸取单质铜得到[Cu(NH3)2]2SO4的原理。
| 编号 | 实验装置及部分操作 | 烧杯中溶液 | 实验现象 |
| 2-1 | 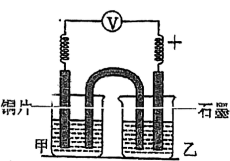 实验开始,先读取电压表示数,后迅速将其换成电流表,继续实验,10min内记录甲烧杯中的现象 | 甲:0.05mol•L-1Na2SO4 乙:0.05mol•L-1Cu(NH3)4SO4 | 电压表指针迅速偏转至0.1V;甲中溶液无明显变化 |
| 2-2 | 甲:0.05mol•L-1Na2SO4 乙:0.05mol•L-1CuSO4 | 电压表指针迅速偏转至0.3V;甲中溶液无明显变化 | |
| 2-3 | 甲:0.1mol•L-1Na2SO4与1mol•L-1氨水等体积混合 乙:溶液A | 电压表指针迅速偏转至0.35V;甲中溶液无明显变化 | |
| 2-4 | 甲:0.1mol•L-1Na2SO4与1mol•L-1氨水等体积混合 乙:0.05mol•L-1CuSO4 | 电压表指针迅速偏转至0.65V;几分钟后,甲烧杯中溶液逐渐由无色变蓝色 |
(3)溶液A为
(4)对比实验2-1和2-2,可以得到的结论是
(5)实验2~4中,甲烧杯中溶液由无色变为蓝色的原因是
(6)结合上述实验分析,用Cu(NH3)4SO4和氨水的混合液浸取单质铜的过程中,Cu(NH3)4SO4和氨水的作用分别是:
您最近一年使用:0次
名校
解题方法
2 . 由下列实验方案、现象得出的结论正确的是
| 实验方案 | 现象 | 结论 | |
| A | 向溴水中加入植物油,振荡后静置 | 水层颜色变浅 | 植物油可用于萃取溴水中的溴 |
| B | 向 溶液中加入乙醇 溶液中加入乙醇 | 析出深蓝色固体 |  在乙醇中溶解度小 在乙醇中溶解度小 |
| C | 用毛皮摩擦过的带电橡胶靠近CF2Cl2液流 | 液流方向改变 | CF2Cl2为四面体结构 |
| D | 将氯气通入盛有鲜花的集气瓶中 | 鲜花褪色 | 氯气具有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-29更新
|
571次组卷
|
2卷引用:山西省晋城市第一中学校2023-2024学年高三下学期开学考试理综化学试题
名校
解题方法
3 . 下列对有关事实的解释不正确的是
| 选项 | 事实 | 解释 |
| A | 水的沸点比硫化氢的沸点高 | 水分子间形成氢键 |
| B | 在CS2中的溶解度:CCl4>H2O | CS2、CCl4为非极性分子,而H2O为极性分子 |
| C | 用质谱仪检测乙酸时,谱图出现了质荷比为120的峰 | 两个乙酸分子通过范德华力形成了二聚体 |
| D | 稳定性:[Cu(H2O)4]2+<[Cu(NH3)4]2+ | N的电负性小于O的电负性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-19更新
|
308次组卷
|
3卷引用:黑龙江省大庆铁人中学2023-2024学年高二下学期开学考试化学试题
解题方法
4 . 硫酸四氨合铜晶体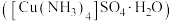 常用作杀虫剂、媒染剂。该物质为深蓝色固体,受热易失氨,常温下在空气中易与水和
常用作杀虫剂、媒染剂。该物质为深蓝色固体,受热易失氨,常温下在空气中易与水和 反应生成铜的碱式盐,变成绿色粉末。某学习小组在实验室中用如图的装置制备硫酸四氨合铜晶体并测定其纯度,请回答下列问题:
反应生成铜的碱式盐,变成绿色粉末。某学习小组在实验室中用如图的装置制备硫酸四氨合铜晶体并测定其纯度,请回答下列问题:
一、硫酸四氨合铜的制备
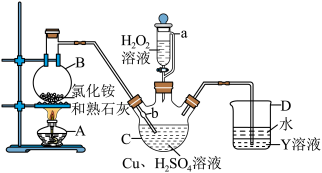
(1)仪器 的名称是
的名称是_____________ ;球泡 的作用是
的作用是_____________ ; 中的
中的 液体可以为
液体可以为_________ (填化学式)。
(2)装置 中得到深蓝色溶液的总反应的离子方程式为
中得到深蓝色溶液的总反应的离子方程式为______________________ 。
(3)反应后取下仪器甲,向其中缓缓加入 乙醇、抽滤、洗涤得到
乙醇、抽滤、洗涤得到 晶体,采用抽滤的原因是
晶体,采用抽滤的原因是______________________ 。
二、测定制备样品中氨的含量
步骤:按如图所示装置进行实验(药品及用量已标出;加热、夹持等装置已略去;硼酸极弱,仅作吸收剂,不影响盐酸标定氨的实验结果),维持沸腾一小时,取下锥形瓶,加入指示剂进行滴定操作,到达滴定终点时,消耗 的盐酸溶液
的盐酸溶液 。
。
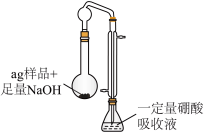
(4)指示剂为_____________ 。
(5)该晶体的纯度为_____________________  。
。
(6)下列实验操作可能使氨含量测定结果偏低的原因是 。
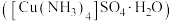 常用作杀虫剂、媒染剂。该物质为深蓝色固体,受热易失氨,常温下在空气中易与水和
常用作杀虫剂、媒染剂。该物质为深蓝色固体,受热易失氨,常温下在空气中易与水和 反应生成铜的碱式盐,变成绿色粉末。某学习小组在实验室中用如图的装置制备硫酸四氨合铜晶体并测定其纯度,请回答下列问题:
反应生成铜的碱式盐,变成绿色粉末。某学习小组在实验室中用如图的装置制备硫酸四氨合铜晶体并测定其纯度,请回答下列问题:一、硫酸四氨合铜的制备

(1)仪器
 的名称是
的名称是 的作用是
的作用是 中的
中的 液体可以为
液体可以为(2)装置
 中得到深蓝色溶液的总反应的离子方程式为
中得到深蓝色溶液的总反应的离子方程式为(3)反应后取下仪器甲,向其中缓缓加入
 乙醇、抽滤、洗涤得到
乙醇、抽滤、洗涤得到 晶体,采用抽滤的原因是
晶体,采用抽滤的原因是二、测定制备样品中氨的含量
步骤:按如图所示装置进行实验(药品及用量已标出;加热、夹持等装置已略去;硼酸极弱,仅作吸收剂,不影响盐酸标定氨的实验结果),维持沸腾一小时,取下锥形瓶,加入指示剂进行滴定操作,到达滴定终点时,消耗
 的盐酸溶液
的盐酸溶液 。
。
(4)指示剂为
(5)该晶体的纯度为
 。
。(6)下列实验操作可能使氨含量测定结果偏低的原因是 。
A.滴定时未用 标准溶液润洗滴定管 标准溶液润洗滴定管 | B.滴定前滴定管内无气泡,滴定后有气泡 |
| C.读数时,滴定前俯视,滴定后仰视 | D.刚看到指示剂局部的颜色变化就停止滴定 |
您最近一年使用:0次
名校
5 . 锌及锌合金(如黄铜)广泛应用于生产、生活。某小组拟以锌矿(主要成分是ZnS,含少量FeS等杂质)为原料采用多种方法冶炼锌,流程如图。回答下列问题:

已知:① 是两性氢氧化物,易溶于NaOH溶液,也溶于氨水,能发生反应:
是两性氢氧化物,易溶于NaOH溶液,也溶于氨水,能发生反应: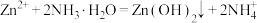 、
、
②常温下,几种金属离子转化成氢氧化物沉淀的pH如表:
(1)已知 中
中 采用
采用 杂化,则
杂化,则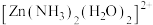 有
有___________ 种结构。
(2)明代宋应星著的《天工开物》中有关“升炼倭铅”的记载:“每炉甘石十斤,装载入一泥罐内,封裹泥固,……然后,逐层用煤炭饼垫盛,其底铺薪,发火煅红……冷定,毁罐取出。……即倭铅也。”(炉甘石主要成分是 ,倭铅即指Zn)古代炼锌方法类似于上述三种方法中的
,倭铅即指Zn)古代炼锌方法类似于上述三种方法中的___________ (填标号,下同)。从环保的角度来看,这三种方法中,最佳方法是___________ 。
a.半湿法 b.火法 c.全湿法
(3)“氧压酸浸”是在稀硫酸中加入锌矿粉,并在加压下通入 ,除生成
,除生成 外,还能回收非金属单质。ZnS参与反应的离子方程式为
外,还能回收非金属单质。ZnS参与反应的离子方程式为___________ 。
(4)“氧化,调pH”时试剂A不宜选择NaOH溶液,也不宜选择氨水,原因是___________ 。
(5)“电解沉积”(以惰性材料为电极)时阳极的电极反应式为___________ 。航母外壳常镶嵌一些锌块,这种保护航母的方法叫___________ 。
(6)通常认为离子浓度 时表示该离子已完全除尽。根据表格数据计算
时表示该离子已完全除尽。根据表格数据计算
___________ 。

已知:①
 是两性氢氧化物,易溶于NaOH溶液,也溶于氨水,能发生反应:
是两性氢氧化物,易溶于NaOH溶液,也溶于氨水,能发生反应: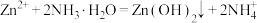 、
、
②常温下,几种金属离子转化成氢氧化物沉淀的pH如表:
| 金属离子 | 开始沉淀的pH | 完全沉淀的pH |
 | 6.5 | 9.7 |
 | 5.4 | 8.0 |
 | 2.3 | 4.1 |
 中
中 采用
采用 杂化,则
杂化,则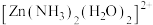 有
有(2)明代宋应星著的《天工开物》中有关“升炼倭铅”的记载:“每炉甘石十斤,装载入一泥罐内,封裹泥固,……然后,逐层用煤炭饼垫盛,其底铺薪,发火煅红……冷定,毁罐取出。……即倭铅也。”(炉甘石主要成分是
 ,倭铅即指Zn)古代炼锌方法类似于上述三种方法中的
,倭铅即指Zn)古代炼锌方法类似于上述三种方法中的a.半湿法 b.火法 c.全湿法
(3)“氧压酸浸”是在稀硫酸中加入锌矿粉,并在加压下通入
 ,除生成
,除生成 外,还能回收非金属单质。ZnS参与反应的离子方程式为
外,还能回收非金属单质。ZnS参与反应的离子方程式为(4)“氧化,调pH”时试剂A不宜选择NaOH溶液,也不宜选择氨水,原因是
(5)“电解沉积”(以惰性材料为电极)时阳极的电极反应式为
(6)通常认为离子浓度
 时表示该离子已完全除尽。根据表格数据计算
时表示该离子已完全除尽。根据表格数据计算
您最近一年使用:0次
名校
6 . 利用如下流程可从废光盘中回收金属层中的银(金属层中其他金属含量过低,对实验影响可忽略): 。下列说法正确的是
。下列说法正确的是

 。下列说法正确的是
。下列说法正确的是| A.若省略第一次过滤,会使氨水的用量增加 |
B.“氧化”时,发生的化学方程式: |
C.若“还原”工序利用原电池来实现,则 是正极产物 是正极产物 |
D.“还原”时,每生成1molAg,理论上消耗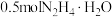 |
您最近一年使用:0次
2024-03-04更新
|
524次组卷
|
2卷引用:江苏省扬州中学2023-2024学年高三下学期阶段练习化学试题
名校
解题方法
7 . 邻二氮菲(phen)与 生成稳定的橙红色邻二氮菲亚铁离子
生成稳定的橙红色邻二氮菲亚铁离子 ,可用于
,可用于 的测定,邻二氮菲的结构简式如图所示。下列说法错误的是
的测定,邻二氮菲的结构简式如图所示。下列说法错误的是

 生成稳定的橙红色邻二氮菲亚铁离子
生成稳定的橙红色邻二氮菲亚铁离子 ,可用于
,可用于 的测定,邻二氮菲的结构简式如图所示。下列说法错误的是
的测定,邻二氮菲的结构简式如图所示。下列说法错误的是
| A.邻二氮菲的一氯代物有4种 | B. 中 中 的配位数为6 的配位数为6 |
| C.邻二氮菲分子不具有旋光性 | D.用邻二氮菲测定 的浓度与溶液的酸碱性无关 的浓度与溶液的酸碱性无关 |
您最近一年使用:0次
名校
解题方法
8 . 湖南大学课题组研究钴催化腈与胺电氢化的反应机理如下图所示(其中 表示苯基,
表示苯基, 表示
表示 ),下列说法错误的是
),下列说法错误的是

A.该反应的催化剂为 和 和 |
B. 中所有碳原子可能共平面 中所有碳原子可能共平面 |
C.所涉及 的配合物中, 的配合物中, 的配位数不同, 的配位数不同, 的杂化方式完全相同 的杂化方式完全相同 |
D.该反应的总方程式为Ph—≡N+PhNH2+4H++4e—  +NH3 +NH3 |
您最近一年使用:0次
9 . 用试管可以完成很多有趣的化学实验。下列说法不正确的是

A.①中出现的蓝色沉淀为 | B.②中生成了配位化合物 |
| C.③中出现的沉淀与①中不同 | D.⑤中发生了氧化还原反应 |
您最近一年使用:0次
2024-02-24更新
|
553次组卷
|
5卷引用:广东省东莞中学、广州二中、惠州一中等六校联考2023-2024学年高三下学期(第六次)开学化学试题
名校
解题方法
10 .  是一种易溶于热水,难溶于乙醇的紫红色晶体。可通过如下实验步骤制备。
是一种易溶于热水,难溶于乙醇的紫红色晶体。可通过如下实验步骤制备。
Ⅰ.将适量氯化铵溶于浓氨水中,搅拌下,分批次加入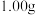 研细的
研细的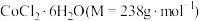 ,得到
,得到 沉淀。
沉淀。
Ⅱ.边搅拌边慢慢滴入足量 溶液,得到
溶液,得到 溶液。
溶液。
Ⅲ.慢慢注入适量浓盐酸,得到沉淀,水浴加热,冷却至室温,得到紫红色晶体,减压过滤。
Ⅳ.依次用不同试剂洗涤晶体,烘干,得到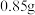 产品。
产品。
回答下列问题:
(1)本实验涉及钴配合物的配体有_______ (填化学式)。
(2)本实验应在通风橱中进行,原因是_______ 。
(3)步骤Ⅰ中分批次加入研细的 ,原因是
,原因是_______ 。
(4)步骤Ⅱ发生反应的离子方程式是_______ 。
(5)步骤Ⅳ中使用的洗涤试剂有:①冷水 ②乙醇 ③冷的盐酸 ④丙酮。试剂使用的先后顺序是:①
_______  ④(填序号)。
④(填序号)。
(6)已知: ;
; 。则在水溶液中的稳定性:
。则在水溶液中的稳定性:
_______  (填“大于”或“小于”)。
(填“大于”或“小于”)。
(7)本实验的产率最接近于_______(填标号)。
 是一种易溶于热水,难溶于乙醇的紫红色晶体。可通过如下实验步骤制备。
是一种易溶于热水,难溶于乙醇的紫红色晶体。可通过如下实验步骤制备。Ⅰ.将适量氯化铵溶于浓氨水中,搅拌下,分批次加入
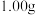 研细的
研细的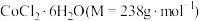 ,得到
,得到 沉淀。
沉淀。Ⅱ.边搅拌边慢慢滴入足量
 溶液,得到
溶液,得到 溶液。
溶液。Ⅲ.慢慢注入适量浓盐酸,得到沉淀,水浴加热,冷却至室温,得到紫红色晶体,减压过滤。
Ⅳ.依次用不同试剂洗涤晶体,烘干,得到
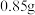 产品。
产品。回答下列问题:
(1)本实验涉及钴配合物的配体有
(2)本实验应在通风橱中进行,原因是
(3)步骤Ⅰ中分批次加入研细的
 ,原因是
,原因是(4)步骤Ⅱ发生反应的离子方程式是
(5)步骤Ⅳ中使用的洗涤试剂有:①冷水 ②乙醇 ③冷的盐酸 ④丙酮。试剂使用的先后顺序是:①

 ④(填序号)。
④(填序号)。(6)已知:
 ;
; 。则在水溶液中的稳定性:
。则在水溶液中的稳定性:
 (填“大于”或“小于”)。
(填“大于”或“小于”)。(7)本实验的产率最接近于_______(填标号)。
A. | B. | C. | D. |
您最近一年使用:0次
2024-01-22更新
|
901次组卷
|
5卷引用:黑龙江省大庆市大庆中学2023-2024学年高三下学期开学化学试题
黑龙江省大庆市大庆中学2023-2024学年高三下学期开学化学试题2024年1月安徽普通高等学校招生考试适应性测试化学试题(已下线)T15-实验探究题(已下线)2024年1月“九省联考”安徽真题完全解读与考后提升(已下线)专题09 化学实验综合题-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)



