1 . 硫代硫酸盐是一类具有应用前景的浸金试剂,硫代硫酸根( )可看作是
)可看作是 中的一个O原子被S原子取代的产物,浸金时
中的一个O原子被S原子取代的产物,浸金时 与
与 配位形成
配位形成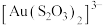 。
。 的晶胞形状为长方体,结构如图所示,下列说法正确的是(
的晶胞形状为长方体,结构如图所示,下列说法正确的是( 表示阿伏伽德罗常数的值)
表示阿伏伽德罗常数的值)
 )可看作是
)可看作是 中的一个O原子被S原子取代的产物,浸金时
中的一个O原子被S原子取代的产物,浸金时 与
与 配位形成
配位形成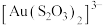 。
。 的晶胞形状为长方体,结构如图所示,下列说法正确的是(
的晶胞形状为长方体,结构如图所示,下列说法正确的是( 表示阿伏伽德罗常数的值)
表示阿伏伽德罗常数的值)
A. 中 中 键数目为12 键数目为12 |
B.晶胞中 的配位数(紧邻的阳离子数)为6 的配位数(紧邻的阳离子数)为6 |
C.与 配位时, 配位时, 中心S原子可作配位原子 中心S原子可作配位原子 |
D. 晶体的密度为: 晶体的密度为: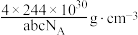 |
您最近一年使用:0次
名校
2 . 电石(CaC2)与水反应生成乙炔,将乙炔通入 溶液中生成Cu2Cl2红棕色沉淀,下列说法正确的是
溶液中生成Cu2Cl2红棕色沉淀,下列说法正确的是
 溶液中生成Cu2Cl2红棕色沉淀,下列说法正确的是
溶液中生成Cu2Cl2红棕色沉淀,下列说法正确的是| A.Cu是第四周期第VIIB族元素 |
B.0.1 mol  中,所含的 中,所含的 键总物质的量为0.2 mol 键总物质的量为0.2 mol |
C.CaC2的电子式可表示为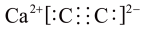 |
D.常温下,将100 mL  的 的 溶液加入足量的NaOH溶液中,可得到448 mL NH3 溶液加入足量的NaOH溶液中,可得到448 mL NH3 |
您最近一年使用:0次
名校
3 . 我国将力争在2030年前实现碳达峰,2060年前实现碳中和的目标,因此二氧化碳的固定以及转化将成为重要的研究课题。
I.在 催化下CO2和H2反应生成甲醇:
催化下CO2和H2反应生成甲醇: 。
。
II.新型 水介质电池放电时,温室气体CO2被转化为储氢物质HCOOH。
水介质电池放电时,温室气体CO2被转化为储氢物质HCOOH。
请回答下列问题:
(1)I中涉及的CO2、H2、CH3OH、H2O,属于非极性分子的是___________ ,基态O原子核外有___________ 种不同空间运动状态的电子。
(2)HCOOH分子中σ键和π键数目之比为___________ 。
(3)反应 中,碳原子的杂化方式由
中,碳原子的杂化方式由___________ 转变为___________ 。CH3OH的沸点高于CH3SH,原因是___________ 。
(4)一种铜的配合物为 ,其配体为
,其配体为___________ 。
I.在
 催化下CO2和H2反应生成甲醇:
催化下CO2和H2反应生成甲醇: 。
。II.新型
 水介质电池放电时,温室气体CO2被转化为储氢物质HCOOH。
水介质电池放电时,温室气体CO2被转化为储氢物质HCOOH。请回答下列问题:
(1)I中涉及的CO2、H2、CH3OH、H2O,属于非极性分子的是
(2)HCOOH分子中σ键和π键数目之比为
(3)反应
 中,碳原子的杂化方式由
中,碳原子的杂化方式由(4)一种铜的配合物为
 ,其配体为
,其配体为
您最近一年使用:0次
4 .  在冶金、化工、电子等多个领域有着广泛的应用,以硫酸工业产生的废钒催化剂为原料(含
在冶金、化工、电子等多个领域有着广泛的应用,以硫酸工业产生的废钒催化剂为原料(含 、
、 、
、 、
、 以及少量的
以及少量的 等)制备
等)制备 的工艺流程如下。
的工艺流程如下。 、
、 形式存在,
形式存在, 较大时
较大时 可转化为
可转化为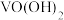 沉淀,
沉淀,
(1) 中
中 为
为___________ (填“过渡元素”或“主族元素”)。
(2)“酸浸还原”过程中。
①硫酸的用量会影响钒的浸出率, 需保持在1.2以下,说明原因
需保持在1.2以下,说明原因___________ 。
②写出 发生反应的离子方程式
发生反应的离子方程式___________ 。
③除 被还原外,写出还可能被还原的离子
被还原外,写出还可能被还原的离子___________ (写离子符号)。
④若以磷酸为介质处理废钒催化剂,可以提高钒的浸出率。一种钒磷配合物的结构如下图所示,形成配位键时 提供
提供___________ (填“孤对电子”或“空轨道”)。 (有机层)
(有机层)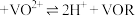 (有几层),则“反萃取”进行的条件是
(有几层),则“反萃取”进行的条件是___________ (填“酸性”“中性”或“碱性”)。
(4)从上述流程中___________ (填“滤渣”“水溶液”或“滤液”)中可提取回收 。
。
(5)若“焙烧”时得到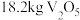 ,计算理论上消耗空气中的
,计算理论上消耗空气中的 在标准状况下的体积
在标准状况下的体积___________ ( ,不要求计算过程)。
,不要求计算过程)。
 在冶金、化工、电子等多个领域有着广泛的应用,以硫酸工业产生的废钒催化剂为原料(含
在冶金、化工、电子等多个领域有着广泛的应用,以硫酸工业产生的废钒催化剂为原料(含 、
、 、
、 、
、 以及少量的
以及少量的 等)制备
等)制备 的工艺流程如下。
的工艺流程如下。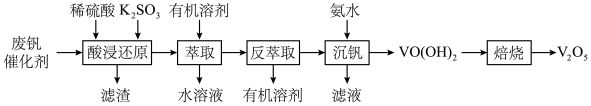
 、
、 形式存在,
形式存在, 较大时
较大时 可转化为
可转化为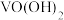 沉淀,
沉淀,(1)
 中
中 为
为(2)“酸浸还原”过程中。
①硫酸的用量会影响钒的浸出率,
 需保持在1.2以下,说明原因
需保持在1.2以下,说明原因②写出
 发生反应的离子方程式
发生反应的离子方程式③除
 被还原外,写出还可能被还原的离子
被还原外,写出还可能被还原的离子④若以磷酸为介质处理废钒催化剂,可以提高钒的浸出率。一种钒磷配合物的结构如下图所示,形成配位键时
 提供
提供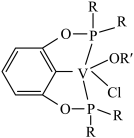
 (有机层)
(有机层)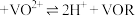 (有几层),则“反萃取”进行的条件是
(有几层),则“反萃取”进行的条件是(4)从上述流程中
 。
。(5)若“焙烧”时得到
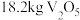 ,计算理论上消耗空气中的
,计算理论上消耗空气中的 在标准状况下的体积
在标准状况下的体积 ,不要求计算过程)。
,不要求计算过程)。
您最近一年使用:0次
5 . 某矿石中富含 和
和 ,还含有Fe、Al、Si、Ca的氧化物。以该矿石为原料制备
,还含有Fe、Al、Si、Ca的氧化物。以该矿石为原料制备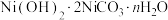 的流程如图所示,请回答下列问题:
的流程如图所示,请回答下列问题:
②Ni2O3在酸性条件下具有强氧化性。
(1)基态Ni原子的简化电子排布式为___________ ;基态 的价层电子轨道表示式为
的价层电子轨道表示式为___________ 。
(2)滤渣1的主要成分为___________ ;加入Ni2O3后生成 的离子方程式为
的离子方程式为___________ 。
(3)“萃取”时发生的反应: ,“反萃取”时加入稀硫酸的目的是
,“反萃取”时加入稀硫酸的目的是___________ 。一种有机萃取剂M及萃取 后生成的N的结构如图所示,M中碳原子的杂化方式有
后生成的N的结构如图所示,M中碳原子的杂化方式有___________ 种;N中Cu元素的化合价为___________ 价,N中提供孤电子对形成配位键的原子有___________ (填标号)。___________ 。
 和
和 ,还含有Fe、Al、Si、Ca的氧化物。以该矿石为原料制备
,还含有Fe、Al、Si、Ca的氧化物。以该矿石为原料制备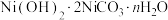 的流程如图所示,请回答下列问题:
的流程如图所示,请回答下列问题: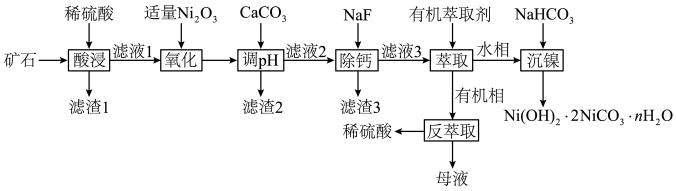
| 金属离子 |  |  |  |  |  |
| 开始沉淀的pH | 7.5 | 2.2 | 3.7 | 4.7 | 7.0 |
| 完全沉淀的pH | 9.0 | 3.3 | 4.5 | 6.5 | 8.7 |
(1)基态Ni原子的简化电子排布式为
 的价层电子轨道表示式为
的价层电子轨道表示式为(2)滤渣1的主要成分为
 的离子方程式为
的离子方程式为(3)“萃取”时发生的反应:
 ,“反萃取”时加入稀硫酸的目的是
,“反萃取”时加入稀硫酸的目的是 后生成的N的结构如图所示,M中碳原子的杂化方式有
后生成的N的结构如图所示,M中碳原子的杂化方式有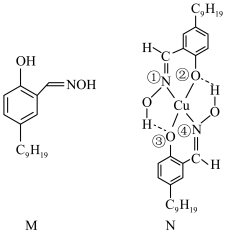
您最近一年使用:0次
名校
解题方法
6 . 下列说法错误的是
| A.相同质量的H2O(l)的体积小于H2O(s)的,原因之一是H2O(l)中含有更多的氢键 |
B.等物质的量的 、 、 中含σ键的个数之比为3:4 中含σ键的个数之比为3:4 |
C.已知 的4s轨道和4p轨道可以形成sp3杂化轨道,则 的4s轨道和4p轨道可以形成sp3杂化轨道,则 的空间结构可能为正四面体形 的空间结构可能为正四面体形 |
| D.晶体具有自范性,能自发地呈现多面体外形 |
您最近一年使用:0次
名校
7 . 一水合甘氨酸锌是一种矿物类饲料添加剂,其结构简式如图所示。下列说法正确的是
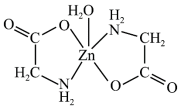
| A.基态Zn原子的核外电子有30种运动状态 |
| B.该结构中元素电负性大小比较:C<O<N |
| C.分子中C、N的杂化方式完全相同 |
D.该结构中Zn为中心原子,O、N为配位原子,与 的配合能力:N<O 的配合能力:N<O |
您最近一年使用:0次
名校
8 . 除少数卤化物外,大部分非金属卤化物都易水解,且反应不可逆。卤化物的水解机理分亲核水解和亲电水解。发生亲核水解的结构条件:中心原子具有 和有空的价轨道:发生亲电水解的结构条件:中心原子有孤对电子,可作Lewis碱,接受
和有空的价轨道:发生亲电水解的结构条件:中心原子有孤对电子,可作Lewis碱,接受 的
的 进攻。其中
进攻。其中 的亲核水解机理如图。下列说法不正确的是
的亲核水解机理如图。下列说法不正确的是
 和有空的价轨道:发生亲电水解的结构条件:中心原子有孤对电子,可作Lewis碱,接受
和有空的价轨道:发生亲电水解的结构条件:中心原子有孤对电子,可作Lewis碱,接受 的
的 进攻。其中
进攻。其中 的亲核水解机理如图。下列说法不正确的是
的亲核水解机理如图。下列说法不正确的是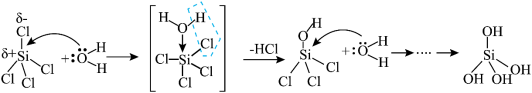
| A.第一个过程Si的杂化方式发生了改变 |
B. 的水解历程中只存在极性键的断裂与生成 的水解历程中只存在极性键的断裂与生成 |
C. 为极性分子 为极性分子 |
D.由上述理论可知 水解会生成 水解会生成 和HCl 和HCl |
您最近一年使用:0次
名校
9 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A. 羟基 羟基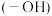 所含的电子数为 所含的电子数为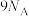 |
B.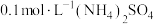 溶液中, 溶液中, 的数目为 的数目为 |
C. 中共价键的数目为 中共价键的数目为 |
D.标准状况下, 分子中含有的分子数目为 分子中含有的分子数目为 |
您最近一年使用:0次
名校
10 .  晶体的晶胞如下图所示(已知该立方晶胞的边长为
晶体的晶胞如下图所示(已知该立方晶胞的边长为 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,
, 的摩尔质量为
的摩尔质量为 ),以下说法正确的是
),以下说法正确的是
 晶体的晶胞如下图所示(已知该立方晶胞的边长为
晶体的晶胞如下图所示(已知该立方晶胞的边长为 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,
, 的摩尔质量为
的摩尔质量为 ),以下说法正确的是
),以下说法正确的是
A. 中,中心离子的配位数为8 中,中心离子的配位数为8 |
B.离 最近的相同微粒有6个 最近的相同微粒有6个 |
C.若规定A点原子坐标为 , , 点原子坐标为 点原子坐标为 ,则 ,则 点原子坐标为 点原子坐标为 |
D. 晶体的密度为 晶体的密度为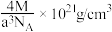 |
您最近一年使用:0次



