(1)根据以上信息可推知:C3O2在常温下为
(2)苯六甲酸(即苯分子中每个氢原子都被羧基取代生成的物质)完全脱水的产物也是一种碳的氧化物,它的分子式为
(1)在元素周期表中,铂元素与铁元素同族,则铂元素位于
A.s区 B.p区 C.d区 D.ds区 E.f区
(2)二氯二吡啶合铂是由Pt2+、Cl-和吡啶结合形成的铂配合物,有顺式和反式两种同分异构体。科学研究表明,反式分子和顺式分子一样具有抗癌活性。
①Cl-的最外层电子排布式为
②吡啶分子是大体积平面配体,其结构简式如图所示,该配体的配位原子是
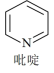
③二氯二吡啶合铂分子中存在的微粒间作用力有
 填序号
填序号 。
。a.离子键 b.配位键 c.金属键 d.非极性键 e.氢键
④反式二氯二吡啶合铂分子结构如图所示,该分子是
 选填“极性”、“非极性”
选填“极性”、“非极性” 。
。
(3)已知金属铂的密度为d g/cm3,NA代表阿伏加德罗常数的值,金属铂的相对原子质量为 M。如图分别表示金属铂原子的堆积方式、晶胞特征,则金属铂的堆积方式为

 3UO2+10NH3↑+9CO2↑+N2↑+9H2O↑;回答下列问题:
3UO2+10NH3↑+9CO2↑+N2↑+9H2O↑;回答下列问题:(1)反应所得气态化合物中属于非极性分子的是
(2)某种铀氮化物的晶体结构是NaCl型。NaCl的Bom-Haber循环如图所示。已知:元素的一个气态原子获得电子成为气态阴离子时所放出的能量称为电子亲和能。下列有关说法正确的是

a.Cl-Cl键的键能为119.6kJ/mol b.Na的第一电离能为603.4kJ/mol
c.NaCl的晶格能为785.6kJ/mol d.Cl的第一电子亲和能为348.3kJ/mol
(3)依据VSEPR理论推测
 的空间构型为
的空间构型为 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为π
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为π ),则
),则 中的大π键应表示为
中的大π键应表示为(4)UO2可用于制备UF4:2UO2+5NH4HF2
 2UF4·2NH4F+3NH3↑+4H2O,其中
2UF4·2NH4F+3NH3↑+4H2O,其中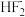 的结构表示为[F—H…F]-,反应中断裂的化学键有
的结构表示为[F—H…F]-,反应中断裂的化学键有a.氢键 b.极性键 c.离子键 d.金属键 e.非极性键
(5)铀氮化物的某两种晶胞如图所示:

①晶胞a中铀元素的化合价为
②已知晶胞b的密度为dg/cm3,U原子的半径为r1cm,N原子的半径为为r2cm,设NA为阿伏加 德罗常数的值,则该晶胞的空间利用率为
(6)氢基倍半硅氧烷的分子结构如图所示,该分子的分子式为
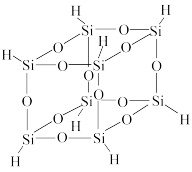
①CH3COOH分子中碳原子的杂化类型有sp2和sp3两种
②元素Ge位于周期表第四周期IVA族,核外电子排布式为 [Ar]4s24p2,属于p区
③非极性分子往往具有高度对称性,如BF3、PCl5、H2O2、CO2这样的分子
④Na2O、Na2O2、NaHSO4晶体中的阴、阳离子个数比均为1 :2
⑤Cu(OH)2是一种蓝色絮状沉淀,既能溶于硝酸、也能溶于氨水,是两性氢氧化物
⑥氨水中大部分NH3与H2O以氢键(用“...”表示)结合成NH3·H2O分子,根据氨水的性质可知NH3·H2O的结构式可记为:
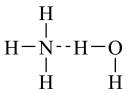
⑦HF沸点高于HCl,是因为 HCl共价键键能小于HF
⑧可燃冰中甲烷分子与水分子之间存在氢键
| A.4项 | B.5项 | C.6项 | D.7项 |
5 . 2019 年的化学诺贝尔奖颁给了为锂电池研究作出贡献的三位科学家,其研究的是两种常见锂电池:一种是采用镍钴锰酸锂Li(NiCoMn)O2或镍钴铝酸锂为正极的“三元材料锂电池”;另一种是采用磷酸铁锂(LiFePO4)为正极的电池。请回答下列问题:
(1)Mn位于元素周期表的
(2)磷元素可以形成多种含氧酸H3PO4、H3PO2、H3PO3、HPO3,这四种酸中酸性最强的是 的空间构型是
的空间构型是
(3)PH3是
(4)硫化锂Li2S(摩尔质量Mg∙mol-1)的纳米晶体是开发先进锂电池的关键材料,硫化锂的晶体为反萤石结构,其晶胞结构如下图。S2-的配位数是

(1)二氧化钛作光催化剂能将居室污染物甲醛、苯等有害气体可转化为二氧化碳和水,达到无害化。有关甲醛、苯、二氧化碳及水说法正确的是
A.苯与B3N3H6互为等电子体
B.甲醛、苯分子中碳原子均采用sp2杂化
C.苯、二氧化碳是非极性分子,水和甲醛是极性分子
D.水的沸点比甲醛高得多,是因为水分子间能形成氢键
(2)2007年诺贝尔物理学奖为法国科学家阿尔贝·费尔和德国科学家彼得·格林贝格尔共同获得,以表彰他们在巨磁电阻效应(CMR效应)研究方面的成就。某钙钛型复合氧化物(如图1),以A原子为晶胞的顶点,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Mn、Fe时,这种化合物具有CMR效应。

①用A、B、O表示这类特殊晶体的化学式:
②已知La为+3价,当被钙等二价元素A替代时,可形成复合钙钛矿化合物La1-xAxMnO3,(x<0.1),此时一部分锰转变为+4价。导致材料在某一温度附近有反铁磁—铁磁、铁磁—顺磁转变及金属—半导体的转变,则La1-xAxMnO3中三价锰与四价锰的物质的量之比为:
③Mn的核外电子排布式为:
④下列有关说法正确的是
A.镧、锰、氧分别位于周期表f、d、p区
B.氧的第一电离能比氮的第一电离能大
C.锰的电负性为1.59,Cr的电负性为1.66,说明锰的金属性比铬强
D.铬的堆积方式与钾相同,则其堆积方式如图2

(1)固氮酶有铁蛋白和钼铁蛋白两种,它们不仅能够催化N2还原成NH3,还能将环境底物乙炔催化还原成乙烯。
①乙炔是
②碳负离子CH3-的立体构型为
③根据等电子原理,NO+的电子式为
(2)钒可用于合成电池电极,也可用于人工合成二价的钒固氮酶(结构如图a)。

①V2+基态时核外电子排布式为
②钒固氮酶中钒的配位原子有
(3)烟酰胺(结构如图b)可用于合成光合辅酶NADPH,烟酰胺分子中氮原子的杂化轨道类型有
(4)12 g石墨烯(结构如图c)中含有的正六边形数目约为
| 目前空气的主要成分 |  、 、 、 、 、水蒸气及稀有气体(如 、水蒸气及稀有气体(如 、 、 等) 等) |
| 原始大气的主要成分 |  、 、 、 、 、 、 等 等 |
用上表所涉及的分子填写下列空白:
(1)含有10个电子的分子有
(2)由极性键构成的非极性分子有
(3)与
 可直接形成配位键的分子有
可直接形成配位键的分子有(4)不含孤电子对的分子(稀有气体除外)是
(5)极易溶于水且水溶液呈碱性的分子是
(6)
 的结构可表示为
的结构可表示为 ,与
,与 结构最相似的分子是
结构最相似的分子是 分子中有一个键的形成与另外两个键不同,它叫
分子中有一个键的形成与另外两个键不同,它叫 是一种油状液体,其分子空间构型与
是一种油状液体,其分子空间构型与 的相似,下列有关
的相似,下列有关 和
和 的叙述正确的是( )
的叙述正确的是( )A. 分子中 分子中 键的键长与 键的键长与 分子中 分子中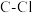 键的键长相等 键的键长相等 |
B. 分子是非极性分子 分子是非极性分子 |
C.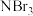 的熔沸点比 的熔沸点比 的低 的低 |
D.在氨水中,大部分 与 与 以氢键结合形成 以氢键结合形成 ,则 ,则 的结构式为 的结构式为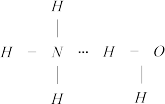 |
A. ( ( ,且 ,且 为整数)型分子中,若中心原子没有孤对电子,则 为整数)型分子中,若中心原子没有孤对电子,则 为空间对称结构,属于非极性分子 为空间对称结构,属于非极性分子 |
| B.水很稳定是因为水中含有大量的氢键 |
C. 、 、 、 、 分子中的 分子中的 分别形成2个、3个、4个键,故 分别形成2个、3个、4个键,故 分别采取 分别采取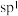 、 、 、 、 杂化 杂化 |
D.配合物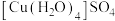 中,中心离子是 中,中心离子是 ,配体是 ,配体是 ,配位数是1 ,配位数是1 |



