解题方法
1 . 回答下列问题。
(1)N2H4是___________ (填“极性”或“非极性”)分子,N2H4中中心原子N杂化类型为___________ 。
(2)乙炔分子的碳原子采取什么杂化方式?___________ ;它的杂化轨道用于形成什么化学键?___________ ;怎样理解它存在碳碳三键?___________ 。
(3)向绿色的NiSO4溶液中滴加过量的氨水,溶液会变成深蓝色,其原因是溶液中生成了一种六配体的配离子,该配离子的化学式为___________ 。
(1)N2H4是
(2)乙炔分子的碳原子采取什么杂化方式?
(3)向绿色的NiSO4溶液中滴加过量的氨水,溶液会变成深蓝色,其原因是溶液中生成了一种六配体的配离子,该配离子的化学式为
您最近一年使用:0次
名校
2 . 依据原子结构知识回答下列问题。
(1)基态硅原子的电子排布式是___________ 。
(2)基态铁原子有___________ 个未成对电子,基态 的价电子排布图为
的价电子排布图为___________ 。
(3)下列说法错误的是___________(填字母)。
(4)过氧化氢( )是一种医用消毒杀菌剂。已知
)是一种医用消毒杀菌剂。已知 的结构如图所示。
的结构如图所示。 不是直线形的,两个氢原子犹如在半展开的书的两面纸上,书面角为93°52′,两个
不是直线形的,两个氢原子犹如在半展开的书的两面纸上,书面角为93°52′,两个 与
与 的夹角均为96°52′。
的夹角均为96°52′。

① 的电子式为
的电子式为___________ ,结构式为___________ 。
② 中存在
中存在___________ 键和___________ 键,为___________ (填“极性”或“非极性”)分子。
(1)基态硅原子的电子排布式是
(2)基态铁原子有
 的价电子排布图为
的价电子排布图为(3)下列说法错误的是___________(填字母)。
A.元素的电负性: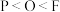 | B.元素的第一电离能: |
C.离子半径: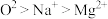 | D.原子的未成对电子数: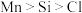 |
(4)过氧化氢(
 )是一种医用消毒杀菌剂。已知
)是一种医用消毒杀菌剂。已知 的结构如图所示。
的结构如图所示。 不是直线形的,两个氢原子犹如在半展开的书的两面纸上,书面角为93°52′,两个
不是直线形的,两个氢原子犹如在半展开的书的两面纸上,书面角为93°52′,两个 与
与 的夹角均为96°52′。
的夹角均为96°52′。
①
 的电子式为
的电子式为②
 中存在
中存在
您最近一年使用:0次
2024-02-03更新
|
339次组卷
|
2卷引用:河南省周口市西华县第一高级中学2023-2024学年高二上学期月考化学试卷
名校
3 . 氨基乙酸铜被广泛应用于染料、涂料、塑料和电池等领域,其化学式为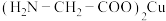 ,结构如图所示。
,结构如图所示。 原子的电子排布式为
原子的电子排布式为_______ , 位于元素周期表中
位于元素周期表中_______ 区元素(填“s、p、d、ds和f”其中一个)。
(2)氨基乙酸铜中碳原子的杂化方式有_______ 、_______ ,该分子中有_______ 个 键。
键。
(3)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态
表示,称为电子的自旋磁量子数。对于基态 原子,其价电子自旋磁量子数的代数和为
原子,其价电子自旋磁量子数的代数和为_______ 。
(4) 原子的第一电离能比
原子的第一电离能比 原子的
原子的_______ (填“大”或“小”),其原因是_______ 。
(5)氨基乙酸铜可由碳酸铜、氯乙酸、乙二胺等制得,碳酸铜中 的VSEPR模型名称为
的VSEPR模型名称为_______ ,氯乙酸的酸性大于乙酸的原因是_______ 。
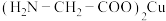 ,结构如图所示。
,结构如图所示。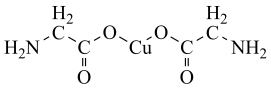
 原子的电子排布式为
原子的电子排布式为 位于元素周期表中
位于元素周期表中(2)氨基乙酸铜中碳原子的杂化方式有
 键。
键。(3)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用
 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态
表示,称为电子的自旋磁量子数。对于基态 原子,其价电子自旋磁量子数的代数和为
原子,其价电子自旋磁量子数的代数和为(4)
 原子的第一电离能比
原子的第一电离能比 原子的
原子的(5)氨基乙酸铜可由碳酸铜、氯乙酸、乙二胺等制得,碳酸铜中
 的VSEPR模型名称为
的VSEPR模型名称为
您最近一年使用:0次
2024-01-23更新
|
347次组卷
|
2卷引用:广东省深圳市光明区2023-2024学年高二上学期1月期末学业水平调研化学试题
名校
4 . 下列分子结构图中的“○”表示氢原子,“●”表示短周期中相邻的三种元素原子。小黑点表示没有形成共价键的最外层电子,短线表示共价键。

(1)以上分子中,中心原子采用 杂化的是
杂化的是_____ (填化学式)。
(2)③的分子中有_____ 个 键。③与溴的四氯化碳溶液反应中,断裂的是③分子中的
键。③与溴的四氯化碳溶液反应中,断裂的是③分子中的_____ 键(填“ ”或“
”或“ ),形成的是
),形成的是_____ 键(填“ ”或“
”或“ ”)。
”)。
(3)4种分子中,属于极性分子的是_____ (填序号,下同)。键角由大到小的顺序是_____ ,能结合质子(即 )形成稳定离子的是
)形成稳定离子的是_____ 。
(4)已知液态①和④相似,也可发生微弱的电离,电离出含有相同电子数的微粒,则①的电离方程式为_____ 。

(1)以上分子中,中心原子采用
 杂化的是
杂化的是(2)③的分子中有
 键。③与溴的四氯化碳溶液反应中,断裂的是③分子中的
键。③与溴的四氯化碳溶液反应中,断裂的是③分子中的 ”或“
”或“ ),形成的是
),形成的是 ”或“
”或“ ”)。
”)。(3)4种分子中,属于极性分子的是
 )形成稳定离子的是
)形成稳定离子的是(4)已知液态①和④相似,也可发生微弱的电离,电离出含有相同电子数的微粒,则①的电离方程式为
您最近一年使用:0次
名校
5 . 工业排放的某些烟气中含有二氧化硫等大气污染物,对其进行脱硫治理不仅可以防止有害物质排放,还可以生产其他有用的产品。
(1) 分子的空间结构和分子的极性分别为___________。
分子的空间结构和分子的极性分别为___________。
(2)第一电离能: ,结合核外电子排布相关知识,说明其原因
,结合核外电子排布相关知识,说明其原因___________ 。
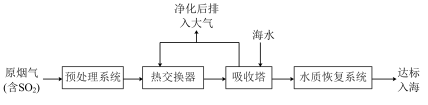
沿海地区的某煤电厂开发出海水脱硫的新工艺,流程如下图所示: ,
, 的电离常数如下表所示:
的电离常数如下表所示:
(3)在吸收塔内,烟气应从吸收塔的___________ 通入,与塔顶喷淋的海水充分接触。
A.上部 B.中部 C.下部
(4)吸收塔内温度不宜过高,原因可能是___________ 。(列举1条)吸收塔内 和海水中
和海水中 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(5)若煤电厂排放烟气量为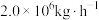 ,其中含
,其中含 为0.15%,该烟气经海水脱硫处理后
为0.15%,该烟气经海水脱硫处理后 为
为 ,则脱硫率
,则脱硫率
___________ 。( )
)
(6)离子液体(ILs)也可以用来处理工业烟气。ILs的负离子吸收 后生成
后生成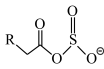 。欲确定
。欲确定 中虚线框内基团的结构,可采用的分析方法有___________。
中虚线框内基团的结构,可采用的分析方法有___________。
工业上还可用 溶液吸收烟气中的二氧化硫,随着反应的进行,其吸收能力会逐渐降低。
溶液吸收烟气中的二氧化硫,随着反应的进行,其吸收能力会逐渐降低。
(7)为使 再生,最适宜向吸收能力降低的溶液中加入或通入一定量的___________。
再生,最适宜向吸收能力降低的溶液中加入或通入一定量的___________。
(8)使用 溶液脱硫时,溶液的pH通常需控制在
溶液脱硫时,溶液的pH通常需控制在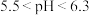 。结合
。结合 的性质和下图,分析pH不宜过小和过大的原因
的性质和下图,分析pH不宜过小和过大的原因___________ 。
(1)
 分子的空间结构和分子的极性分别为___________。
分子的空间结构和分子的极性分别为___________。| A.直线形,非极性 | B.直线形,极性 | C.角形,非极性 | D.角形,极性 |
(2)第一电离能:
 ,结合核外电子排布相关知识,说明其原因
,结合核外电子排布相关知识,说明其原因沿海地区的某煤电厂开发出海水脱硫的新工艺,流程如下图所示:
 ,
, 的电离常数如下表所示:
的电离常数如下表所示:| 弱酸 |  |  |
 | 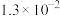 | 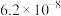 |
 | 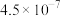 | 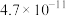 |
(3)在吸收塔内,烟气应从吸收塔的
A.上部 B.中部 C.下部
(4)吸收塔内温度不宜过高,原因可能是
 和海水中
和海水中 发生反应的离子方程式为
发生反应的离子方程式为(5)若煤电厂排放烟气量为
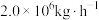 ,其中含
,其中含 为0.15%,该烟气经海水脱硫处理后
为0.15%,该烟气经海水脱硫处理后 为
为 ,则脱硫率
,则脱硫率
 )
)(6)离子液体(ILs)也可以用来处理工业烟气。ILs的负离子吸收
 后生成
后生成 。欲确定
。欲确定 中虚线框内基团的结构,可采用的分析方法有___________。
中虚线框内基团的结构,可采用的分析方法有___________。| A.原子发射光谱 | B.红外光谱 | C.核磁共振氢谱 | D.晶体X射线衍射 |
工业上还可用
 溶液吸收烟气中的二氧化硫,随着反应的进行,其吸收能力会逐渐降低。
溶液吸收烟气中的二氧化硫,随着反应的进行,其吸收能力会逐渐降低。(7)为使
 再生,最适宜向吸收能力降低的溶液中加入或通入一定量的___________。
再生,最适宜向吸收能力降低的溶液中加入或通入一定量的___________。A. | B.CaO | C. | D.NaOH |
(8)使用
 溶液脱硫时,溶液的pH通常需控制在
溶液脱硫时,溶液的pH通常需控制在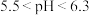 。结合
。结合 的性质和下图,分析pH不宜过小和过大的原因
的性质和下图,分析pH不宜过小和过大的原因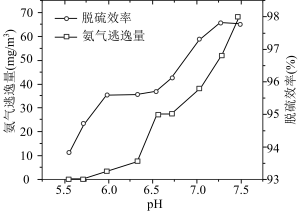
您最近一年使用:0次
2024-01-13更新
|
294次组卷
|
3卷引用:上海市四区联考2023-2024学年高三上学期化学一模试卷
名校
6 . 卤素单质及其化合物在生产、生活、化工、医药、材料等领域中有着非常广泛的应用。回答下列问题:
(1)基态Br原子的价层电子轨道表示式为__________ 。
(2)下列现象中,不能用“相似相溶”原理解释的是__________(填序号)。
(3)卤族元素除F元素外,Cl、Br、I均可形成多种含氧酸根,① ;②
;②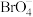 ;③
;③ 中键角最大的是
中键角最大的是__________ (填序号)。
(4)光气( )在有机合成中常作氯化剂,分子中所有原子均满足8电子稳定结构,
)在有机合成中常作氯化剂,分子中所有原子均满足8电子稳定结构, 分子中
分子中 键和
键和 键的个数比为
键的个数比为__________ 。
(5)请在下图含溴有机物的结构简式中,用星号(*)标出含有的手性碳原子__________ 。 的数值来衡量。室温下,
的数值来衡量。室温下, ;
; ,依据数据分析,酸性:
,依据数据分析,酸性:
__________  (填“>”“<”或“=”),请从键的极性角度解释原因
(填“>”“<”或“=”),请从键的极性角度解释原因__________ 。
(1)基态Br原子的价层电子轨道表示式为
(2)下列现象中,不能用“相似相溶”原理解释的是__________(填序号)。
A.HCl易溶于 | B. 易溶于NaOH溶液 易溶于NaOH溶液 |
C. 易溶于 易溶于 | D. 易溶于 易溶于 |
 ;②
;②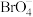 ;③
;③ 中键角最大的是
中键角最大的是(4)光气(
 )在有机合成中常作氯化剂,分子中所有原子均满足8电子稳定结构,
)在有机合成中常作氯化剂,分子中所有原子均满足8电子稳定结构, 分子中
分子中 键和
键和 键的个数比为
键的个数比为(5)请在下图含溴有机物的结构简式中,用星号(*)标出含有的手性碳原子
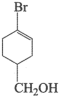
 的数值来衡量。室温下,
的数值来衡量。室温下, ;
; ,依据数据分析,酸性:
,依据数据分析,酸性:
 (填“>”“<”或“=”),请从键的极性角度解释原因
(填“>”“<”或“=”),请从键的极性角度解释原因
您最近一年使用:0次
2024-01-13更新
|
494次组卷
|
3卷引用:辽宁省锦州市2023-2024学年高二上学期1月期末化学试题
名校
7 . “天问一号”轨道飞行器近距离拍摄了火星北极,看到大量白色冰冻区域, 主要是二氧 化碳低温凝结形成的干冰,虽然看起来和地球两极很像,但实际温度却比地球两极冷多了!
(1)已知 25℃时, H2CO3 的 Ka1 = 4.2×10-7 、Ka2 = 4.8×10- 11 ,HCN 的 Ka = 4.0×10-10,若向NaCN 溶液中通入少量 CO2,发生反应的离子方程式为___________ 。
(2)下列关于二氧化碳的说法正确的是______。
(1)已知 25℃时, H2CO3 的 Ka1 = 4.2×10-7 、Ka2 = 4.8×10- 11 ,HCN 的 Ka = 4.0×10-10,若向NaCN 溶液中通入少量 CO2,发生反应的离子方程式为
(2)下列关于二氧化碳的说法正确的是______。
A.电子式为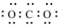 | B.空间填充模型为  |
| C.CO2 是极性分子, 能溶于水 | D.CO2 的水溶液能够导电,但 CO2是非电解质 |
您最近一年使用:0次
名校
8 . Ⅰ.自然界中的氮循环和硫循环紧密相关,它们通过各种生物地球化学过程耦合链接,在此过程中微生物发挥着至关重要的作用。
(1)生物固氮是土壤氮素的重要来源之一、生物固氮是指根瘤菌___________。
(2)动植物体内的氮除了蛋白质外,在___________ 中也大量存在。
A.纤维素 B.脂肪 C.核酸
(3)水体中的 在反硝化菌作用下与
在反硝化菌作用下与 反应生成
反应生成 ,写出发生反应的离子方程式
,写出发生反应的离子方程式___________ 。
Ⅱ.微生物分解海洋生物遗体时会向大气中释放以二甲硫醚( )为代表的有机硫化合物,是硫循环与碳循环的重要环节之一
)为代表的有机硫化合物,是硫循环与碳循环的重要环节之一
(4)关于二甲硫醚分子结构说法正确的是___________。
(5)二甲醚( )与二甲硫醚结构相似,关于两者物理性质比较及原因解释正确的是___________。
)与二甲硫醚结构相似,关于两者物理性质比较及原因解释正确的是___________。
(6)二甲硫醚在大气中经过一系列的氧化,最终生成硫酸盐气溶胶。高压电场常用于气溶胶的净化去除,该过程称为___________。
Ⅲ.脱硫木醋杆菌能将有机化合物中的硫(视作O价硫)转化为气体,此过程表示如下,该反应也是湿沼区域腐败臭味的来源之一
□ □CH₃COOH+□
□CH₃COOH+□ ___________
___________ +□
+□
(7)完成并配平该反应(若化学计量数为1可不写)_______ 。
(8)若产生的气体在标准状况下体积为672 mL,转移电子数为___________ 。
(9)脱硫木醋杆菌利用该反应获取能量,简要分析该反应的自发性___________ 。
(1)生物固氮是土壤氮素的重要来源之一、生物固氮是指根瘤菌___________。
| A.从土壤中吸收含氮养料 | B.将氨转变为植物蛋白质 |
| C.将氨转变成硝酸 | D.将空气中的氮气转变成氨 |
A.纤维素 B.脂肪 C.核酸
(3)水体中的
 在反硝化菌作用下与
在反硝化菌作用下与 反应生成
反应生成 ,写出发生反应的离子方程式
,写出发生反应的离子方程式Ⅱ.微生物分解海洋生物遗体时会向大气中释放以二甲硫醚(
 )为代表的有机硫化合物,是硫循环与碳循环的重要环节之一
)为代表的有机硫化合物,是硫循环与碳循环的重要环节之一(4)关于二甲硫醚分子结构说法正确的是___________。
| A.只含有极性键的极性分子 | B.含有非极性键的极性分子 |
| C.只含有极性键的非极性分子 | D.含有非极性键的非极性分子 |
 )与二甲硫醚结构相似,关于两者物理性质比较及原因解释正确的是___________。
)与二甲硫醚结构相似,关于两者物理性质比较及原因解释正确的是___________。| A.二甲醚熔点相对更高,因为二甲醚分子间存在氢键,作用更强 |
| B.二甲硫醚熔点相对更高,因为二甲硫醚相对分子质量更大,范德华力更强 |
| C.二甲醚水溶性相对更好,因为二甲醚能与水形成氢键 |
| D.二甲硫醚水溶性相对更好,因为二甲硫醚能形成内盐 |
| A.电离 | B.电解 | C.电泳 | D.渗析 |
Ⅲ.脱硫木醋杆菌能将有机化合物中的硫(视作O价硫)转化为气体,此过程表示如下,该反应也是湿沼区域腐败臭味的来源之一
□
 □CH₃COOH+□
□CH₃COOH+□ ___________
___________ +□
+□
(7)完成并配平该反应(若化学计量数为1可不写)
(8)若产生的气体在标准状况下体积为672 mL,转移电子数为
(9)脱硫木醋杆菌利用该反应获取能量,简要分析该反应的自发性
您最近一年使用:0次
名校
解题方法
9 . 官能团决定着有机物的性质,官能团的转化是有机合成的主要方式之一。
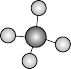
(1)甲烷是最简单的有机物。通过甲烷分子的球棍模型不能得出的信息是_______。
(2)酒精是一种常见的含氧衍生物。关于75%酒精的叙述的是_______。
(3)丙烯二聚体CH2=CHCH2CH(CH3)2是合成“人工肺”(ECMO)设备膜丝的重要原料,下列关于丙烯二聚体说法正确的是_______。
(1)甲烷是最简单的有机物。通过甲烷分子的球棍模型不能得出的信息是_______。

| A.C-H的共用电子对偏向C原子 |
| B.正四面体结构 |
| C.非极性分子 |
| D.二氯取代物只有一种 |
(2)酒精是一种常见的含氧衍生物。关于75%酒精的叙述的是_______。
| A.能够消毒、杀菌 | B.必须避光保存 |
| C.在空气中易氧化变质 | D.可直接用于制乙烯 |
(3)丙烯二聚体CH2=CHCH2CH(CH3)2是合成“人工肺”(ECMO)设备膜丝的重要原料,下列关于丙烯二聚体说法正确的是_______。
| A.加聚产物可以使溴水褪色 |
B.与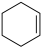 互为同分异构体 互为同分异构体 |
| C.催化加氢生成的一氯代物有4种 |
| D.完全燃烧与等质量丙烯耗氧量相同 |
您最近一年使用:0次
名校
解题方法
10 . Ⅰ.元素周期表的确立是化学发展史上的里程碑。我们往往可以通过元素在周期表中的位置,对某些不熟悉元素的性质及用途做出预测。
(1)下列具有特殊性能的材料中,由主族元素和副族元素形成化合物的是_____
(2)下列事实不能用元素周期律解释的是___________
(3)短周期元素 X、Y、Z、M、N、W原子序数依次递增,六种元素形成的一种化合物结构如图所示,其中元素Z最外层电子数为内层电子数的3倍。下列说法正确的是_________

Ⅱ.在地壳里硅的含量在所有元素中居第二位,仅次于氧。接下来我们尝试利用元素周期表,通过与其相邻元素类比来了解硅的一些特点。
(4)硅在元素周期表中位于第___________ 周期___________ 族。
(5)晶体硅的结构和金刚石结构相似,碳化硅(SiC)也是一种具有类似于金刚石结构的晶体,其中碳原子核硅原子的位置是交替的。在①金刚石,②晶体硅,③碳化硅这三种晶体中,它们的熔点从高到低的顺序是___________
(6)与铝类似,硅也能溶于强碱溶液并生成硅酸根(SiO )。写出硅与氢氧化钠反应的离子方程式:
)。写出硅与氢氧化钠反应的离子方程式:___________ 。
(7)比较元素非金属性:Si___________ P(选填“<”或“>”),给出一个可以用来说明该结论的化学事实是:___________ 。
(8)二氧化硅一般不能与酸反应,但可以与氢氟酸发生如下反应:SiO2+4HF=SiF4↑+2H2O,二氧化硅属于___________ (选填“酸性”、“碱性”或“两性”)氧化物。该反应涉及的所有元素中原子半径最小的是___________ (填元素符号),生成物中属于极性分子的是___________ (填化学式)。
(1)下列具有特殊性能的材料中,由主族元素和副族元素形成化合物的是_____
| A.半导体材料砷化镓 | B.吸氢材料镧镍合金 |
| C.透明陶瓷材料硒化锌 | D.超导材料K3C60 |
(2)下列事实不能用元素周期律解释的是___________
| A.F2在暗处遇 H2爆炸,I2在暗处遇H2几乎不反应 |
| B.Br2和 NaI溶液发生置换反应,和 NaCl溶液不发生置换反应 |
| C.金属 Na 和熔融KCl反应置换出金属K |
| D.常温下,NaCl溶液的 pH=7, AlCl₃溶液的 pH<7 |
(3)短周期元素 X、Y、Z、M、N、W原子序数依次递增,六种元素形成的一种化合物结构如图所示,其中元素Z最外层电子数为内层电子数的3倍。下列说法正确的是_________

| A. 最高价氧化物对应水化物的酸性 W>Y>N |
| B. 元素Z与其他五种元素均可形成2种及以上化合物 |
| C. 简单离子半径Z>M>W |
| D. 元素 X与其他五种元素均可形成共价化合物 |
Ⅱ.在地壳里硅的含量在所有元素中居第二位,仅次于氧。接下来我们尝试利用元素周期表,通过与其相邻元素类比来了解硅的一些特点。
(4)硅在元素周期表中位于第
(5)晶体硅的结构和金刚石结构相似,碳化硅(SiC)也是一种具有类似于金刚石结构的晶体,其中碳原子核硅原子的位置是交替的。在①金刚石,②晶体硅,③碳化硅这三种晶体中,它们的熔点从高到低的顺序是___________
| A.①③② | B.③②① | C.③①② | D.②①③ |
(6)与铝类似,硅也能溶于强碱溶液并生成硅酸根(SiO
 )。写出硅与氢氧化钠反应的离子方程式:
)。写出硅与氢氧化钠反应的离子方程式:(7)比较元素非金属性:Si
(8)二氧化硅一般不能与酸反应,但可以与氢氟酸发生如下反应:SiO2+4HF=SiF4↑+2H2O,二氧化硅属于
您最近一年使用:0次



