名校
1 . 短周期主族元素X、Y、Z、W原子序数依次增大,常温下它们的单质有一种固体和三种气体。由这四种元素中的一种或两种组成的三种有色物质与水发生氧化还原反应时,水既不作氧化剂也不作还原剂。下列说法错误的是
| A.简单气态氢化物的沸点:W<Y |
| B.离子半径:r(W)>r(X)>r(Y)>r(Z) |
| C.这三种有色物质与水反应后,所得溶液均呈酸性 |
| D.X、Y分别与氢元素形成的化合物中可能既有极性键又有非极性键 |
您最近一年使用:0次
2 . 氢元素及其化合物在自然界广泛存在且具有重要应用。 、
、 、
、 是氢元素的3种核素,H原子最外层只有1个电子,使得H既可以形成
是氢元素的3种核素,H原子最外层只有1个电子,使得H既可以形成 又可以形成
又可以形成 ,还能形成
,还能形成 、
、 、
、 、
、 、
、 等重要化合物。下列有关说法错误的是
等重要化合物。下列有关说法错误的是
 、
、 、
、 是氢元素的3种核素,H原子最外层只有1个电子,使得H既可以形成
是氢元素的3种核素,H原子最外层只有1个电子,使得H既可以形成 又可以形成
又可以形成 ,还能形成
,还能形成 、
、 、
、 、
、 、
、 等重要化合物。下列有关说法错误的是
等重要化合物。下列有关说法错误的是A. 、 、 、 、 互为同位素 互为同位素 |
| B.水在结冰时体积膨胀,是因为水分子之间存在氢键 |
C. 、 、 两种分子中含有的共价键类型不完全相同 两种分子中含有的共价键类型不完全相同 |
D. 与水反应: 与水反应: |
您最近一年使用:0次
名校
3 . 元素周期表的一部分如图, 代表对应的元素,回答下列问题:
代表对应的元素,回答下列问题:_____ ,元素I在周期表中的位置为_____ 。
(2)D、E和J三种元素的离子半径由大到小的顺序是_____ (用离子符号表示)。
(3)图中对应元素最高价氧化物的水化物中,碱性最强的是_____ (填物质名称)。
(4)A、C和J三种元素能形成多种化合物,其中酸性最强的化合物的化学式是_____ 。
(5)元素F的单质与元素E的最高价氧化物对应水化物反应的离子方程式为_____ 。
(6)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是_____(填字母)。
 代表对应的元素,回答下列问题:
代表对应的元素,回答下列问题:
(2)D、E和J三种元素的离子半径由大到小的顺序是
(3)图中对应元素最高价氧化物的水化物中,碱性最强的是
(4)A、C和J三种元素能形成多种化合物,其中酸性最强的化合物的化学式是
(5)元素F的单质与元素E的最高价氧化物对应水化物反应的离子方程式为
(6)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是_____(填字母)。

| A.若a、b、c表示第ⅦA族元素,则X表示对应气态氢化物的沸点 |
| B.若a、b、c表示第ⅥA族元素,则X表示对应氢化物的稳定性 |
| C.若a、b、c表示第ⅡA族元素,则X表示最高价氧化物对应水化物的碱性 |
| D.若a、b、c表示第ⅦA族元素,则X表示对应简单离子的还原性 |
您最近一年使用:0次
名校
解题方法
4 . 下列五种有机物:①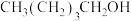 ②
②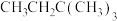 ③
③ ④
④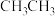 ⑤
⑤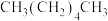 ,其沸点按由高到低的顺序排列正确的是
,其沸点按由高到低的顺序排列正确的是
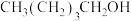 ②
②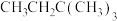 ③
③ ④
④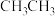 ⑤
⑤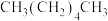 ,其沸点按由高到低的顺序排列正确的是
,其沸点按由高到低的顺序排列正确的是| A.①⑤②③④ | B.②③④⑤① | C.⑤②①③④ | D.④①②⑤③ |
您最近一年使用:0次
2023-06-30更新
|
751次组卷
|
3卷引用:湖北省武汉外国语学校2022-2023学年高一下学期期末考试化学试题
名校
5 . 下列有关化学用语正确的是
| A.金刚砂的分子式:SiC |
B. 的空间结构模型与VSEPR模型都是平面三角形 的空间结构模型与VSEPR模型都是平面三角形 |
C.邻羟基苯甲醛分子内氢键示意图: |
D.O3分子的球棍模型: |
您最近一年使用:0次
6 . X、Y、Z、W为原子序数依次增大的短周期主族元素,其中X、Y相邻,Y是地壳中含量最高的元素,Z的原子半径在短周期元素中最大,W形成的单质可用于自来水消毒。下列说法错误的是
A.最简单氢化物的熔沸点: | B.简单离子半径: |
C. 的最高价氧化物对应的水化物为强酸 的最高价氧化物对应的水化物为强酸 | D.X、Y按原子个数比1∶1组成的化合物为无色气体 |
您最近一年使用:0次
2023-06-27更新
|
79次组卷
|
3卷引用:湖北省十堰市2022-2023学年高一下学期期末调研考试化学试题
名校
7 . 硒(Se)是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光(AIE)效应以来,AIE在发光材料、生物医学等领域引起广泛关注。一种含Se的新型AIE分子Ⅳ的合成路线如下:
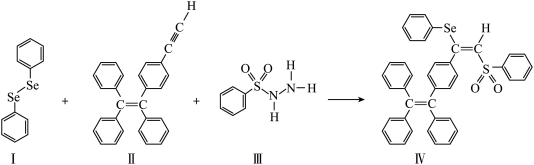
(1)Se与S同主族,Se在元素周期表中的位置为___________ ,用电子式写出 的形成过程
的形成过程___________ 。
(2) 是一种有恶臭的气体,常作半导体用料。与
是一种有恶臭的气体,常作半导体用料。与 相比,沸点
相比,沸点
___________  (填“>”或“<”,下同),原因是
(填“>”或“<”,下同),原因是___________ ;热稳定性:
___________  。
。
(3)研究发现,给小鼠喂食适量硒酸钠( )可减轻重金属㸰引起的中毒。Na、Se、O形成的简单离子的半径由大到小的顺序为
)可减轻重金属㸰引起的中毒。Na、Se、O形成的简单离子的半径由大到小的顺序为___________ 。
(4)反应物Ⅲ的局部结构与肼( )十分相似,
)十分相似, 与
与 性质十分相似,肼可与过量的硫酸反应生成酸式盐,该酸式盐化学式为
性质十分相似,肼可与过量的硫酸反应生成酸式盐,该酸式盐化学式为___________ ,以为原料合成的液体火箭燃料偏二甲肼( ),偏二甲肼与液态氧化剂
),偏二甲肼与液态氧化剂 接触立刻反应,产生大量无害气体,放出巨大能量,把火箭送上天空,该反应的化学方程式为
接触立刻反应,产生大量无害气体,放出巨大能量,把火箭送上天空,该反应的化学方程式为___________ ,已知1g偏二甲肼发生此反应发出42.5KJ热量,则该反应的反应热为___________ 。

(1)Se与S同主族,Se在元素周期表中的位置为
 的形成过程
的形成过程(2)
 是一种有恶臭的气体,常作半导体用料。与
是一种有恶臭的气体,常作半导体用料。与 相比,沸点
相比,沸点
 (填“>”或“<”,下同),原因是
(填“>”或“<”,下同),原因是
 。
。(3)研究发现,给小鼠喂食适量硒酸钠(
 )可减轻重金属㸰引起的中毒。Na、Se、O形成的简单离子的半径由大到小的顺序为
)可减轻重金属㸰引起的中毒。Na、Se、O形成的简单离子的半径由大到小的顺序为(4)反应物Ⅲ的局部结构与肼(
 )十分相似,
)十分相似, 与
与 性质十分相似,肼可与过量的硫酸反应生成酸式盐,该酸式盐化学式为
性质十分相似,肼可与过量的硫酸反应生成酸式盐,该酸式盐化学式为 ),偏二甲肼与液态氧化剂
),偏二甲肼与液态氧化剂 接触立刻反应,产生大量无害气体,放出巨大能量,把火箭送上天空,该反应的化学方程式为
接触立刻反应,产生大量无害气体,放出巨大能量,把火箭送上天空,该反应的化学方程式为
您最近一年使用:0次
名校
解题方法
8 . 回答下列关于氮族元素的问题:
(1)位于第五周期的元素符号和名称分别为_______ 、_______ 。铋(Bi)的最高正化合价为_______ 。
(2)①热稳定性:NH3_______ PH3(填“>”或“<”)。
②沸点:N2H4_______ P2H4(填“>”或“<”),判断依据是_______ 。
③化合物NH2NH2的电子式为_______ ,其分子内存在的共价键类型有_______
④磷能呈现多种化合价,其中+3价氧化物为10原子分子,该氧化物的分子式为_______ ,+5价简单含氧酸的分子式为_______ 。
(3)PH3与卤化氢的反应和NH3与卤化氢的反应相似,产物的结构和性质也相似。下列对PH3与HI反应产物的推断正确的是_______ (填序号)。
a.能与NaOH反应 b.含离子键、共价键 c.受热可分解
(1)位于第五周期的元素符号和名称分别为
(2)①热稳定性:NH3
②沸点:N2H4
③化合物NH2NH2的电子式为
④磷能呈现多种化合价,其中+3价氧化物为10原子分子,该氧化物的分子式为
(3)PH3与卤化氢的反应和NH3与卤化氢的反应相似,产物的结构和性质也相似。下列对PH3与HI反应产物的推断正确的是
a.能与NaOH反应 b.含离子键、共价键 c.受热可分解
您最近一年使用:0次
名校
9 . 下列关于物质的结构或性质的描述及解释都正确的是
A.键角: ,是由于 ,是由于 中O上孤电子对数比 中O上孤电子对数比 分中O上的少 分中O上的少 |
| B.沸点:对羟基苯甲醛>邻羟基苯甲醛,是由于对羟基苯甲醛分子间范德华力更强 |
C.稳定性: ,是由于水分子间存在氢键 ,是由于水分子间存在氢键 |
D.酸性: ,是由于 ,是由于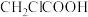 的羧基中羟基极性更小 的羧基中羟基极性更小 |
您最近一年使用:0次
2023-01-10更新
|
1691次组卷
|
8卷引用:湖北省华中师范大学第一附属中学2022-2023学年高一下学期期末考试化学试题
名校
解题方法
10 . 下列说法不正确的是
①N2H4分子中既含极性键又含非极性键
②若R2-和M+的电子层结构相同,则原子序数:R>M
③F2、Cl2、Br2、I2熔点随相对分子质量的增大而升高
④NCl3、PCl3、CO2、CS2分子中各原子均达到8e-稳定结构
⑤固体熔化成液体的过程是物理变化,所以不会破坏化学键
⑥HF分子很稳定是由于HF分子之间能形成氢键
⑦由于非金属性:Cl>Br>I,所以酸性:HCl>HBr>HI
①N2H4分子中既含极性键又含非极性键
②若R2-和M+的电子层结构相同,则原子序数:R>M
③F2、Cl2、Br2、I2熔点随相对分子质量的增大而升高
④NCl3、PCl3、CO2、CS2分子中各原子均达到8e-稳定结构
⑤固体熔化成液体的过程是物理变化,所以不会破坏化学键
⑥HF分子很稳定是由于HF分子之间能形成氢键
⑦由于非金属性:Cl>Br>I,所以酸性:HCl>HBr>HI
| A.②⑤⑥⑦ | B.①③⑤ | C.②④⑤ | D.③⑤⑦ |
您最近一年使用:0次
2022-12-10更新
|
207次组卷
|
21卷引用:湖北省黄冈市黄梅国际育才高级中学2019-2020学年高一下学期期中考试化学试题
湖北省黄冈市黄梅国际育才高级中学2019-2020学年高一下学期期中考试化学试题成都外国语学校2017-2018学年高一下学期期中考试化学试题辽宁省实验中学2017-2018学年高一下学期期末考试化学试题湖北省黄石市第二中学2019--2020学年高二下学期5月考试化学试题黑龙江省大庆第一中学2019-2020学年高一下学期期末考试化学试题辽宁省瓦房店市高级中学2019-2020学年高一下学期期末考试化学试题河南省新乡市辉县市第二高级中学2019-2020学年高一下学期第一次月考化学试题(B部)河南省新乡市辉县市第二高级中学2019-2020学年高一下学期第一次月考试化学试题(A部)苏教版(2020)高一必修第一册专题5 总结检测人教版(2019)高一必修第一册 第四章素养检测黑龙江省哈尔滨市第六中学2020-2021学年高一下学期线下开学考试化学试题陕西省西安市长安区第一中学2021-2022学年高一下学期第一次月考化学试题黑龙江牡丹江农管局密山农垦子弟学校2021-2022学年高一上学期期末考试化学试题黑龙江省大庆市实验中学实验二部2023-2024学年高一下学期开学考试化学试题河北省石家庄市第二中学2023-2024学年高一下学期学情调研化学试题【全国百强校】黑龙江省牡丹江市第一高级中学2018-2019学年高二下学期期中考试化学试题(已下线)第35讲 分子结构与性质-2021年高考化学一轮复习名师精讲练辽宁省沈阳市辽宁省实验中学2020届高三上学期期中考试化学试题湖南省娄底市双峰县第一中学2020-2021学年高二上学期9月入学考试化学试题四川省威远中学2020-2021学年高二上学期第一次月考化学试题(已下线)第8单元 原子结构 元素周期律(A卷 基础过关检测)-2021年高考化学一轮复习单元滚动双测卷



