解题方法
1 . 根据题意回答下列问题
(1)利用价层电子对互斥理论预测分子的构型或VSEPR模型
① 的分子的构型
的分子的构型___________ ;
② 模型
模型___________ 。
(2)水的沸点比氨气___________ (填“低”或“高”),原因是___________ 。
(3)当0原子的价层电子排布为 该电子排布图违背了
该电子排布图违背了___________ ;当P原子的价电子排布式由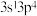 转变为
转变为 时,产生
时,产生___________ 光谱。
(4)硫酸亚铁不稳定在空气放置一段时间后生成硫酸铁,铁离子稳定的原因___________ 。
(1)利用价层电子对互斥理论预测分子的构型或VSEPR模型
①
 的分子的构型
的分子的构型②
 模型
模型(2)水的沸点比氨气
(3)当0原子的价层电子排布为
 该电子排布图违背了
该电子排布图违背了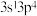 转变为
转变为 时,产生
时,产生(4)硫酸亚铁不稳定在空气放置一段时间后生成硫酸铁,铁离子稳定的原因
您最近一年使用:0次
名校
2 . VA族的氮、磷、砷(As)等元素的化合物在科研和生产中有许多重要用途,请回答下列问题。
(1)砷的基态原子的电子排布式为___________________ 。
(2)原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,N、P、As原子的第一电离能由大到小的顺序为______________ 。
(3)NH3的沸点比PH3高,原因是___________ ;PO43-离子的立体构型为___________ 。
(4)AsH3是无色稍有大蒜气味的气体,在AsH3中As原子的杂化轨道类型为______________ 。
(5)H3AsO4和H3AsO3是砷的两种含氧酸,请根据结构与性质的关系,解释H3AsO4比H3AsO3 酸性强的原因_____________________ 。
(6)磷的一种单质白磷(P4)属于分子晶体,其晶胞结构如下图。已知最近两个白磷分子间的距离为 a pm(1pm=10-12m),阿伏伽德罗常数的值为NA,则该晶体的密度为__________________ g/cm3(只要求列算式,不必计算)。
(1)砷的基态原子的电子排布式为
(2)原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离子所需要的最低能量,N、P、As原子的第一电离能由大到小的顺序为
(3)NH3的沸点比PH3高,原因是
(4)AsH3是无色稍有大蒜气味的气体,在AsH3中As原子的杂化轨道类型为
(5)H3AsO4和H3AsO3是砷的两种含氧酸,请根据结构与性质的关系,解释H3AsO4比H3AsO3 酸性强的原因
(6)磷的一种单质白磷(P4)属于分子晶体,其晶胞结构如下图。已知最近两个白磷分子间的距离为 a pm(1pm=10-12m),阿伏伽德罗常数的值为NA,则该晶体的密度为

您最近一年使用:0次
2019-01-19更新
|
611次组卷
|
2卷引用:【全国百强校】西藏自治区拉萨中学2019届高三上学期第五次月考理科综合化学试题



