解题方法
1 . 回答下列问题:
(1)麻醉剂的发现和使用是人类医学史上一项了不起的成就。一种常用麻醉剂氯仿常因保存不慎而被氧化,产生剧毒光气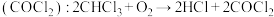 ,光气
,光气 分子的立体构型是
分子的立体构型是________ 形。
(2)某有机物的结构简式为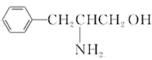 。该有机物分子是
。该有机物分子是____________ (填“极性”或“非极性”)分子,该有机物分子中采取 杂化的原子对应元素的电负性由大到小的顺序为
杂化的原子对应元素的电负性由大到小的顺序为____________ 。
(3)乙二胺 分子中氮原子杂化类型为
分子中氮原子杂化类型为_________________ 。
(4)叠氮化合物是一类重要的化合物,其中氢叠氮酸( )是一种弱酸,其分子结构可表示为
)是一种弱酸,其分子结构可表示为 ,肼
,肼 被亚硝酸氧化时便可得到氢叠氮酸
被亚硝酸氧化时便可得到氢叠氮酸 ,发生的反应为
,发生的反应为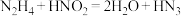 。
。 的酸性和醋酸相近,可微弱电离出
的酸性和醋酸相近,可微弱电离出 和
和 。
。
①叠氮酸根能与许多金属离子等形成配合物,如 ,根据价层电子对互斥理论判断
,根据价层电子对互斥理论判断 的空间构型为
的空间构型为________________ 。
②下列有关说法正确的是_____________ (填序号)。
A. 中含有5个
中含有5个 键
键
B. 中的三个氮原子均采用
中的三个氮原子均采用 杂化
杂化
C. 、
、 、
、 、
、 都是极性分子
都是极性分子
D.肼 的沸点高达
的沸点高达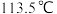 ,说明肼分子间可形成氢键
,说明肼分子间可形成氢键
(1)麻醉剂的发现和使用是人类医学史上一项了不起的成就。一种常用麻醉剂氯仿常因保存不慎而被氧化,产生剧毒光气
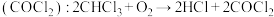 ,光气
,光气 分子的立体构型是
分子的立体构型是(2)某有机物的结构简式为
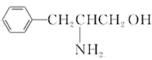 。该有机物分子是
。该有机物分子是 杂化的原子对应元素的电负性由大到小的顺序为
杂化的原子对应元素的电负性由大到小的顺序为(3)乙二胺
 分子中氮原子杂化类型为
分子中氮原子杂化类型为(4)叠氮化合物是一类重要的化合物,其中氢叠氮酸(
 )是一种弱酸,其分子结构可表示为
)是一种弱酸,其分子结构可表示为 ,肼
,肼 被亚硝酸氧化时便可得到氢叠氮酸
被亚硝酸氧化时便可得到氢叠氮酸 ,发生的反应为
,发生的反应为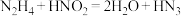 。
。 的酸性和醋酸相近,可微弱电离出
的酸性和醋酸相近,可微弱电离出 和
和 。
。①叠氮酸根能与许多金属离子等形成配合物,如
 ,根据价层电子对互斥理论判断
,根据价层电子对互斥理论判断 的空间构型为
的空间构型为②下列有关说法正确的是
A.
 中含有5个
中含有5个 键
键B.
 中的三个氮原子均采用
中的三个氮原子均采用 杂化
杂化C.
 、
、 、
、 、
、 都是极性分子
都是极性分子D.肼
 的沸点高达
的沸点高达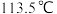 ,说明肼分子间可形成氢键
,说明肼分子间可形成氢键
您最近一年使用:0次
解题方法
2 . 回答下列问题
(1)在 分子中,CO
分子中,CO 的价层电子对的空间构型为
的价层电子对的空间构型为___________ ,以极性键相结合,具有正四面体结构的分子是___________ ,以极性键相结合,具有三角锥形结构的分子是___________ ,以极性键相结合,具有V形结构的分子是___________ 。
(2)元素As与N同族。预测As的氢化物分子的空间结构为___________ ,其沸点比NH3的___________ (填“高”或“低”),其判断理由是___________ 。
(1)在
 分子中,CO
分子中,CO 的价层电子对的空间构型为
的价层电子对的空间构型为(2)元素As与N同族。预测As的氢化物分子的空间结构为
您最近一年使用:0次
名校
3 . 完成下列问题。
(1)硅是重要的半导体材料,构成了现代电子工业的基础。碳和硅的有关化学键键能如表所示,简要分析和解释下列有关事实:
硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多,原因是___________ 。SiH4的稳定性小于CH4,更易生成氧化物,原因是___________ 。
(2)比较NH3和[Cu(NH3)4]2+中H−N−H键角的大小:NH3___________ [Cu(NH3)4]2+(填“>”或“<”),并说明理由:___________
(3)Xe是第五周期的稀有气体元素,与F形成的XeF2室温下易升华。XeF2中心原子的价层电子对数为_______ ,下列对XeF2中心原子杂化方式推断合理的是_______ (填标号)。
A.sp B.sp2 C.sp3 D.sp3d
(4)苯胺( )与甲苯(
)与甲苯(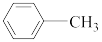 )的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是
)的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是_______ 。
(5)硒的两种含氧酸的酸分别为 、
、 ,试比较其酸性强弱并说明原因:
,试比较其酸性强弱并说明原因:___________ 。
(6)在水中的溶解度,吡啶(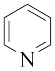 )远大于苯,主要原因是①
)远大于苯,主要原因是①_______ ,②_______ 。
(1)硅是重要的半导体材料,构成了现代电子工业的基础。碳和硅的有关化学键键能如表所示,简要分析和解释下列有关事实:
| 化学键 | C−C | C−H | C−O | Si−Si | Si−H | Si−O |
| 键能/ (kJ·mol-1) | 365 | 413 | 336 | 226 | 318 | 452 |
(2)比较NH3和[Cu(NH3)4]2+中H−N−H键角的大小:NH3
(3)Xe是第五周期的稀有气体元素,与F形成的XeF2室温下易升华。XeF2中心原子的价层电子对数为
A.sp B.sp2 C.sp3 D.sp3d
(4)苯胺(
 )与甲苯(
)与甲苯(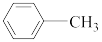 )的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是
)的相对分子质量相近,但苯胺的熔点(-5.9℃)、沸点(184.4℃)分别高于甲苯的熔点(-95.0℃)、沸点(110.6℃),原因是(5)硒的两种含氧酸的酸分别为
 、
、 ,试比较其酸性强弱并说明原因:
,试比较其酸性强弱并说明原因:(6)在水中的溶解度,吡啶(
 )远大于苯,主要原因是①
)远大于苯,主要原因是①
您最近一年使用:0次
解题方法
4 . 请按要求回答下列问题:
(1)符号“3px”没有给出的信息是___________。
(2)某元素基态原子4s轨道上有1个电子,则该元素基态原子价电子排布不可能是___________。
(3)X元素的原子最外层电子排布式为(n+1)sn(n+1)pn+1,则X的氢化物的化学式是___________。
(4)下列比较正确的是___________ 。
A.酸性:H3PO4<H3AsO4 B.键角:H2O<NH3 C.离子半径:r(Al3+)>r(O2-)
(5)下列实验事实不能用氢键来解释的是___________。
(1)符号“3px”没有给出的信息是___________。
| A.能层 | B.能级 | C.电子云在空间的伸展方向 | D.电子的自旋方向 |
| A.4s1 | B.3p64s1 | C.3d54s1 | D.3d104s1 |
| A.HX | B.H2X | C.XH3 | D.XH4 |
A.酸性:H3PO4<H3AsO4 B.键角:H2O<NH3 C.离子半径:r(Al3+)>r(O2-)
(5)下列实验事实不能用氢键来解释的是___________。
| A.CH4比SiH4稳定 |
| B.乙醇能与水以任意比互溶 |
| C.邻羟基苯甲醛的沸点低于对羟基苯甲醛 |
| D.接近沸点的水蒸气的相对分子质量测量值大于18 |
您最近一年使用:0次
名校
5 . 二氟草酸硼酸锂 是新型锂离子电池电解质,乙酸锰
是新型锂离子电池电解质,乙酸锰 可用于制造离子电池的负极材料。合成方程式如下:
可用于制造离子电池的负极材料。合成方程式如下: 、
、
(1)基态 原子的核外电子排布式为
原子的核外电子排布式为___________ , 原子的价电子排布图为:
原子的价电子排布图为:___________ 。
(2)草酸 分子中碳原子轨道的杂化类型是
分子中碳原子轨道的杂化类型是___________ , 草酸分子中含有
草酸分子中含有 键的数目为
键的数目为___________ 。
(3)与 互为等电子体的两种阴离子的化学式为
互为等电子体的两种阴离子的化学式为___________ 。
(4) 易溶于水,除了它是极性分子外,还因为
易溶于水,除了它是极性分子外,还因为___________ 。
(5)向硫酸铜溶液中加入过量氨水,可生成 配离子。已知
配离子。已知 与
与 的空间构型都是三角锥形,但
的空间构型都是三角锥形,但 不易与
不易与 形成配离子的原因是
形成配离子的原因是___________ 。
 是新型锂离子电池电解质,乙酸锰
是新型锂离子电池电解质,乙酸锰 可用于制造离子电池的负极材料。合成方程式如下:
可用于制造离子电池的负极材料。合成方程式如下: 、
、
(1)基态
 原子的核外电子排布式为
原子的核外电子排布式为 原子的价电子排布图为:
原子的价电子排布图为:(2)草酸
 分子中碳原子轨道的杂化类型是
分子中碳原子轨道的杂化类型是 草酸分子中含有
草酸分子中含有 键的数目为
键的数目为(3)与
 互为等电子体的两种阴离子的化学式为
互为等电子体的两种阴离子的化学式为(4)
 易溶于水,除了它是极性分子外,还因为
易溶于水,除了它是极性分子外,还因为(5)向硫酸铜溶液中加入过量氨水,可生成
 配离子。已知
配离子。已知 与
与 的空间构型都是三角锥形,但
的空间构型都是三角锥形,但 不易与
不易与 形成配离子的原因是
形成配离子的原因是
您最近一年使用:0次
名校
解题方法
6 . 太阳能的开发利用在新能源研究中占据重要地位,单晶硅太阳能电池片在加工时,一般掺杂微量的铜、钴、硼、镓、硒等。已知铜的配合物A结构如图。请回答下列问题:

(1)基态二价铜离子的电子排布式为_________ ,已知高温下Cu2O比CuO更稳定,试从核外电子排布角度解释_________ 。
(2)配体氨基乙酸根(H2NCH2COO-)受热分解可产生CO2和N2,N2中σ键和π键数目之比是_________ ;N2O与CO2互为等电子体,则N2O的电子式为_________ 。
(3)铜与(SCN)2反应生成Cu(SCN)2,1mol(SCN)2中含有π键的数目为_________ (用NA表示),HSCN结构有两种,硫氰酸(H—S—C≡N)的沸点低于异硫氰酸(H—N=C=S)的原因是_________ 。
(4)六方氮化硼晶体结构与石墨晶体相似,层间相互作用力为_________ 。六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构、硬度与金刚石相似,其晶胞如图,晶胞边长为361.5pm,立方氮化硼的密度是_________ g·cm-3(只列算式,NA为阿伏加德罗常数的值)。

(5)关于两种晶体的说法正确的是_________ (填序号)。
a.立方相氮化硼含有σ键和π键,所以硬度大
b.六方相氮化硼层间作用力小,所以质地软
c.两种晶体中的B-N键均为共价键
d.两种晶体均为分子晶体

(1)基态二价铜离子的电子排布式为
(2)配体氨基乙酸根(H2NCH2COO-)受热分解可产生CO2和N2,N2中σ键和π键数目之比是
(3)铜与(SCN)2反应生成Cu(SCN)2,1mol(SCN)2中含有π键的数目为
(4)六方氮化硼晶体结构与石墨晶体相似,层间相互作用力为

(5)关于两种晶体的说法正确的是
a.立方相氮化硼含有σ键和π键,所以硬度大
b.六方相氮化硼层间作用力小,所以质地软
c.两种晶体中的B-N键均为共价键
d.两种晶体均为分子晶体
您最近一年使用:0次
名校
7 . VIA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含VIA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题:
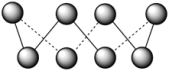
(1)S单质的常见形式为S8,其环状结构如图所示,S原子采用的轨道杂化方式是_______ 。
(2)比较酸性:H2SeO4_______ H2SeO3(填“>”、“<”或“=”)。
(3)气态SeO3分子的立体构型为_______ ,  离子的VSEPR模型为
离子的VSEPR模型为_______ 。
(4)H2Se、H2S、H2O的沸点由高到低的顺序是_______ ,原因是_______ 。
(5)H+可与H2O形成H3O+,H3O+中H-O-H键角比H2O中H-O-H键角大,原因是_______ 。
(1)S单质的常见形式为S8,其环状结构如图所示,S原子采用的轨道杂化方式是

(2)比较酸性:H2SeO4
(3)气态SeO3分子的立体构型为
 离子的VSEPR模型为
离子的VSEPR模型为(4)H2Se、H2S、H2O的沸点由高到低的顺序是
(5)H+可与H2O形成H3O+,H3O+中H-O-H键角比H2O中H-O-H键角大,原因是
您最近一年使用:0次
2022-10-04更新
|
485次组卷
|
3卷引用:陕西省西安市阎良区关山中学2021-2022学年高二下学期第三次质量检测化学试题
陕西省西安市阎良区关山中学2021-2022学年高二下学期第三次质量检测化学试题山东省昌乐第一中学2022-2023学年高二下学期第一次月考化学试题(已下线)第05讲 分子结构与物质的性质-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)
名校
8 . VIA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含VIA族元素的化合物在研究和生产中有许多重要用途。请回答下列问题:
(1)S单质的常见形式为S8,其环状结构如图所示,S原子采用的轨道杂化方式是_______ 。

(2)Se原子序数为_______ ,其核外M层电子的排布式为_______ 。
(3)O、S、Se原子的第一电离能由大到小的顺序为_______ 。
(4)比较酸性:H2SeO4_______ H2SeO3(填“>”、“<”或“=”),理由是:_______ 。
(5)气态SeO3分子的立体构型为_______ ,  离子的VSEPR模型为
离子的VSEPR模型为_______ 。
(6)H2Se、H2S、H2O的稳定性由强到弱的顺序是_______ ,原因是_______ (用共价键理论解释)。H2Se、H2S、H2O的沸点由高到低的顺序是_______ ,原因是_______ 。
(7)H+可与H2O形成H3O+,H3O+中H-O-H键角比H2O中H-O-H键角大,原因是_______ 。
(1)S单质的常见形式为S8,其环状结构如图所示,S原子采用的轨道杂化方式是

(2)Se原子序数为
(3)O、S、Se原子的第一电离能由大到小的顺序为
(4)比较酸性:H2SeO4
(5)气态SeO3分子的立体构型为
 离子的VSEPR模型为
离子的VSEPR模型为(6)H2Se、H2S、H2O的稳定性由强到弱的顺序是
(7)H+可与H2O形成H3O+,H3O+中H-O-H键角比H2O中H-O-H键角大,原因是
您最近一年使用:0次
9 . 2020年6月,比亚迪正式发布刀片电池,大幅度提高了电动汽车的续航里程,媒体称其可媲美特斯拉。刀片电池主要材料为磷酸铁锂技术,文献表明磷酸铁锂可采用 、
、 、
、 和苯胺等作为原料制备。回答下列问题:
和苯胺等作为原料制备。回答下列问题:
(1)回答下列各题:
①元素周期表中,和 性质最相似的元素是
性质最相似的元素是_______ 。(填元素符号)
②试比较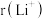
_______ 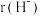 。(填“>”、“<”或“=”)
。(填“>”、“<”或“=”)
(2)苯胺与甲苯( )的相对分子质量相近,但苯胺的沸点(
)的相对分子质量相近,但苯胺的沸点( )高于甲苯的沸点(
)高于甲苯的沸点( ),原因是
),原因是_______ 。
(3)结合核外电子排布分析,基态 与
与 中更稳定的是
中更稳定的是 ,原因是
,原因是_______ 。
(4)回答下列各题:
① 中,电负性最高的元素是
中,电负性最高的元素是_______ ;P的_______ 杂化轨道与O的 轨道形成
轨道形成_______ 键。
② 和
和 ,属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如图所示:
,属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如图所示:

这类磷酸根离子的化学式可用通式表示为_______ (用n代表P原子数)。
 、
、 、
、 和苯胺等作为原料制备。回答下列问题:
和苯胺等作为原料制备。回答下列问题:(1)回答下列各题:
①元素周期表中,和
 性质最相似的元素是
性质最相似的元素是②试比较
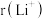
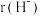 。(填“>”、“<”或“=”)
。(填“>”、“<”或“=”)(2)苯胺与甲苯(
 )的相对分子质量相近,但苯胺的沸点(
)的相对分子质量相近,但苯胺的沸点( )高于甲苯的沸点(
)高于甲苯的沸点( ),原因是
),原因是(3)结合核外电子排布分析,基态
 与
与 中更稳定的是
中更稳定的是 ,原因是
,原因是(4)回答下列各题:
①
 中,电负性最高的元素是
中,电负性最高的元素是 轨道形成
轨道形成②
 和
和 ,属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如图所示:
,属于简单磷酸盐,而直链的多磷酸盐则是一种复杂磷酸盐,如:焦磷酸钠、三磷酸钠等。焦磷酸根离子、三磷酸根离子如图所示:
这类磷酸根离子的化学式可用通式表示为
您最近一年使用:0次
10 . 按要求完成下列各题
(1)气态氢化物热稳定性 大于
大于 的主要原因是
的主要原因是___________ 。
(2)常温下,在水中的溶解度乙醇大于氯乙烷,原因是___________ 。
(3)过氧化钠的电子式是___________ 。
(4) 溶液显碱性的原因是(用离子方程式说明)
溶液显碱性的原因是(用离子方程式说明)___________ 。
(5)已知葡萄糖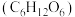 的燃烧热为
的燃烧热为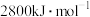 ,试写出葡萄糖燃烧的热化学方程式
,试写出葡萄糖燃烧的热化学方程式___________ 。
(1)气态氢化物热稳定性
 大于
大于 的主要原因是
的主要原因是(2)常温下,在水中的溶解度乙醇大于氯乙烷,原因是
(3)过氧化钠的电子式是
(4)
 溶液显碱性的原因是(用离子方程式说明)
溶液显碱性的原因是(用离子方程式说明)(5)已知葡萄糖
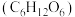 的燃烧热为
的燃烧热为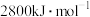 ,试写出葡萄糖燃烧的热化学方程式
,试写出葡萄糖燃烧的热化学方程式
您最近一年使用:0次



