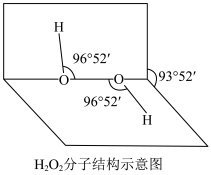
1 . H2O2是常用的氧化剂,其分子结构如图所示,两个氢原子犹如在半展开的书的两面上。H2O2的电子式是___________ ,结构式是___________ 。含有___________ 键和___________ 键的___________ 分子(填“极性”或“非极性”)。H2O2能与水混溶,却不溶于CCl4。请予以解释:___________ 。
您最近一年使用:0次
解题方法
2 . 青蒿素(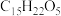 )是治疗疟疾的有效药物,白色针状晶体,溶于乙醇和乙醚,对热不稳定。青蒿素晶胞(长方体,含4个青蒿素分子)及分子结构如下图所示。
)是治疗疟疾的有效药物,白色针状晶体,溶于乙醇和乙醚,对热不稳定。青蒿素晶胞(长方体,含4个青蒿素分子)及分子结构如下图所示。
在浸取、蒸馏过程中,发现用沸点比乙醇低的乙醚( )提取,效果更好。
)提取,效果更好。
①乙醚沸点低于乙醇,原因是___________ 。
②用乙醚提取效果更好,原因是___________ 。
(2)确定结构
①测量晶胞中各处电子云密度大小,可确定原子的位置、种类。比较青蒿素分子中 、
、 、
、 的原子核附近电子云密度大小:
的原子核附近电子云密度大小:___________ 。
②图中晶胞的棱长分别为 、
、 、
、 ,晶体的密度为
,晶体的密度为___________  。(用
。(用 表示阿伏加德罗常数;
表示阿伏加德罗常数; ;青蒿素的相对分子质量为282)
;青蒿素的相对分子质量为282)
③能确定晶体中哪些原子间存在化学键、并能确定键长和键角,从而得出分子空间结构的一种方法是___________ 。
a.质谱法 b.X射线衍射 c.核磁共振氢谱 d.红外光谱
(3)修饰结构,提高疗效
一定条件下,用 将青蒿素选择性还原生成双氢青蒿素。
将青蒿素选择性还原生成双氢青蒿素。___________ 。
② 的空间结构为
的空间结构为___________ 。
③青蒿素与双氢青蒿素中相同的官能团是___________ 和___________ 。
双氢青蒿素比青蒿素水溶性更好,治疗疟疾的效果更好。
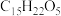 )是治疗疟疾的有效药物,白色针状晶体,溶于乙醇和乙醚,对热不稳定。青蒿素晶胞(长方体,含4个青蒿素分子)及分子结构如下图所示。
)是治疗疟疾的有效药物,白色针状晶体,溶于乙醇和乙醚,对热不稳定。青蒿素晶胞(长方体,含4个青蒿素分子)及分子结构如下图所示。
在浸取、蒸馏过程中,发现用沸点比乙醇低的乙醚(
 )提取,效果更好。
)提取,效果更好。①乙醚沸点低于乙醇,原因是
②用乙醚提取效果更好,原因是
(2)确定结构
①测量晶胞中各处电子云密度大小,可确定原子的位置、种类。比较青蒿素分子中
 、
、 、
、 的原子核附近电子云密度大小:
的原子核附近电子云密度大小:②图中晶胞的棱长分别为
 、
、 、
、 ,晶体的密度为
,晶体的密度为 。(用
。(用 表示阿伏加德罗常数;
表示阿伏加德罗常数; ;青蒿素的相对分子质量为282)
;青蒿素的相对分子质量为282)③能确定晶体中哪些原子间存在化学键、并能确定键长和键角,从而得出分子空间结构的一种方法是
a.质谱法 b.X射线衍射 c.核磁共振氢谱 d.红外光谱
(3)修饰结构,提高疗效
一定条件下,用
 将青蒿素选择性还原生成双氢青蒿素。
将青蒿素选择性还原生成双氢青蒿素。
②
 的空间结构为
的空间结构为③青蒿素与双氢青蒿素中相同的官能团是
双氢青蒿素比青蒿素水溶性更好,治疗疟疾的效果更好。
您最近一年使用:0次
名校
3 .  的资源化利用是解决温室效应的重要途径。科学家致力于
的资源化利用是解决温室效应的重要途径。科学家致力于 与
与 反应制
反应制 的研究。
的研究。
(1) 分子中碳原子的杂化轨道类型为
分子中碳原子的杂化轨道类型为________ ;干冰是很好的致冷剂,干冰升华时, 需要克服的作用力是
需要克服的作用力是________ 。
(2) 所含有的三种元素电负性从大到小的顺序为
所含有的三种元素电负性从大到小的顺序为________ (用元素符号表示)。
(3) 被氧化为
被氧化为 ,
, 继续被氧化可生成
继续被氧化可生成 。
。 分子的空间结构为
分子的空间结构为________ , 分子内
分子内 键与
键与 键个数之比为
键个数之比为________ 。
(4) 沸点远远高于乙烷,原因是
沸点远远高于乙烷,原因是________ 。
 的资源化利用是解决温室效应的重要途径。科学家致力于
的资源化利用是解决温室效应的重要途径。科学家致力于 与
与 反应制
反应制 的研究。
的研究。(1)
 分子中碳原子的杂化轨道类型为
分子中碳原子的杂化轨道类型为 需要克服的作用力是
需要克服的作用力是(2)
 所含有的三种元素电负性从大到小的顺序为
所含有的三种元素电负性从大到小的顺序为(3)
 被氧化为
被氧化为 ,
, 继续被氧化可生成
继续被氧化可生成 。
。 分子的空间结构为
分子的空间结构为 分子内
分子内 键与
键与 键个数之比为
键个数之比为(4)
 沸点远远高于乙烷,原因是
沸点远远高于乙烷,原因是
您最近一年使用:0次
名校
4 . 回答下列问题。
(1)基态Mn原子核外未成对电子有________ 个。
(2) 与
与 具有相同的电子构型,
具有相同的电子构型, 小于
小于 ,原因是
,原因是________ 。
(3) 是有机合成中常用的还原剂,
是有机合成中常用的还原剂, 中的阴离子空间结构是
中的阴离子空间结构是________ , 中,存在
中,存在________ (填标号)。
A.离子键 B.σ键 C.π键 D.氢键
(4)X射线衍射测定发现, 中存在
中存在 离子,
离子, 离子的空间结构为
离子的空间结构为________ ;反应 中,
中, 中心原子的杂化为
中心原子的杂化为________ 。
A. B.
B. C.
C.
(5)在 低压合成甲醇反应(
低压合成甲醇反应(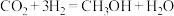 )所涉及的4种物质中,沸点从高到低的顺序为
)所涉及的4种物质中,沸点从高到低的顺序为________ 。
(6)乙二胺( )能与
)能与 、
、 等金属离子形成环状离子,其原因是
等金属离子形成环状离子,其原因是________ 。
(7)经X射线衍射测得化合物R的晶体结构,其局部结构如图所示。 中的σ键总数为
中的σ键总数为________ 个。分子中的大π键可用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为 ),则
),则 中的大π键应表示为
中的大π键应表示为________ 。
(1)基态Mn原子核外未成对电子有
(2)
 与
与 具有相同的电子构型,
具有相同的电子构型, 小于
小于 ,原因是
,原因是(3)
 是有机合成中常用的还原剂,
是有机合成中常用的还原剂, 中的阴离子空间结构是
中的阴离子空间结构是 中,存在
中,存在A.离子键 B.σ键 C.π键 D.氢键
(4)X射线衍射测定发现,
 中存在
中存在 离子,
离子, 离子的空间结构为
离子的空间结构为 中,
中, 中心原子的杂化为
中心原子的杂化为A.
 B.
B. C.
C.
(5)在
 低压合成甲醇反应(
低压合成甲醇反应(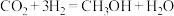 )所涉及的4种物质中,沸点从高到低的顺序为
)所涉及的4种物质中,沸点从高到低的顺序为(6)乙二胺(
 )能与
)能与 、
、 等金属离子形成环状离子,其原因是
等金属离子形成环状离子,其原因是(7)经X射线衍射测得化合物R的晶体结构,其局部结构如图所示。

 中的σ键总数为
中的σ键总数为 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为 ),则
),则 中的大π键应表示为
中的大π键应表示为
您最近一年使用:0次
解题方法
5 . 分子的结构与物质性质之间存在紧密的联系。
(1)如图是部分主族元素氢化物的沸点变化趋势_______ ,其汽化过程中克服的作用力是 _______ 。
②氢化物b、c、d的沸点均高于同族其它元素氢化物的沸点,原因是_______ 。
③H2O的沸点高于HF,预测可能的原因是_______ 。
(2)如图是冰(H2O)和干冰(CO2)的结构模型。_______ (填字母序号)。
a.冰中氢键存在方向性,晶体有较大空隙,空间利用率低
b.水分子极性强,分子间作用力大
c.二氧化碳分子的质量大于水分子
d.干冰晶胞中二氧化碳分子堆积得更密集
(3)苯胺(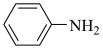 )与甲苯(
)与甲苯(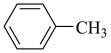 )的相对分子质量接近,但苯胺的熔点(﹣6.2℃)和沸点(184.4℃)高于甲苯的熔点(﹣95.0℃)和沸点(110.6℃),原因是
)的相对分子质量接近,但苯胺的熔点(﹣6.2℃)和沸点(184.4℃)高于甲苯的熔点(﹣95.0℃)和沸点(110.6℃),原因是 _______ 。
(1)如图是部分主族元素氢化物的沸点变化趋势
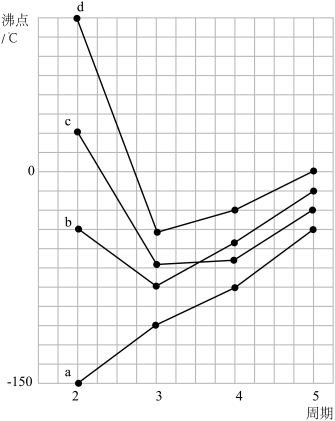
②氢化物b、c、d的沸点均高于同族其它元素氢化物的沸点,原因是
③H2O的沸点高于HF,预测可能的原因是
(2)如图是冰(H2O)和干冰(CO2)的结构模型。
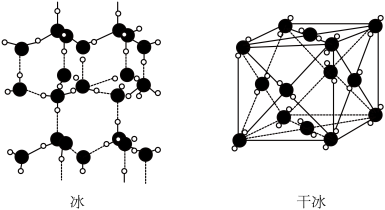
a.冰中氢键存在方向性,晶体有较大空隙,空间利用率低
b.水分子极性强,分子间作用力大
c.二氧化碳分子的质量大于水分子
d.干冰晶胞中二氧化碳分子堆积得更密集
(3)苯胺(
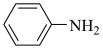 )与甲苯(
)与甲苯( )的相对分子质量接近,但苯胺的熔点(﹣6.2℃)和沸点(184.4℃)高于甲苯的熔点(﹣95.0℃)和沸点(110.6℃),原因是
)的相对分子质量接近,但苯胺的熔点(﹣6.2℃)和沸点(184.4℃)高于甲苯的熔点(﹣95.0℃)和沸点(110.6℃),原因是
您最近一年使用:0次
名校
6 . 硒(Se)是一种有抗癌、抗氧化作用的元素,可以形成多种化合物。
(1)基态硒原子的价层电子排布式为___________ ;As的第一电离能比Se的第一电离能大的原因为___________ 。
(2) 中心原子的杂化类型是:
中心原子的杂化类型是:___________ , 的立体构型是
的立体构型是___________ 。
(3) 属于
属于___________ (填“极性”或“非极性”)分子;比较 与
与 沸点高低,并说明原因:
沸点高低,并说明原因:___________ 。
(4)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为___________ ;若该晶胞密度为ρg⋅cm ,硒化锌的摩尔质量为Mg⋅mol
,硒化锌的摩尔质量为Mg⋅mol ,
, 代表阿伏加德罗常数的值,则晶胞参数(边长)a为
代表阿伏加德罗常数的值,则晶胞参数(边长)a为___________ 。
(1)基态硒原子的价层电子排布式为
(2)
 中心原子的杂化类型是:
中心原子的杂化类型是: 的立体构型是
的立体构型是(3)
 属于
属于 与
与 沸点高低,并说明原因:
沸点高低,并说明原因:(4)硒化锌(ZnSe)是一种重要的半导体材料,其晶胞结构如图所示,该晶胞中硒原子的配位数为
 ,硒化锌的摩尔质量为Mg⋅mol
,硒化锌的摩尔质量为Mg⋅mol ,
, 代表阿伏加德罗常数的值,则晶胞参数(边长)a为
代表阿伏加德罗常数的值,则晶胞参数(边长)a为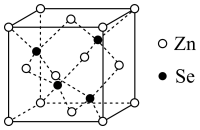
您最近一年使用:0次
2024-05-03更新
|
388次组卷
|
2卷引用:北京市大兴区第一中学2023-2024学年高二下学期3月月考化学试题
解题方法
7 . 研究发现, 低压合成甲醇的反应:
低压合成甲醇的反应: ,钴氧化物负载的锰氧化物纳米粒子催化剂具有较高的活性,有良好的应用前景。
,钴氧化物负载的锰氧化物纳米粒子催化剂具有较高的活性,有良好的应用前景。
(1) 分子和
分子和 分子中,
分子中, 原子的杂化轨道类型分别为
原子的杂化轨道类型分别为______________ 和______________ 。
(2) 和
和 中,沸点较高的是
中,沸点较高的是_____________ ,从结构角度分析,原因是______________________ 。
(3)基态锰原子的价层电子排布式为_______________ 。
(4)工业上利用甲醇空气氧化法生产甲醛(HCHO)。下列关于甲醛分子的说法正确的是____________ (填序号)。
a.碳氧双键中有一个 键,一个
键,一个 键
键
b.中心原子的孤电子对数为0
c.甲醛分子为极性分子
d.甲醛的VSEPR模型为平面三角形
 低压合成甲醇的反应:
低压合成甲醇的反应: ,钴氧化物负载的锰氧化物纳米粒子催化剂具有较高的活性,有良好的应用前景。
,钴氧化物负载的锰氧化物纳米粒子催化剂具有较高的活性,有良好的应用前景。(1)
 分子和
分子和 分子中,
分子中, 原子的杂化轨道类型分别为
原子的杂化轨道类型分别为(2)
 和
和 中,沸点较高的是
中,沸点较高的是(3)基态锰原子的价层电子排布式为
(4)工业上利用甲醇空气氧化法生产甲醛(HCHO)。下列关于甲醛分子的说法正确的是
a.碳氧双键中有一个
 键,一个
键,一个 键
键b.中心原子的孤电子对数为0
c.甲醛分子为极性分子
d.甲醛的VSEPR模型为平面三角形
您最近一年使用:0次
名校
解题方法
8 . 有机物中的( 键较难断裂,活化
键较难断裂,活化 键是有机反应研究的热点之一、由
键是有机反应研究的热点之一、由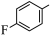 经两步反应合成
经两步反应合成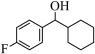 ,均需使
,均需使 键活化,步骤如下
键活化,步骤如下
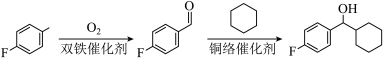
a.s区 b.d区 c.p区 d.ds区
(2)
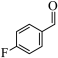 转化为
转化为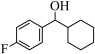 的过程中,
的过程中, 键中的
键中的 ”或“
”或“ ”)键断裂,发生加成反应,转化为
”)键断裂,发生加成反应,转化为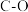 键。
键。(3)利用有机金属框架(MOF)构筑双铁催化剂,制备过程的核心结构变化如下。
注:
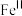 代表+2价铁,
代表+2价铁,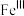 代表+3价铁。
代表+3价铁。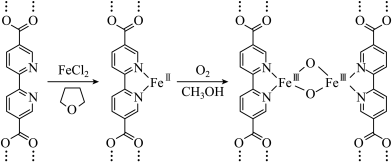
①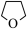 与
与 的相对分子质量相差较大,但二者的沸点却极为接近(相差1℃左右),原因有:
的相对分子质量相差较大,但二者的沸点却极为接近(相差1℃左右),原因有:
ⅰ. 的极性强于
的极性强于 ;
;
②
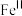 易被氧化为
易被氧化为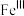 ,结合价层电子排布解释原因:
,结合价层电子排布解释原因:(4)铜铬催化剂的主要成分是CuCl、
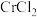 和
和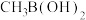 (甲基硼酸)等,
(甲基硼酸)等,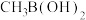 能有效抑制副产物的生成。
能有效抑制副产物的生成。①
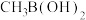 中B的杂化轨道类型是
中B的杂化轨道类型是②已知:
 和
和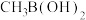 均为一元弱酸。推测
均为一元弱酸。推测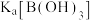
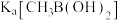 (填“>”或“<”)
(填“>”或“<”)
您最近一年使用:0次
2023-07-12更新
|
409次组卷
|
2卷引用:北京朝阳区2022-2023学年高二下学期期末考试化学试题
解题方法
9 . 对氨基苯甲酸和邻氨基苯甲酸分别用于防晒剂和制造药物,某小组以甲苯为主要原料进行合成,设计流程如下图。
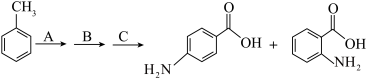
已知:i.羧基使苯环上与羧基处于间位的氢原子易被取代
ii .苯胺中的氨基易被氧化
iii.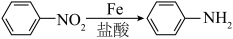
(1)基态N原子的电子有___________ 种运动状态。
(2)氨基苯甲酸中C=O中O原子的杂化方式是___________ 。
(3)组成氨基苯甲酸的4种元素的电负性由大到小的顺序是___________ 。
(4)对氨基苯甲酸和邻氨基苯甲酸的沸点分别是339.9℃和311.9℃,沸点不同的原因是___________ 。
(5)甲同学认为邻氨基苯甲酸可以形成“内盐”,请从化学键的角度解释“内盐”中离子键的形成过程___________ 。
(6)步骤A的反应条件___________ ;步骤C中生成1 mol对氨基苯甲酸电子转移___________ mol。

已知:i.羧基使苯环上与羧基处于间位的氢原子易被取代
ii .苯胺中的氨基易被氧化
iii.
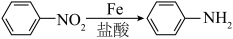
(1)基态N原子的电子有
(2)氨基苯甲酸中C=O中O原子的杂化方式是
(3)组成氨基苯甲酸的4种元素的电负性由大到小的顺序是
(4)对氨基苯甲酸和邻氨基苯甲酸的沸点分别是339.9℃和311.9℃,沸点不同的原因是
(5)甲同学认为邻氨基苯甲酸可以形成“内盐”,请从化学键的角度解释“内盐”中离子键的形成过程
(6)步骤A的反应条件
您最近一年使用:0次
名校
10 . 硅是地壳中储量仅次于氧的元素,在自然界中主要以 和硅酸盐的形式存在。
和硅酸盐的形式存在。
(1)基态硅原子的价层电子的轨道表示式为_________ 。
(2)①晶态 的晶体类型为
的晶体类型为_________ ;
② 晶体中硅原子的杂化方式为
晶体中硅原子的杂化方式为_________ 。
(3)硅、金刚石和碳化硅晶体的熔点由高到低的顺序为_______ ,请解释原因__________ 。
(4)硅元素最高价氧化物对应的水化物为原硅酸 。已知:原硅酸(
。已知:原硅酸( )可溶于水。原硅酸的羟基可以发生分子间脱水逐渐转化为硅酸、硅胶。
)可溶于水。原硅酸的羟基可以发生分子间脱水逐渐转化为硅酸、硅胶。
①原硅酸钠 溶液吸收空气中的
溶液吸收空气中的 会生成
会生成 ,结合元素周期律解释原因:
,结合元素周期律解释原因:_______ 。
②从结构的角度解释 脱水后溶解度降低的原因:
脱水后溶解度降低的原因:______ 。
 和硅酸盐的形式存在。
和硅酸盐的形式存在。(1)基态硅原子的价层电子的轨道表示式为
(2)①晶态
 的晶体类型为
的晶体类型为②
 晶体中硅原子的杂化方式为
晶体中硅原子的杂化方式为(3)硅、金刚石和碳化硅晶体的熔点由高到低的顺序为
(4)硅元素最高价氧化物对应的水化物为原硅酸
 。已知:原硅酸(
。已知:原硅酸( )可溶于水。原硅酸的羟基可以发生分子间脱水逐渐转化为硅酸、硅胶。
)可溶于水。原硅酸的羟基可以发生分子间脱水逐渐转化为硅酸、硅胶。①原硅酸钠
 溶液吸收空气中的
溶液吸收空气中的 会生成
会生成 ,结合元素周期律解释原因:
,结合元素周期律解释原因:②从结构的角度解释
 脱水后溶解度降低的原因:
脱水后溶解度降低的原因:
您最近一年使用:0次



