名校
解题方法
1 . 氮化硼(BN)是一种重要的功能陶瓷材料。以天然硼砂为起始物,经过一系列反应可以得到BF3和BN,如图一所示。下列叙述错误的是
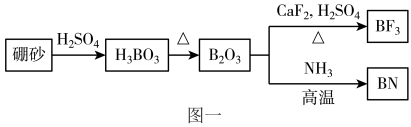


A.H3BO3在水溶液中发生反应: ,可知H3BO3是一元弱酸 ,可知H3BO3是一元弱酸 |
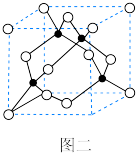
| B.六方氮化硼在高温高压下,可以转化为立方氮化硼,其晶胞结构如图二,立方氮化硼晶胞中含有4个氮原子、4个硼原子 |
| C.由B2O3可制备晶体硼,晶体硼的熔点2573K,沸点2823K,硬度大,属于共价晶体 |
| D.NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一,1 mol NH4BF4含有配位键的数目为NA |
您最近半年使用:0次
名校
解题方法
2 . 硒(Se)是人体必需微量元素之一,含硒化合物在材料领域具有重要应用。一种具有聚集诱导发光效应的含Se分子(Ⅳ)合成路线如下:
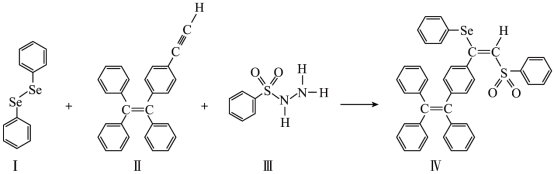
(1)Se与S同族,基态硒原子价电子排布式为__________ 。
(2) 的沸点低于
的沸点低于 ,根据结构解释其原因:
,根据结构解释其原因:__________ 。
(3)关于Ⅰ~Ⅳ四种物质中,下列说法正确的有__________ 。
a.Ⅰ中仅有 键,其中的Se—Se键为非极性键
键,其中的Se—Se键为非极性键
b.Ⅱ易溶于水,其分子式为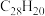
c.Ⅲ、Ⅳ中C均为 杂化,S均为
杂化,S均为 杂化
杂化
d.Ⅰ~Ⅳ含有的元素中,O电负性最大
(4)Ⅳ中具有孤对电子的原子有__________ 。
(5)推测硒的两种含氧酸的酸性强弱为
______  (填“>”或“<”)。研究发现,给小鼠喂适量硒酸钠
(填“>”或“<”)。研究发现,给小鼠喂适量硒酸钠 可减轻重金属铊引起的中毒。
可减轻重金属铊引起的中毒。 的空间结构为
的空间结构为__________ 。
(6)我国科学家发展了一种理论计算方法,可利用晶体衍射实验获得的结构数据预测其热电性能。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。
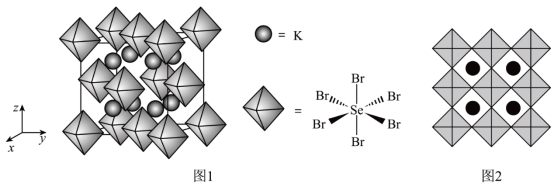
①X的化学式为__________ 。
②设X的最简式的式量为Mr,晶体密度为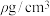 ,则X中相邻K之间的最短距离为
,则X中相邻K之间的最短距离为__________ nm(列出计算式, 为阿伏加德罗常数的值,
为阿伏加德罗常数的值,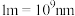 )。
)。

(1)Se与S同族,基态硒原子价电子排布式为
(2)
 的沸点低于
的沸点低于 ,根据结构解释其原因:
,根据结构解释其原因:(3)关于Ⅰ~Ⅳ四种物质中,下列说法正确的有
a.Ⅰ中仅有
 键,其中的Se—Se键为非极性键
键,其中的Se—Se键为非极性键b.Ⅱ易溶于水,其分子式为
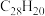
c.Ⅲ、Ⅳ中C均为
 杂化,S均为
杂化,S均为 杂化
杂化d.Ⅰ~Ⅳ含有的元素中,O电负性最大
(4)Ⅳ中具有孤对电子的原子有
(5)推测硒的两种含氧酸的酸性强弱为

 (填“>”或“<”)。研究发现,给小鼠喂适量硒酸钠
(填“>”或“<”)。研究发现,给小鼠喂适量硒酸钠 可减轻重金属铊引起的中毒。
可减轻重金属铊引起的中毒。 的空间结构为
的空间结构为(6)我国科学家发展了一种理论计算方法,可利用晶体衍射实验获得的结构数据预测其热电性能。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。

①X的化学式为
②设X的最简式的式量为Mr,晶体密度为
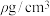 ,则X中相邻K之间的最短距离为
,则X中相邻K之间的最短距离为 为阿伏加德罗常数的值,
为阿伏加德罗常数的值,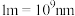 )。
)。
您最近半年使用:0次
3 . 关于各晶体说法错误的是
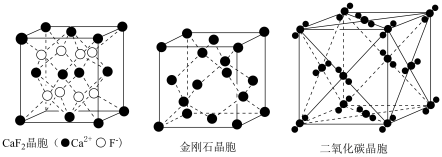
| A.金刚石是共价晶体,熔化时不会破坏化学键 |
B.在 晶体中,每个晶胞平均占有4个 晶体中,每个晶胞平均占有4个 |
C.在金刚石晶体中,碳原子与碳碳键数目之比为 |
D.每个 分子周围紧邻且等距 分子周围紧邻且等距 分子的有12个 分子的有12个 |
您最近半年使用:0次
2024-03-12更新
|
425次组卷
|
3卷引用:广东省东莞市第十高级中学2023-2024学年高二上学期第一次段考化学试题
4 . 叠氮化合物是重要的有机合成试剂,化学兴趣小组的同学在实验室制备了一种叠氮化合物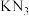 ,结构如图。下列说法正确的是
,结构如图。下列说法正确的是
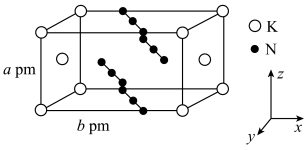
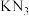 ,结构如图。下列说法正确的是
,结构如图。下列说法正确的是
A.该晶体中每个 周围距离最近且相等的 周围距离最近且相等的 共有12个 共有12个 |
B.该叠氮化合物的密度为 |
| C.测定该晶体结构的方法是红外光谱法 |
D. 与 与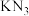 相比, 相比, 的熔点低于 的熔点低于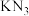 的熔点 的熔点 |
您最近半年使用:0次
名校
解题方法
5 . 教材插图具有简洁而又内涵丰富的特点。请回答以下问题:
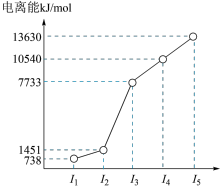
(1)第三周期的某主族元素,其第一至第五电离能数据如图所示,则该元素对应的原子有________ 种不同运动状态的电子。
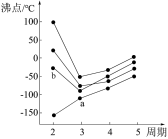
(2)如图所示,每条折线表示周期表ⅣA~ⅦA中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a代表的是________ (写化学式)。
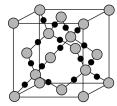
(3) 在高温高压下所形成的晶体其晶胞如图所示。则该晶体的类型属于
在高温高压下所形成的晶体其晶胞如图所示。则该晶体的类型属于________ 晶体。
(4)第一电离能介于Al、P之间的第三周期元素有________ 种。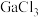 中中心原子的杂化方式为
中中心原子的杂化方式为________ 。
(5) 的一种配离子
的一种配离子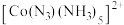 中,
中, 的配位数是
的配位数是________ ,配体的空间结构分别为________ 。
(6)金属磷化物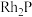 (化学式量为237)可用作电解水的高效催化剂,其立方晶胞如图所示,已知晶胞参数为
(化学式量为237)可用作电解水的高效催化剂,其立方晶胞如图所示,已知晶胞参数为 ,则晶体的密度为
,则晶体的密度为________ (列式即可)。

(1)第三周期的某主族元素,其第一至第五电离能数据如图所示,则该元素对应的原子有

(2)如图所示,每条折线表示周期表ⅣA~ⅦA中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中a代表的是

(3)
 在高温高压下所形成的晶体其晶胞如图所示。则该晶体的类型属于
在高温高压下所形成的晶体其晶胞如图所示。则该晶体的类型属于
(4)第一电离能介于Al、P之间的第三周期元素有
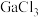 中中心原子的杂化方式为
中中心原子的杂化方式为(5)
 的一种配离子
的一种配离子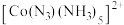 中,
中, 的配位数是
的配位数是(6)金属磷化物
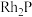 (化学式量为237)可用作电解水的高效催化剂,其立方晶胞如图所示,已知晶胞参数为
(化学式量为237)可用作电解水的高效催化剂,其立方晶胞如图所示,已知晶胞参数为 ,则晶体的密度为
,则晶体的密度为
您最近半年使用:0次
6 . 铁、铜及其化合物在日常生产、生活中有着广泛的应用。回答下列问题:
(1)基态Fe原子的价层电子的电子排布图为___________ 。
(2)三氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华。易溶于水,也易溶于乙醚、丙酮等有机溶剂。在蒸气中也容易双聚,据此判断三氯化铁晶体为___________ (填“分子晶体”或“离子晶体”)。
(3)(NH4)2Fe(SO4)2∙6H2O俗称摩尔盐,其阴离子 的空间构型为
的空间构型为___________ 。
(4)Fe(CO)5可用作催化剂、汽油抗爆剂等,其分子中σ键和π键的数目之比为___________ 。CO的沸点高于N2的原因是___________ 。
(5)CuCl2和CuCl是铜的两种氯化物。
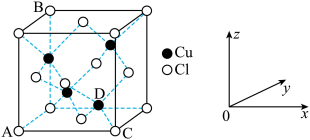
①图中表示的是___________ (填“CuCl2”或“CuCl”)的晶胞。
②原子坐标参数可用来表示晶胞内各原子的相对位置,图中各原子坐标参数A为 (0,0,0);B为(0,1,1);C为(1,0,0);则D原子的坐标参数为___________ 。
(1)基态Fe原子的价层电子的电子排布图为
(2)三氯化铁常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华。易溶于水,也易溶于乙醚、丙酮等有机溶剂。在蒸气中也容易双聚,据此判断三氯化铁晶体为
(3)(NH4)2Fe(SO4)2∙6H2O俗称摩尔盐,其阴离子
 的空间构型为
的空间构型为(4)Fe(CO)5可用作催化剂、汽油抗爆剂等,其分子中σ键和π键的数目之比为
(5)CuCl2和CuCl是铜的两种氯化物。

①图中表示的是
②原子坐标参数可用来表示晶胞内各原子的相对位置,图中各原子坐标参数A为 (0,0,0);B为(0,1,1);C为(1,0,0);则D原子的坐标参数为
您最近半年使用:0次
7 . 图甲是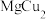 的拉维斯结构,Mg以金刚石方式堆积,在八面体空隙和半数的四面体空隙中,填入以四面体方式排列的Cu。图乙是沿立方格子对角面取得的截图,下列说法不正确的是
的拉维斯结构,Mg以金刚石方式堆积,在八面体空隙和半数的四面体空隙中,填入以四面体方式排列的Cu。图乙是沿立方格子对角面取得的截图,下列说法不正确的是
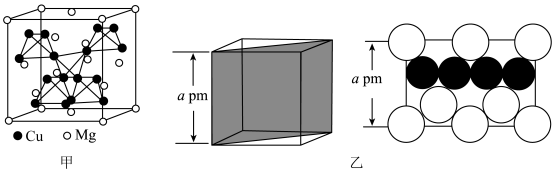
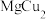 的拉维斯结构,Mg以金刚石方式堆积,在八面体空隙和半数的四面体空隙中,填入以四面体方式排列的Cu。图乙是沿立方格子对角面取得的截图,下列说法不正确的是
的拉维斯结构,Mg以金刚石方式堆积,在八面体空隙和半数的四面体空隙中,填入以四面体方式排列的Cu。图乙是沿立方格子对角面取得的截图,下列说法不正确的是
| A.该晶胞含有16个Cu原子 |
B.Mg原子围成的八面体空隙的边长为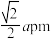 |
C.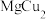 的密度 的密度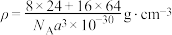 |
D.两个Cu原子之间的最短距离为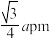 |
您最近半年使用:0次
8 . 低碳经济已成为人们一种新的生活理念,二氧化碳的捕捉和利用是能源领域的一个重要研究方向。回答下列问题:
(1)工业上用 和
和 反应合成二甲醚。已知:
反应合成二甲醚。已知:
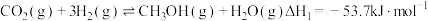
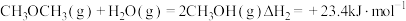
则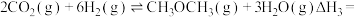
_______ kJ∙mol-1。
(2)二氧化碳的捕集、利用是我国能源领域的一个重要战略方向。科学家提出由 制取
制取 的太阳能工艺如图:
的太阳能工艺如图: ,则
,则 的化学式为
的化学式为_______ ,“热分解系统”中每转移 电子,需消耗
电子,需消耗
_______  。
。
(3)催化时还可以使用一种无机固体电解质作催化剂,其由正离子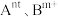 和负离子
和负离子 组成,该物质
组成,该物质 以上形成无序结构(高温相),
以上形成无序结构(高温相), 以下变为有序结构(低温相),二者晶体晶胞结构如图所示:
以下变为有序结构(低温相),二者晶体晶胞结构如图所示:_______ 。
ii.“高温相”具有良好的离子导电性,其主要原因是_______ 。
(4)铜基催化剂 (
( 为
为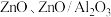 等)是
等)是 加氢制甲醇常用的催化剂,部分合成路线如图所示。
加氢制甲醇常用的催化剂,部分合成路线如图所示。 上发生反应的总化学方程式
上发生反应的总化学方程式_______ 。
(5)利用电解法在碱性或酸性条件下将 还原为
还原为 和
和 的原理如下图所示:
的原理如下图所示: 和法拉第效率(
和法拉第效率(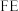 )的定义(X代表
)的定义(X代表 或
或 )如下:
)如下:
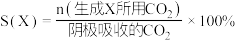

①实验测得,碱性条件生成 总的选择性小于酸性条件,原因是
总的选择性小于酸性条件,原因是_______ 。
②实验测得,酸性条件生成 总的法拉第效率小于碱性条件,原因是
总的法拉第效率小于碱性条件,原因是_______ 。
(1)工业上用
 和
和 反应合成二甲醚。已知:
反应合成二甲醚。已知: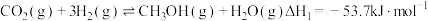
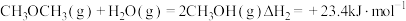
则
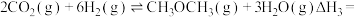
(2)二氧化碳的捕集、利用是我国能源领域的一个重要战略方向。科学家提出由
 制取
制取 的太阳能工艺如图:
的太阳能工艺如图: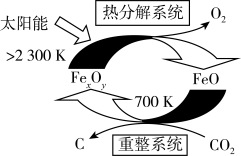
 ,则
,则 的化学式为
的化学式为 电子,需消耗
电子,需消耗
 。
。(3)催化时还可以使用一种无机固体电解质作催化剂,其由正离子
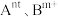 和负离子
和负离子 组成,该物质
组成,该物质 以上形成无序结构(高温相),
以上形成无序结构(高温相), 以下变为有序结构(低温相),二者晶体晶胞结构如图所示:
以下变为有序结构(低温相),二者晶体晶胞结构如图所示: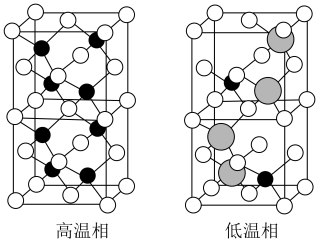
说明:图中,○球为负离子;高温相中的●深色球为正离子或空位;低温相中的 球为
球为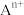 离子,●球为
离子,●球为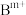 离子。
离子。
ii.“高温相”具有良好的离子导电性,其主要原因是
(4)铜基催化剂
 (
( 为
为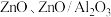 等)是
等)是 加氢制甲醇常用的催化剂,部分合成路线如图所示。
加氢制甲醇常用的催化剂,部分合成路线如图所示。 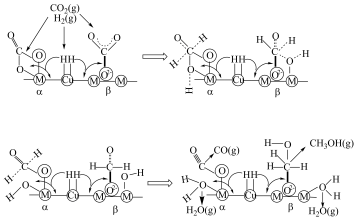
 上发生反应的总化学方程式
上发生反应的总化学方程式(5)利用电解法在碱性或酸性条件下将
 还原为
还原为 和
和 的原理如下图所示:
的原理如下图所示: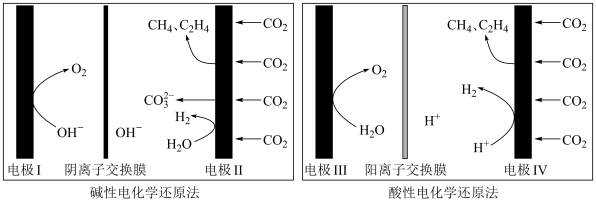
 和法拉第效率(
和法拉第效率(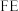 )的定义(X代表
)的定义(X代表 或
或 )如下:
)如下: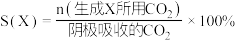

①实验测得,碱性条件生成
 总的选择性小于酸性条件,原因是
总的选择性小于酸性条件,原因是②实验测得,酸性条件生成
 总的法拉第效率小于碱性条件,原因是
总的法拉第效率小于碱性条件,原因是
您最近半年使用:0次
解题方法
9 . 硫酸氧钒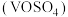 广泛用于媒染剂、催化剂、着色剂等方面。制备方法如下,回答下列问题:
广泛用于媒染剂、催化剂、着色剂等方面。制备方法如下,回答下列问题:
方法一:还原法制备

已知:在溶液中,钒主要以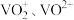 的形式存在。
的形式存在。
(1)基态 原子价层电子的轨道表示式为
原子价层电子的轨道表示式为_____________________
(2)真空干燥时需通入 的作用是
的作用是_____________________________ 。
(3)溶液 转化为
转化为 需要加入还原剂,最佳的还原剂为
需要加入还原剂,最佳的还原剂为_________ (填字母),写出相对应的离子方程式__________________________________________________
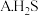
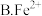

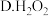
方法二:电解法制备
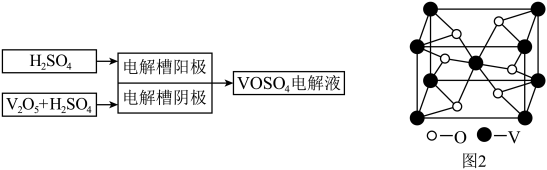
(4)写出电解槽中阴极反应式_________________________________________________________ 。
(5)与“电解法”相比,“还原法”的主要不足之处有_____________________ (写出一点)。
(6)钒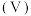 的某种氧化物的晶胞结构如图2所示。已知该晶体的密度为
的某种氧化物的晶胞结构如图2所示。已知该晶体的密度为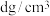 ,
, 表示阿伏加德罗常数的值,则晶胞的体积为
表示阿伏加德罗常数的值,则晶胞的体积为_____________________ 。
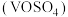 广泛用于媒染剂、催化剂、着色剂等方面。制备方法如下,回答下列问题:
广泛用于媒染剂、催化剂、着色剂等方面。制备方法如下,回答下列问题:方法一:还原法制备


已知:在溶液中,钒主要以
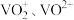 的形式存在。
的形式存在。(1)基态
 原子价层电子的轨道表示式为
原子价层电子的轨道表示式为(2)真空干燥时需通入
 的作用是
的作用是(3)溶液
 转化为
转化为 需要加入还原剂,最佳的还原剂为
需要加入还原剂,最佳的还原剂为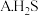
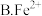

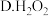
方法二:电解法制备


(4)写出电解槽中阴极反应式
(5)与“电解法”相比,“还原法”的主要不足之处有
(6)钒
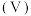 的某种氧化物的晶胞结构如图2所示。已知该晶体的密度为
的某种氧化物的晶胞结构如图2所示。已知该晶体的密度为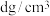 ,
, 表示阿伏加德罗常数的值,则晶胞的体积为
表示阿伏加德罗常数的值,则晶胞的体积为
您最近半年使用:0次
解题方法
10 . 钛及其化合物具有优异的物理、化学性能,相关的研究备受关注。
回答下列问题:
(1)基态钛原子的价电子排布式为______ 。
(2)钛元素的检验方法如图:
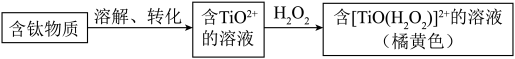
TiO2+可与H2O2形成稳定的配离子[TiO(H2O2)]2+,其原因是______ 。
(3)二氧化钛是良好的光催化剂,可催化转化多种有毒物质,如:可将水中的 转化为
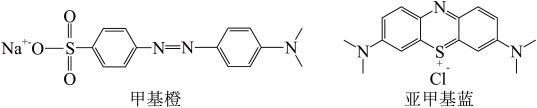
转化为 ;将甲基橙、亚甲基蓝、HCHO转化为CO2等。
;将甲基橙、亚甲基蓝、HCHO转化为CO2等。
① 的空间构型为
的空间构型为______ 。
②甲基橙、亚甲基蓝中S原子的杂化类型分别为______ 、______ 。
③常温下,1 L水中大约可溶解CO2、HCHO的体积分别为1 L、480 L,其主要原因是______ 。
(4)具有双钙钛矿型结构的晶体通过掺杂改性可用作固体电解质材料。双钙钛矿型晶体的一种典型结构单元如图所示:
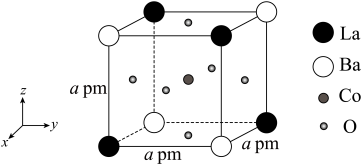
①晶体中与La距离最近的Ba的数目为______ 。
②该晶体的一个完整晶胞中含有______ 个Co原子。
③该晶胞的化学式为______
回答下列问题:
(1)基态钛原子的价电子排布式为
(2)钛元素的检验方法如图:

TiO2+可与H2O2形成稳定的配离子[TiO(H2O2)]2+,其原因是
(3)二氧化钛是良好的光催化剂,可催化转化多种有毒物质,如:可将水中的
 转化为
转化为 ;将甲基橙、亚甲基蓝、HCHO转化为CO2等。
;将甲基橙、亚甲基蓝、HCHO转化为CO2等。
①
 的空间构型为
的空间构型为②甲基橙、亚甲基蓝中S原子的杂化类型分别为
③常温下,1 L水中大约可溶解CO2、HCHO的体积分别为1 L、480 L,其主要原因是
(4)具有双钙钛矿型结构的晶体通过掺杂改性可用作固体电解质材料。双钙钛矿型晶体的一种典型结构单元如图所示:

①晶体中与La距离最近的Ba的数目为
②该晶体的一个完整晶胞中含有
③该晶胞的化学式为
您最近半年使用:0次



