名校
1 . 分析晶体与非晶体具有的性质:
(1)下图是冰块熔化过程中温度随时间的变化图像。分析图像可知,冰块熔化过程持续___________ min,此过程需___________ (填“吸热”或“放热”),温度___________ (填“升高”“不变”或“降低”)。所以,冰是___________ (填“晶体”或“非晶体”),区分晶体与非晶体的重要依据是___________ 。

(2)甲为石墨晶体,甲说明晶体具有___________ ;乙说明晶体具有各向异性而非晶体具有___________ ;丙说明晶体的内部微粒排列规范___________ 而非晶体内部微粒排列无序。

(3)如图所示为高温超导领域里的一种化合物——钙钛矿的晶体结构,该结构是具有代表性的最小重复单位。

①在该物质的晶体结构中,每个钛离子周围与它最近且距离相等的氧离子、钙离子、钛离子各有___________ 个、___________ 个、___________ 个。
②该晶体结构中,元素氧、钛、钙的离子个数比是___________ ,该物质的化学式可表示为___________ 。
(1)下图是冰块熔化过程中温度随时间的变化图像。分析图像可知,冰块熔化过程持续

(2)甲为石墨晶体,甲说明晶体具有

(3)如图所示为高温超导领域里的一种化合物——钙钛矿的晶体结构,该结构是具有代表性的最小重复单位。

①在该物质的晶体结构中,每个钛离子周围与它最近且距离相等的氧离子、钙离子、钛离子各有
②该晶体结构中,元素氧、钛、钙的离子个数比是
您最近一年使用:0次
名校
解题方法
2 . 在下列各题的横线上选择正确选项(A.“>”、B.“<”、C.“=”、D.“不确定”)。
(1)键能:
___________ Cl-Cl。
(2)分子极性:H2O___________ CH4。
(3)硬度:Si___________ SiC。
(4)键角:SO2___________ SO3。
(5)最外层电子数:B___________ Mn。
(6)熔沸点:MgO___________ NaCl。
(7)单电子数:Cr___________ Co。
(8)酸性:H3AsO4___________ H3AsO3。
(9)与NaOH反应中和热:HAc___________ HCl。
(10)晶体中阳离子配位数:CaF2___________ NaCl。
(11)晶胞空间利用率:Na___________ K。
(12)中心原子孤电子对:SO2___________ XeF2。
(13)第一电离能:I1(S)___________ I1(P)。
(14)分解温度:MgCO3___________ BaCO3。
(15)配位数:Mg___________ Cu。
(1)键能:

(2)分子极性:H2O
(3)硬度:Si
(4)键角:SO2
(5)最外层电子数:B
(6)熔沸点:MgO
(7)单电子数:Cr
(8)酸性:H3AsO4
(9)与NaOH反应中和热:HAc
(10)晶体中阳离子配位数:CaF2
(11)晶胞空间利用率:Na
(12)中心原子孤电子对:SO2
(13)第一电离能:I1(S)
(14)分解温度:MgCO3
(15)配位数:Mg
您最近一年使用:0次
3 . 某晶体晶胞结构如图所示,●表示X , 表示Y,请回答下列问题:
表示Y,请回答下列问题:

(1)晶体中每个X周围与之等距且距离最近的Y有___________ 个,每个Y周围与之等距且距离最近的Y有___________ 个,每个晶胞中含X的个数为___________ 个,该晶体的化学式为___________ 。
(2)若该晶胞的边长为a cm,则晶体的密度为___________ g·cm-3(列出计算式即可,已知该物质的摩尔质量为M g/mol,阿伏加德罗常数为NA)。
 表示Y,请回答下列问题:
表示Y,请回答下列问题:
(1)晶体中每个X周围与之等距且距离最近的Y有
(2)若该晶胞的边长为a cm,则晶体的密度为
您最近一年使用:0次
4 . C、Si元素组成的一些单质或化合物在科研领域中具有重要的作用。请回答下列问题。
(1)硅原子价层电子的轨道表示式中能量最低的是___________。
(2)由C、H、N可以形成化合物 ,C、H、N电负性大小顺序为
,C、H、N电负性大小顺序为___________ 。
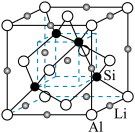
(3)Si与一些金属可以形成不同化合物,如图是Si与Al、Li形成的某化合物的晶胞示意图。已知晶胞棱长为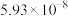 cm,Si与Al之间的共价键键长是
cm,Si与Al之间的共价键键长是___________ cm(只要求列算式,不必计算出数值)。
(1)硅原子价层电子的轨道表示式中能量最低的是___________。
A. | B. | C. | D. |
 ,C、H、N电负性大小顺序为
,C、H、N电负性大小顺序为(3)Si与一些金属可以形成不同化合物,如图是Si与Al、Li形成的某化合物的晶胞示意图。已知晶胞棱长为
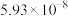 cm,Si与Al之间的共价键键长是
cm,Si与Al之间的共价键键长是
您最近一年使用:0次
解题方法
5 . 回答下列问题:
(1)有机物分子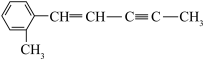 中最多有_______个原子共面。
中最多有_______个原子共面。
(2)从薄荷油中得到一种烃A(C10H16),与A相关的反应如下:

已知: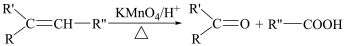 。
。
B的结构简式为_______ 。
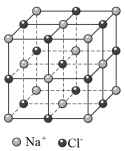
(3)NaCl晶体的结构如图所示,已知食盐的密度为ρ g·cm-3,摩尔质量为M g·mol-1,阿伏加德罗常数的值为NA,则在食盐晶体中Na+和Cl-的最小距离是_______ cm 。
(1)有机物分子
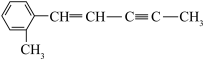 中最多有_______个原子共面。
中最多有_______个原子共面。| A.12 | B.16 | C.20 | D.24 |

已知:
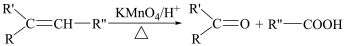 。
。B的结构简式为
(3)NaCl晶体的结构如图所示,已知食盐的密度为ρ g·cm-3,摩尔质量为M g·mol-1,阿伏加德罗常数的值为NA,则在食盐晶体中Na+和Cl-的最小距离是

您最近一年使用:0次
6 . 按要求完成下列题目。
(1)3,3-二甲基-1-丁烯 的结构简式:_______ 。
(2)甲晶体的晶胞结构如图所示:
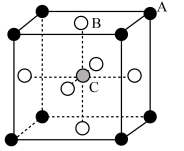
则甲晶体中A、B、C三种微粒的个数比是_______ 。
(3)12 g金刚石中含有的C—C数目为_______ NA(NA为阿伏加德罗常数的值)
(4)1-丙烯发生加聚反应,生成产物的结构简式:_______ 。
(5)完全燃烧1 mol 苯甲醇(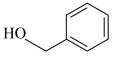 ),消耗
),消耗_______ mol O2
(1)3,3-二甲基-1-丁烯 的结构简式:
(2)甲晶体的晶胞结构如图所示:

则甲晶体中A、B、C三种微粒的个数比是
(3)12 g金刚石中含有的C—C数目为
(4)1-丙烯发生加聚反应,生成产物的结构简式:
(5)完全燃烧1 mol 苯甲醇(
 ),消耗
),消耗
您最近一年使用:0次
7 . 按要求回答以下问题:
(1)现有 的配合物
的配合物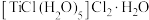 ,其中配离子是
,其中配离子是_______ ,配位数为_______ ,在0.2mol该配合物溶液中滴加足量的 溶液,产生沉淀的物质的量为
溶液,产生沉淀的物质的量为_______ ;
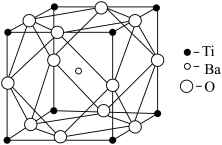
(2)偏钛酸钡晶体中晶胞的结构如图所示,晶胞边长为apm,阿伏加德罗常数为 ,则该晶体的密度为
,则该晶体的密度为_______  。
。
(1)现有
 的配合物
的配合物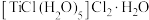 ,其中配离子是
,其中配离子是 溶液,产生沉淀的物质的量为
溶液,产生沉淀的物质的量为(2)偏钛酸钡晶体中晶胞的结构如图所示,晶胞边长为apm,阿伏加德罗常数为
 ,则该晶体的密度为
,则该晶体的密度为 。
。
您最近一年使用:0次
解题方法
8 . Na、Mg、Fe、Cu是四种重要的金属元素。回答下列问题:
(1)基态Mg原子的价层电子轨道表示式为__________________ 。
(2) 的电子式为
的电子式为____________ 。
(3)在钢铁厂的生产中,炽热的铁水注入模具之前,模具必须进行充分的干燥处理,不得留有水,请用化学方程式解释原因:__________________ 。
(4)检验 溶液中是否残留
溶液中是否残留 的试剂是
的试剂是__________________ 。
(5)NaCl熔点为800.8℃,工业上采用电解熔融NaCl制备金属Na。电解反应方程式为 ,加入
,加入 的目的是
的目的是____________ 。
(6)采用空气和Na为原料可直接制备 。空气与熔融金属Na反应前,需依次通过
。空气与熔融金属Na反应前,需依次通过____________ 、____________ (填序号)。
a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d. 溶液
溶液
(7)天然碱的主要成分为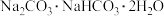 ,2 mol
,2 mol 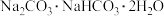 经充分加热得到
经充分加热得到 的质量为
的质量为______ g。
(8)一个 晶胞(如图)中,Cu原子的数目为
晶胞(如图)中,Cu原子的数目为______ 。
(1)基态Mg原子的价层电子轨道表示式为
(2)
 的电子式为
的电子式为(3)在钢铁厂的生产中,炽热的铁水注入模具之前,模具必须进行充分的干燥处理,不得留有水,请用化学方程式解释原因:
(4)检验
 溶液中是否残留
溶液中是否残留 的试剂是
的试剂是(5)NaCl熔点为800.8℃,工业上采用电解熔融NaCl制备金属Na。电解反应方程式为
 ,加入
,加入 的目的是
的目的是(6)采用空气和Na为原料可直接制备
 。空气与熔融金属Na反应前,需依次通过
。空气与熔融金属Na反应前,需依次通过a.浓硫酸 b.饱和食盐水 c.NaOH溶液 d.
 溶液
溶液(7)天然碱的主要成分为
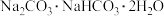 ,2 mol
,2 mol 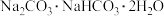 经充分加热得到
经充分加热得到 的质量为
的质量为(8)一个
 晶胞(如图)中,Cu原子的数目为
晶胞(如图)中,Cu原子的数目为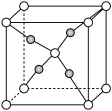
您最近一年使用:0次
2023-02-20更新
|
555次组卷
|
4卷引用:2022年天津市普通高中学业水平等级性考试化学试题变式题(结构与性质)
(已下线)2022年天津市普通高中学业水平等级性考试化学试题变式题(结构与性质)天津市南开区2022~2023 学年高三上学期阶段性质量监测 (二) 化学试题(已下线)结构与性质天津市八校2024届高三下学期联合模拟考试化学试题(二)
名校
解题方法
9 . 研究表明新冠病毒在铜表面存活时间最短,仅为4小时,铜被称为细菌病毒的“杀手”。回答下列问题:
(1)铜的晶胞结构如下图所示,铜原子的配位数为_______ ,基态铜原子价层电子排布式为_______ 。

(2)如果A原子的坐标为(0,1,0),则B原子的坐标为_______ ;
(3)与铜同周期,N能层电子数与铜相同,熔点最低的金属是_______ 。
(4)农药波尔多液的有效杀菌成分是Cu2(OH)2SO4(碱式硫酸铜),碱式硫酸铜中非金属元素电负性由大到小的顺序是_______ , 的空间构型为
的空间构型为_______ 。
(1)铜的晶胞结构如下图所示,铜原子的配位数为

(2)如果A原子的坐标为(0,1,0),则B原子的坐标为
(3)与铜同周期,N能层电子数与铜相同,熔点最低的金属是
(4)农药波尔多液的有效杀菌成分是Cu2(OH)2SO4(碱式硫酸铜),碱式硫酸铜中非金属元素电负性由大到小的顺序是
 的空间构型为
的空间构型为
您最近一年使用:0次
名校
解题方法
10 . 关于物质结构与性质的内在联系,请回答下列问题:
(1)已知Se与O同族,基态Se原子价层电子的运动状态有______ 种,基态O原子的电子排布式不能表示为1s22s22p 2p
2p ,因为这违背了
,因为这违背了______ (填选项)。
A.能量最低原理 B.泡利不相容原理 C.洪特规则
(2)已知液态的二氧化硫可以发生类似的水自身电离反应:2SO2(l) SO2++SO
SO2++SO 。SO2+中的σ键和π键数目之比为
。SO2+中的σ键和π键数目之比为______ ,SO2的空间构型为______ 。
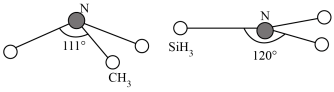
(3)由于硅的价层有d轨道可以利用,而碳没有,因此它们的化合物结构和性质存在较大差异。化合物N(CH3)3(三角锥形)和N(SiH3)3(平面形)的结构如图所示,则二者中N的杂化方式分别为______ 。更易形成配合物的是______ 。______ 。______ g•cm-3(用含NA、a、b的式子表示)。
(1)已知Se与O同族,基态Se原子价层电子的运动状态有
 2p
2p ,因为这违背了
,因为这违背了A.能量最低原理 B.泡利不相容原理 C.洪特规则
(2)已知液态的二氧化硫可以发生类似的水自身电离反应:2SO2(l)
 SO2++SO
SO2++SO 。SO2+中的σ键和π键数目之比为
。SO2+中的σ键和π键数目之比为(3)由于硅的价层有d轨道可以利用,而碳没有,因此它们的化合物结构和性质存在较大差异。化合物N(CH3)3(三角锥形)和N(SiH3)3(平面形)的结构如图所示,则二者中N的杂化方式分别为
您最近一年使用:0次



