名校
1 . NA表示阿伏加 德罗常数的值,下列叙述不正确的是( )
| A.60gSiO2晶体含4NA个σ键 |
| B.78gNa2O2晶体中含有离子个数为4NA |
| C.在12g石墨中含C−C共价键数目为1.5NA |
| D.CO和N2是等电子体,标况下22.4L的CO气体与1molN2所含的电子数相等 |
您最近一年使用:0次
名校
解题方法
2 . 科学家成功地制成了一种新型的碳氧化合物,该化合物晶体中每个碳原子均以四个共价单键与氧原子结合为一种空间网状的无限伸展结构,下列对该晶体的叙述错误的是( )
| A.该物质的化学式为CO4 |
| B.晶体中C原子数与C−O键数之比为1:4 |
| C.晶体的熔、沸点高,硬度大 |
| D.该晶体为原子晶体 |
您最近一年使用:0次
2020-03-21更新
|
125次组卷
|
2卷引用:福建省福州市格致中学2018-2019学年高二下学期期中考试化学试题
名校
解题方法
3 . 氮氧化铝(AlON)是一种透明高硬度防弹材料,硬度为石英玻璃的 4 倍,可耐 120 摄氏度的高温。下列描述错误的是( )
| A.AlON 和石英的化学键类型相同 | B.AlON 和石英晶体类型相同 |
| C.AlON 和 NaCl 的化学键类型不同 | D.AlON 和 NaCl 晶体类型相同 |
您最近一年使用:0次
2020-03-20更新
|
164次组卷
|
2卷引用:福建省福州市福州三中 2018-2019 学年高一下学期期中考试化学试题
4 . 氮氧化铝(AlON)属于原子晶体,是一种超强透明材料,下列描述错的是( )
| A.AlON和石英的化学键类型相同 | B.电解熔融AlON可得到Al |
| C.AlON的N元素化合价为﹣1 | D.AlON和石英晶体类型相同 |
您最近一年使用:0次
2020-03-06更新
|
442次组卷
|
3卷引用:福建省莆田第十五中学2019-2020学年高二下学期期末考试化学试题
5 . 中国科学家以二氧化碳为碳源,金属钠为还原剂,在470℃、 下成功合成金刚石。下列说法不正确的是
下成功合成金刚石。下列说法不正确的是
 下成功合成金刚石。下列说法不正确的是
下成功合成金刚石。下列说法不正确的是| A.由二氧化碳合成金刚石是化学变化 | B.金刚石是碳的一种同位素 |
| C.金刚石属于原子晶体 | D.金刚石中只含有共价键 |
您最近一年使用:0次
2020-03-02更新
|
174次组卷
|
3卷引用:福建省仙游县枫亭中学2022-2023学年高一下学期期中考试化学试题
解题方法
6 . 硼是新型无机材料中的明星元素。

(1)磷化硼是一种耐磨涂料,可由三溴化硼和三溴化磷高温下在氢气中反应合成,其化学方程式为______ ,图为磷化硼晶体结构中最小的重复单元,磷化硼的晶体类型是 ______ ,一个晶胞中含 ______ 个P原子,每个B或P均形成4个共价键,其中有一个配位键,提供空轨道的是 ______ 原子。
(2)氮化硼是一种重要的功能陶瓷材料,其结构与磷化硼相似,B和N相比,电负性较大的是______ (填元素符号),其基态原子的电子排布式为 ______ ,氮化硼中B元素的化合价为 ______ 。
(3)环硼氮烷与苯是等电子体,其一氯代物有两种结构、二氯代物有四种结构,写出环硼氮烷分子结构式______ 。
(4)BF3用作有机合成中的催化剂,也用于制造火箭的高能燃料。在BF3分子中,F-B-F的键角是______ 度,B原子采用 ______ 杂化; BF3和过量NaF作用可生成NaBF4,BF4-的立体构型为 ______ 。

(1)磷化硼是一种耐磨涂料,可由三溴化硼和三溴化磷高温下在氢气中反应合成,其化学方程式为
(2)氮化硼是一种重要的功能陶瓷材料,其结构与磷化硼相似,B和N相比,电负性较大的是
(3)环硼氮烷与苯是等电子体,其一氯代物有两种结构、二氯代物有四种结构,写出环硼氮烷分子结构式
(4)BF3用作有机合成中的催化剂,也用于制造火箭的高能燃料。在BF3分子中,F-B-F的键角是
您最近一年使用:0次
名校
7 . 设NA为阿伏加 德罗常数的值,下列说法正确的是( )。
| A.20 g D2O与18 g H2O中,中子数之比为2∶1 |
| B.常温常压下,0.5 mol O3与11.2 L O2 所含的分子数均为0.5NA |
| C.6.0 g SiO2 中含有0.1NA个SiO2分子 |
| D.1 mol过氧化钠和1 mol氧化钠中阴、阳离子个数之比相同 |
您最近一年使用:0次
8 . 已知NA为阿伏加 德罗常数的值。下列说法不正确的是( )
| A.12g金刚石中平均含有2NA个σ键 |
| B.1mol SiO2晶体中平均含有4NA个σ键 |
| C.12g石墨中平均含1.5NA个σ键 |
| D.1mol CH4中含4NA个s﹣p σ键 |
您最近一年使用:0次
9 . 下图表示一些晶体中的某些结构,请回答下列问题:
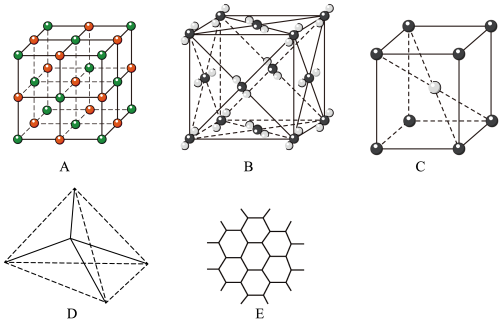
(1)代表金刚石的是(填编号字母,下同)_____ ,其中每个碳原子与_____ 个碳原子最近且距离相等。
(2)代表石墨的是_____ ,每个正六边形占有的碳原子数平均为_____ 个。
(3)代表 NaCl 的是_________ ,每个 Na+周围与它最近且距离相等的 Cl-有_____ 个。
(4)代表 CsCl 的是_____ ,每个 Cs+与_____ 个 Cl-紧邻。
(5)代表干冰的是_____ ,每个 CO2分子与_____ 个 CO2分子紧邻。
(6)已知石墨中碳碳键的键长比金刚石中碳碳键的键长短,则上述五种物质熔点由高到低的排列顺序为_____ 。

(1)代表金刚石的是(填编号字母,下同)
(2)代表石墨的是
(3)代表 NaCl 的是
(4)代表 CsCl 的是
(5)代表干冰的是
(6)已知石墨中碳碳键的键长比金刚石中碳碳键的键长短,则上述五种物质熔点由高到低的排列顺序为
您最近一年使用:0次
名校
10 . 下列各组物质的性质排序正确的是
| A.熔点:NaF <NaCl <NaBr <NaI | B.沸点:CF4 <CCl4 <CBr4 <CI4 |
| C.熔点:碳化硅<晶体硅<金刚石 | D.硬 度 :Li <Na <K <Rb |
您最近一年使用:0次
2019-07-01更新
|
396次组卷
|
4卷引用:福建省莆田第六中学2018-2019学年高二下学期期中考试(B卷)化学试题



