名校
解题方法
1 . 铜和三氧化二铁在工农业生产中用途广泛,用黄铜矿(主要成分为CuFeS2,其中Cu为+2价、Fe为+2价)制取铜和三氧化二铁的工艺流程如图所示:
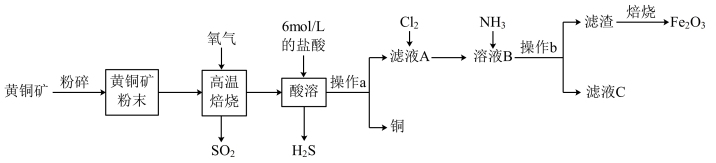
(1)将黄铜矿粉碎的目的是____ 。
(2)高温熔烧时发生的反应是CuFeS2+O2 SO2+FeS+Cu、1molO2参加反应时,反应中转移电子
SO2+FeS+Cu、1molO2参加反应时,反应中转移电子____ mol。
(3)操作a为____ 。
(4)向滤液A中通入Cl2的目的是____ 。
(5)向溶液B中通入NH3后发生反应的离子方程式为____ 。
(6)工业上用生物法处理H2S的原理为(硫杆菌作催化剂):
H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4=2Fe2(SO4)3+2H2O
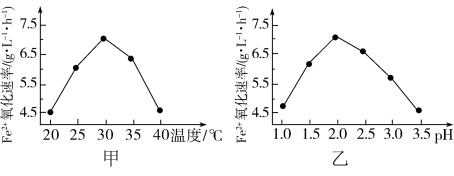
由图甲和图乙判断使用硫杆菌的最佳条件为___ ,若反应温度过高,反应速率下降,其原因是___ 。

(1)将黄铜矿粉碎的目的是
(2)高温熔烧时发生的反应是CuFeS2+O2
 SO2+FeS+Cu、1molO2参加反应时,反应中转移电子
SO2+FeS+Cu、1molO2参加反应时,反应中转移电子(3)操作a为
(4)向滤液A中通入Cl2的目的是
(5)向溶液B中通入NH3后发生反应的离子方程式为
(6)工业上用生物法处理H2S的原理为(硫杆菌作催化剂):
H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4=2Fe2(SO4)3+2H2O
由图甲和图乙判断使用硫杆菌的最佳条件为

您最近一年使用:0次
2022-06-16更新
|
1326次组卷
|
5卷引用:河南省项城市第三高级中学2021-2022学年高二下学期期末考试化学试题
河南省项城市第三高级中学2021-2022学年高二下学期期末考试化学试题北京市第一七一中学2021-2022学年高一下学期6月月考化学试题(已下线)模拟卷02-2023年高三化学对接新高考全真模拟试卷(云南,安徽,黑龙江,山西,吉林五省通用)(已下线)模拟卷06-2023年高三化学对接新高考全真模拟试卷(云南,安徽,黑龙江,山西,吉林五省通用)(已下线)模拟卷05-2023年高三化学对接新高考全真模拟试卷(云南,安徽,黑龙江,山西,吉林五省通用)
名校
2 . Ⅰ、我国规定生活用水中镉排放的最大允许浓度为0.005mg/L。处理含镉废水可采用化学沉淀法。试回答下列问题:
(1)磷酸镉[Cd3(PO4)2]沉淀溶解平衡常数的表达式Ksp=______ 。
(2)一定温度下,CdCO3的Ksp=4.0×10-12,CdS的Ksp=7.9×10-27,欲将某含镉废水中的Cd2+沉淀下来,最好选用______ (填“Na2CO3”或“Na2S”)
(3)若往某含镉废水中加入Na2S,当S2-浓度达到7.9×10-8mol·L-1时,水体中Cd2+浓度为______ mol·L-1(已知:Ksp(CdS)=7.9×10-27,Cd的相对原子质量为112);此时是否符合水源标准?______ (填“是”或“否”)。
Ⅱ、炼锌烟尘(主要成分为ZnO,含少量CuO和FeO)为原料,可以制取氯化锌和金属锌。制取氯化锌主要工艺如下:
(4)加入H2O2溶液的作用是______ 。
(5)流程图中,调节pH时,加入的试剂X可以是______ (填序号)
A、ZnO B、NaOH C、Zn2(OH)2CO3 D、ZnSO4
pH应调整到______ 。再将生成的氢氧化铁沉淀除去。
(1)磷酸镉[Cd3(PO4)2]沉淀溶解平衡常数的表达式Ksp=
(2)一定温度下,CdCO3的Ksp=4.0×10-12,CdS的Ksp=7.9×10-27,欲将某含镉废水中的Cd2+沉淀下来,最好选用
(3)若往某含镉废水中加入Na2S,当S2-浓度达到7.9×10-8mol·L-1时,水体中Cd2+浓度为
Ⅱ、炼锌烟尘(主要成分为ZnO,含少量CuO和FeO)为原料,可以制取氯化锌和金属锌。制取氯化锌主要工艺如下:

| 金属离子 | Fe3+ | Zn2+ | Fe2+ |
| 开始沉淀的pH | 1.1 | 5.2 | 5.8 |
| 沉淀完全的pH | 3.2 | 6.4 | 8.8 |
(4)加入H2O2溶液的作用是
(5)流程图中,调节pH时,加入的试剂X可以是
A、ZnO B、NaOH C、Zn2(OH)2CO3 D、ZnSO4
pH应调整到
您最近一年使用:0次
2023-11-10更新
|
818次组卷
|
3卷引用:广东省茂名市信宜市2023-2024学年高二上学期11月期中考试化学试题
名校
3 . 选择下列实验方法分离、提纯物质,将分离、提纯方法的字母填在横线上。
A.萃取 B.重结晶 C.分液 D.蒸馏 E.过滤 F.洗气
(1)分离水和汽油的混合物:___________ 。
(2)分离四氯化碳 (沸点为76.75 ℃)和甲苯(沸点为110.6 ℃)的混合物:___________ 。
(3)提取碘水中的碘:___________ 。
(4)除去混在乙烷中的乙烯:___________ 。
(5)从硝酸钾和氯化钠的混合溶液中获得硝酸钾:___________ 。
A.萃取 B.重结晶 C.分液 D.蒸馏 E.过滤 F.洗气
(1)分离水和汽油的混合物:
(2)分离四氯化碳 (沸点为76.75 ℃)和甲苯(沸点为110.6 ℃)的混合物:
(3)提取碘水中的碘:
(4)除去混在乙烷中的乙烯:
(5)从硝酸钾和氯化钠的混合溶液中获得硝酸钾:
您最近一年使用:0次
2022-02-14更新
|
1690次组卷
|
5卷引用:2016-2017学年内蒙古集宁一中高二下月考二化学卷
2016-2017学年内蒙古集宁一中高二下月考二化学卷课前-1.2.1 有机化合物的分离、提纯-人教2019选择性必修3(已下线)第03讲 有机物的分离、提纯(word讲义)-【帮课堂】2021-2022学年高二化学同步精品讲义(人教2019选择性必修3)(已下线)【知识图鉴】单元讲练测选择性必修3第1单元01讲核心安徽省安庆市第七中学2021-2022学年高二下学期3月阶段性考试化学试题
名校
解题方法
4 . 工业制胆矾时,将粗制CuO粉末(含杂质FeO、Fe2O3)慢慢加入适量的稀H2SO4中完全溶解,除去杂质离子后,再蒸发结晶可得纯净的胆矾晶体。已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH接近4时,Fe3+以Fe(OH)3的形式完全沉淀。回答下列问题:
(1)为除去溶液中的Fe2+,可先加入_______ ,(从下面四个选项选择)将Fe2+氧化为Fe3+,反应的离子方程式为_______ ,然后加入适量的_______ ,(从下面四个选项选择)调整溶液的pH使Fe3+转化为Fe(OH)3沉淀。
A.CuO B.Cl2 C.Cu(OH)2 D.H2O2
(2)甲同学怀疑调整至溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp = 1×10-38,Cu(OH)2的溶度积Ksp=3×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol•L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3mol•L-1,则Cu(OH)2开始沉淀时溶液的pH为___________ ,Fe3+完全沉淀时溶液的pH为___________ ,通过计算即可确定上述方案是否可行。
(1)为除去溶液中的Fe2+,可先加入
A.CuO B.Cl2 C.Cu(OH)2 D.H2O2
(2)甲同学怀疑调整至溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp = 1×10-38,Cu(OH)2的溶度积Ksp=3×10-20,通常认为残留在溶液中的离子浓度小于1×10-5 mol•L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3mol•L-1,则Cu(OH)2开始沉淀时溶液的pH为
您最近一年使用:0次
2021-08-24更新
|
1679次组卷
|
9卷引用:河南省洛阳市2020-2021学年高二上学期期中考试化学试题
河南省洛阳市2020-2021学年高二上学期期中考试化学试题(已下线)第三章 水溶液中的离子反应与平衡(能力提升)-2020-2021学年高二化学单元测试定心卷(人教版2019选择性必修一)山东省莱西市第一中学2020-2021学年高二上学期12月月考化学试题课选择性必修1 专题3 第四单元 课时2 Ksp相关计算及其图像分析吉林省延边第二中学2020-2021学年高二上学期第二次考试月考化学试题(已下线)第三章第四节 难溶电解的溶解平衡(备作业)-【上好课】2021-2022学年高二化学选修4同步备课系列(人教版)吉林省汪清县第六中学2021-2022学年高二12月月考化学试题吉林省延边第二中学2022-2023学年高二上学期期末考试化学试题3.4.2沉淀溶解平衡原理的应用 课后
名校
5 . 工业废水中的重金属离子会导致环境污染危害人体健康,可用多种方法去除。
I.臭氧法
络合态的金属离子难以直接去除。O3与水反应产生的·OH(羟基自由基)可以氧化分解金属配合物[mRa+ ·nX]中的有机配体,使金属离子游离到水中,反应原理为:
·OH+[mRa+·nX] →mRa++CO2+H2O (Ra+表示金属离子,X表示配体)
·OH同时也能与溶液中的 、
、 反应。在某废水中加入Ca(OH)2,再通入O3可处理其中的络合态镍(II)。
反应。在某废水中加入Ca(OH)2,再通入O3可处理其中的络合态镍(II)。
(1)基态Ni2+的核外电子排布式为_______ 。
(2)加入的Ca(OH)2的作用是_______ 。
Ⅱ.纳米零价铝法
纳米铝粉有很强的吸附性和还原性,水中溶解的氧在纳米铝粉表面产生·OH(羟基自由基),可将甘氨酸铬中的有机基团降解,释放出的铬(VI)被纳米铝粉去除。
(3)向AlCl3溶液中滴加碱性NaBH4溶液,溶液中BH (B元素的化合价为+3)与Al3+反应可生成纳米铝粉、H2和B(OH)
(B元素的化合价为+3)与Al3+反应可生成纳米铝粉、H2和B(OH) ,其离子方程式为
,其离子方程式为 _______ 。
(4)向含有甘氨酸铬的废水中加入纳米铝粉,研究溶液中总氮含量[ ]随时间的变化可知甘氨酸铬在降解过程中的变化状态。实验测得溶液中总氮含量随时间的变化如图所示,反应初期溶液中的总氮含量先迅速降低后随即上升的原因是
]随时间的变化可知甘氨酸铬在降解过程中的变化状态。实验测得溶液中总氮含量随时间的变化如图所示,反应初期溶液中的总氮含量先迅速降低后随即上升的原因是 _______ 。

Ⅲ.金属炭法
其他条件相同,分别取铝炭混合物和铁炭混合物,与含Zn2+的废水反应相同时间,Zn2+去除率与废水pH的关系如图所示。

(5)废水pH为3时,铝炭混合物对Zn2+去除率远大于铁炭混合物的主要原因是_______ 。
(6)废水pH大于6,随着pH增大,铝炭混合物对Zn2+去除率增大的原因是_______ 。
I.臭氧法
络合态的金属离子难以直接去除。O3与水反应产生的·OH(羟基自由基)可以氧化分解金属配合物[mRa+ ·nX]中的有机配体,使金属离子游离到水中,反应原理为:
·OH+[mRa+·nX] →mRa++CO2+H2O (Ra+表示金属离子,X表示配体)
·OH同时也能与溶液中的
 、
、 反应。在某废水中加入Ca(OH)2,再通入O3可处理其中的络合态镍(II)。
反应。在某废水中加入Ca(OH)2,再通入O3可处理其中的络合态镍(II)。(1)基态Ni2+的核外电子排布式为
(2)加入的Ca(OH)2的作用是
Ⅱ.纳米零价铝法
纳米铝粉有很强的吸附性和还原性,水中溶解的氧在纳米铝粉表面产生·OH(羟基自由基),可将甘氨酸铬中的有机基团降解,释放出的铬(VI)被纳米铝粉去除。
(3)向AlCl3溶液中滴加碱性NaBH4溶液,溶液中BH
 (B元素的化合价为+3)与Al3+反应可生成纳米铝粉、H2和B(OH)
(B元素的化合价为+3)与Al3+反应可生成纳米铝粉、H2和B(OH) ,其离子方程式为
,其离子方程式为 (4)向含有甘氨酸铬的废水中加入纳米铝粉,研究溶液中总氮含量[
 ]随时间的变化可知甘氨酸铬在降解过程中的变化状态。实验测得溶液中总氮含量随时间的变化如图所示,反应初期溶液中的总氮含量先迅速降低后随即上升的原因是
]随时间的变化可知甘氨酸铬在降解过程中的变化状态。实验测得溶液中总氮含量随时间的变化如图所示,反应初期溶液中的总氮含量先迅速降低后随即上升的原因是 
Ⅲ.金属炭法
其他条件相同,分别取铝炭混合物和铁炭混合物,与含Zn2+的废水反应相同时间,Zn2+去除率与废水pH的关系如图所示。

(5)废水pH为3时,铝炭混合物对Zn2+去除率远大于铁炭混合物的主要原因是
(6)废水pH大于6,随着pH增大,铝炭混合物对Zn2+去除率增大的原因是
您最近一年使用:0次
2022-05-07更新
|
915次组卷
|
3卷引用:江苏省扬州中学2022-2023学年高二下学期期中考试化学试题
6 . 请回答实验室石油分馏的有关问题:________ ;B_____ 。
(2)图中有______ 处错误。
(3)实验室石油分馏的正确操作顺序是E→ F→____→A→______→_____→G,________ 。
A.连接接液管 B.装入碎瓷片和石油,塞上带温度计的塞子 C.检查装置气密性 D.连接B仪器及进出水管 E.在铁架台上放酒精灯,固定好铁圈,放上石棉网 F.固定好A仪器 G.加热
(4)分馏石油得到的各个馏分都是___________ (填“混合物”或“纯净物”),在A中注入原油后,加几片碎瓷片的目的是___________ 。
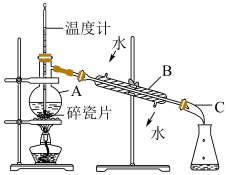
(2)图中有
(3)实验室石油分馏的正确操作顺序是E→ F→____→A→______→_____→G,
A.连接接液管 B.装入碎瓷片和石油,塞上带温度计的塞子 C.检查装置气密性 D.连接B仪器及进出水管 E.在铁架台上放酒精灯,固定好铁圈,放上石棉网 F.固定好A仪器 G.加热
(4)分馏石油得到的各个馏分都是
您最近一年使用:0次
名校
解题方法
7 . 肉桂酸( )主要用于香精香料、食品添加剂、医药工业、美容、农药有机合成等方面。实验室可通过如下反应合成,实验装置如图所示:
)主要用于香精香料、食品添加剂、医药工业、美容、农药有机合成等方面。实验室可通过如下反应合成,实验装置如图所示:
主反应: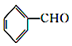 +(CH3CO)2O(乙酸酐)
+(CH3CO)2O(乙酸酐)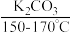
 +CH3COOH
+CH3COOH
副反应:
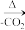


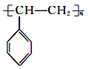 (树脂状物)
(树脂状物)

| 名称 | 相对分子质量 | 熔点/℃ | 沸点/℃ | 密度/g mL-1 mL-1 | 溶解性 |
| 乙酸 | 60 | 16.6 | 117.9 | 1.05 | 能与冷水任意比互溶 |
| 苯甲醛 | 106 | -26 | 179 | 1.06 | 微溶于水,与苯,乙醇、乙醚混溶 |
| 乙酸酐 | 102 | -73.1 | 138.6 | 1.082 | 能溶于冷水 |
| 肉桂酸 | 148 | 133 | 300 | 1.248 | 不溶于冷水,易溶于苯、乙醚,在热水中溶于乙醇 |
Ⅰ.将7.00g无水K2CO3、14.5mL乙酸酐和5.0mL苯甲醛依次加入150mL仪器a中,加热至微沸后保持温度150-170℃加热回流30-45min。
Ⅱ.将反应后的混合物冷却,边搅拌边分次加入40mL水浸泡。
Ⅲ.连接水蒸气蒸馏装置将未完全反应的苯甲醛用水蒸气蒸馏除去。
Ⅳ.将仪器a冷却,加入40mL10%NaOH溶液,使所有的肉桂酸形成钠盐而溶解。加入90mL蒸馏水,将混合物加热,活性炭脱色,趁热过滤除去树脂状物,将滤液冷却至室温以下。
Ⅴ.边搅拌边将20mL浓盐酸和20mL水的混合物加到肉桂酸盐溶液中至呈酸性。用冷水冷却,待结晶完全后抽滤得到粗产品,粗产品经进一步提纯后,得到3.56g产品。
回答下列问题:
(1)仪器a的名称为
(2)冷却水的入口为
(3)水蒸气蒸馏将苯甲醛完全除去的标志是
(4)步骤Ⅳ趁热过滤的目的是
(5)加入浓盐酸与水的混合物后发生反应的化学方程式为
(6)将粗产品提纯的操作名称为
您最近一年使用:0次
2022-05-06更新
|
1153次组卷
|
6卷引用:河北省石家庄市第十七中学2023-2024学年高二下学期第一次月考化学试题
河北省石家庄市第十七中学2023-2024学年高二下学期第一次月考化学试题宁夏石嘴山市第三中学2022届高三第三次模拟考试理综化学试题福建省连城县第一中学2022-2023学年高三上学期暑期月考化学试题(已下线)微专题46 常见有机物的制备实验-备战2023年高考化学一轮复习考点微专题(已下线)第十一章 有机化学基础 (测)-2023年高考化学一轮复习讲练测(全国通用)(已下线)专题03 化学实验专题-【大题精做】冲刺2023年高考化学大题突破+限时集训(新高考专用)
8 . 已知 和
和 的一些物理性质如下表所示:
的一些物理性质如下表所示:
(1)分离这两种物质的混合物可采用的方法是___________ (填字母)。
a、过滤 b、分液 c、蒸发 d、蒸镏
(2)该分离方法需要用到的主要玻璃仪器是___________ 、___________ 、___________ 、___________ 、___________ 、牛角管。
 和
和 的一些物理性质如下表所示:
的一些物理性质如下表所示:| 物质 | 熔点/℃ | 沸点/℃ | 密度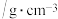 | 水溶性 |
 | 54 | 238 | 1.1581 | 难溶 |
 | -10 | 212 | 1.1622 | 难溶 |
(1)分离这两种物质的混合物可采用的方法是
a、过滤 b、分液 c、蒸发 d、蒸镏
(2)该分离方法需要用到的主要玻璃仪器是
您最近一年使用:0次
22-23高二下·全国·课时练习
名校
解题方法
9 . 现拟分离乙酸乙酯、乙酸和乙醇的混合物,下图是分离操作步骤流程图。

已知各物质的沸点:乙酸乙酯 77.1 ℃ 乙醇 78.5 ℃ 乙酸 118 ℃
请回答下列问题:
(1)试剂(a)为_______ ,试剂(b)为_______ 。
(2)图中的分离方法分别是①为_______ ;②为_______ ;③为_______ 。
(3)写出下列有机物的化学式:A_______ 、B_______ 、C_______ 、D_______ 、E_______ 。

已知各物质的沸点:乙酸乙酯 77.1 ℃ 乙醇 78.5 ℃ 乙酸 118 ℃
请回答下列问题:
(1)试剂(a)为
(2)图中的分离方法分别是①为
(3)写出下列有机物的化学式:A
您最近一年使用:0次
10 . 现有直馏汽油和裂化汽油各一瓶。已知:裂化汽油主要成分为烷烃、烯烃,直馏汽油主要成分为烷烃、环烷烃、芳香烃。
(1)请从下列试剂中选择最合理的试剂区别上述两种汽油。所选试剂是_______ (填字母)。
A.酸性 溶液 B.乙醇 C.溴水
溶液 B.乙醇 C.溴水
(2)加入所选试剂后,直馏汽油中观察到的现象是_______ ;裂化汽油中观察到的现象是_______ 。
(1)请从下列试剂中选择最合理的试剂区别上述两种汽油。所选试剂是
A.酸性
 溶液 B.乙醇 C.溴水
溶液 B.乙醇 C.溴水(2)加入所选试剂后,直馏汽油中观察到的现象是
您最近一年使用:0次



