1 . 三氯化铬是常用的媒染剂和催化剂,易潮解,高温下易被氧气氧化。实验室中用如图所示装置(夹持装置略)制取三氯化铬( 、
、 为气流控制开关)。
为气流控制开关)。

已知:① 气体有毒,能被
气体有毒,能被 溶液吸收,
溶液吸收,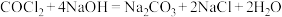 。
。
② 在碱性条件下具有较强还原性,能被
在碱性条件下具有较强还原性,能被 等氧化剂氧化为
等氧化剂氧化为 。
。
③某些物质的颜色、状态、熔点、沸点如下表:
回答下列问题:
(1)制备 的实验步骤如下:
的实验步骤如下:
i.连接装置,检查装置气密性,装入药品,打开 、
、 ,通入
,通入 并通入冷凝水。
并通入冷凝水。
ii.加热管式炉的反应管至 。
。
iii.关闭 (
( 为打开状态),加热
为打开状态),加热 ,温度保持在
,温度保持在 之间。
之间。
iv.加热反应管继续升温至 ,反应所生成的
,反应所生成的 将升华并凝聚在反应管的右端,直到装置
将升华并凝聚在反应管的右端,直到装置 中反应完全,切断管式炉的电源。
中反应完全,切断管式炉的电源。
v.停止加热装置 ,打开
,打开 ,关闭
,关闭 ,继续通入
,继续通入 直至装置
直至装置 中无液滴滴下,停止通入冷凝水。
中无液滴滴下,停止通入冷凝水。
vi.装置冷却后,结束制备实验。
①步骤i中,通 的作用为
的作用为________ 。步骤ⅲ中加热 通常采用的加热方式是
通常采用的加热方式是_________ 。
②步骤iv中装置 中反应完全的标志是
中反应完全的标志是___________ 。
(2)装置 中发生反应的化学方程式为
中发生反应的化学方程式为___________ 。
(3)装置 、
、 的作用是
的作用是___________ 。
(4)准确称取 无水三氯化铬样品置于
无水三氯化铬样品置于 烧杯中,加水定容于
烧杯中,加水定容于 容量瓶中。移取
容量瓶中。移取 于
于 碘量瓶中,加热至沸,慢慢加入
碘量瓶中,加热至沸,慢慢加入 (足量),待溶液变成黄色后,再加水至
(足量),待溶液变成黄色后,再加水至 ,充分加热煮沸,冷却后用
,充分加热煮沸,冷却后用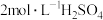 溶液中和至呈橙红色,再加入足量
溶液中和至呈橙红色,再加入足量 溶液,加塞摇匀充分反应后,铬元素只以
溶液,加塞摇匀充分反应后,铬元素只以 存在,暗处静置
存在,暗处静置 后,加入指示剂,用
后,加入指示剂,用 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 标准溶液
标准溶液 (已知杂质不参加反应,且
(已知杂质不参加反应,且 )。
)。
①向碘量瓶中加入 后,发生反应的离子方程式为
后,发生反应的离子方程式为___________ 。
②该样品中无水三氯化铬的质量分数为___________ (用含 、
、 、
、 的代数式表示)。
的代数式表示)。
 、
、 为气流控制开关)。
为气流控制开关)。
已知:①
 气体有毒,能被
气体有毒,能被 溶液吸收,
溶液吸收,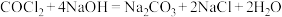 。
。②
 在碱性条件下具有较强还原性,能被
在碱性条件下具有较强还原性,能被 等氧化剂氧化为
等氧化剂氧化为 。
。③某些物质的颜色、状态、熔点、沸点如下表:
| 物质 | 颜色、状态 | 熔点 | 沸点/ |
 | 绿色晶体 | — | — |
 | 紫色晶体 | — | — |
 | 无色液体 | 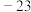 | 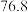 |
(1)制备
 的实验步骤如下:
的实验步骤如下:i.连接装置,检查装置气密性,装入药品,打开
 、
、 ,通入
,通入 并通入冷凝水。
并通入冷凝水。ii.加热管式炉的反应管至
 。
。iii.关闭
 (
( 为打开状态),加热
为打开状态),加热 ,温度保持在
,温度保持在 之间。
之间。iv.加热反应管继续升温至
 ,反应所生成的
,反应所生成的 将升华并凝聚在反应管的右端,直到装置
将升华并凝聚在反应管的右端,直到装置 中反应完全,切断管式炉的电源。
中反应完全,切断管式炉的电源。v.停止加热装置
 ,打开
,打开 ,关闭
,关闭 ,继续通入
,继续通入 直至装置
直至装置 中无液滴滴下,停止通入冷凝水。
中无液滴滴下,停止通入冷凝水。vi.装置冷却后,结束制备实验。
①步骤i中,通
 的作用为
的作用为 通常采用的加热方式是
通常采用的加热方式是②步骤iv中装置
 中反应完全的标志是
中反应完全的标志是(2)装置
 中发生反应的化学方程式为
中发生反应的化学方程式为(3)装置
 、
、 的作用是
的作用是(4)准确称取
 无水三氯化铬样品置于
无水三氯化铬样品置于 烧杯中,加水定容于
烧杯中,加水定容于 容量瓶中。移取
容量瓶中。移取 于
于 碘量瓶中,加热至沸,慢慢加入
碘量瓶中,加热至沸,慢慢加入 (足量),待溶液变成黄色后,再加水至
(足量),待溶液变成黄色后,再加水至 ,充分加热煮沸,冷却后用
,充分加热煮沸,冷却后用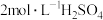 溶液中和至呈橙红色,再加入足量
溶液中和至呈橙红色,再加入足量 溶液,加塞摇匀充分反应后,铬元素只以
溶液,加塞摇匀充分反应后,铬元素只以 存在,暗处静置
存在,暗处静置 后,加入指示剂,用
后,加入指示剂,用 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗 标准溶液
标准溶液 (已知杂质不参加反应,且
(已知杂质不参加反应,且 )。
)。①向碘量瓶中加入
 后,发生反应的离子方程式为
后,发生反应的离子方程式为②该样品中无水三氯化铬的质量分数为
 、
、 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
2 . 氯化钠(NaCl)是生活中常用的化学品,也是重要的化工生产原料。粗盐中一般含有 、
、 、
、 和
和 杂质。粗盐制得精盐的过程如下:
杂质。粗盐制得精盐的过程如下:

下列说法错误的是
 、
、 、
、 和
和 杂质。粗盐制得精盐的过程如下:
杂质。粗盐制得精盐的过程如下:
下列说法错误的是
A.试剂I是足量 溶液 溶液 |
| B.操作a所需的玻璃仪器有烧杯、漏斗、玻璃棒 |
C.试剂II为碳酸钠,其作用为除去溶液中的 和 和 |
| D.用pH试纸检验溶液B,可发现溶液B显碱性 |
您最近一年使用:0次
2023-11-10更新
|
364次组卷
|
6卷引用:山西省部分学校2023-2024学年高一上学期11月期中联合考试化学试题
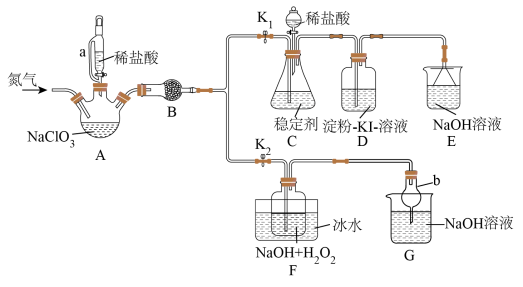
3 . 二氧化氯( )是目前国际上公认的第四代高效、无毒的广谱消毒剂,用如图所示装置(夹持装置已省略)制备、吸收、释放
)是目前国际上公认的第四代高效、无毒的广谱消毒剂,用如图所示装置(夹持装置已省略)制备、吸收、释放 ,并探究其性质。(已知
,并探究其性质。(已知 ,实验室可用稳定剂吸收
,实验室可用稳定剂吸收 ,生成
,生成 ,使用时加酸只释放出
,使用时加酸只释放出 一种气体)。
一种气体)。
已知:① 沸点为9.9℃,可溶于水,浓度较高时易发生爆炸;
沸点为9.9℃,可溶于水,浓度较高时易发生爆炸;
② 饱和溶液低于38℃时析出
饱和溶液低于38℃时析出 ,高于38℃时析出
,高于38℃时析出 ,高于60℃时
,高于60℃时 分解为
分解为 和NaCl。回答下列问题:
和NaCl。回答下列问题:
(1)仪器a的名称是______ ;仪器b的作用是______ 。
(2)按图组装好仪器后,首先应该进行的操作是______ ,实验过程中需持续通入一定量的氮气,其目的是将装置A产生的气体赶入吸收装置被充分吸收,还有______ 。
(3)打开仪器a的活塞,装置A中发生反应,生成 、
、 、NaCl等,写出装置A中发生反应的化学方程式:
、NaCl等,写出装置A中发生反应的化学方程式:_____________ ,关闭仪器a的活塞, 在装置C中被稳定剂完全吸收,此时观察到装置D中溶液的颜色不变,其中的原因可能是
在装置C中被稳定剂完全吸收,此时观察到装置D中溶液的颜色不变,其中的原因可能是__________________ 。
(4)向装置C中滴加稀盐酸,反应剧烈,若将稀盐酸换成等pH的硫酸,开始反应缓慢,稍后一段时间产生气体速率迅速加快,产生气体速率迅速加快的原因可能是____________ 。
(5)装置F的目的是制备 ,装置F中加入NaOH溶液的目的有两个,其一为用作反应物,其二为
,装置F中加入NaOH溶液的目的有两个,其一为用作反应物,其二为______ ,从装置F广口瓶内的溶液中获得晶体 的操作步骤是蒸发浓缩、
的操作步骤是蒸发浓缩、______ 、洗涤、干燥。
(6)城市饮用水处理新技术用 替代
替代 ,如果以单位质量的氧化剂所得到的电子数来表示消毒效率(
,如果以单位质量的氧化剂所得到的电子数来表示消毒效率( ),那么消毒杀菌剂消毒效率:
),那么消毒杀菌剂消毒效率:
______ 。
 )是目前国际上公认的第四代高效、无毒的广谱消毒剂,用如图所示装置(夹持装置已省略)制备、吸收、释放
)是目前国际上公认的第四代高效、无毒的广谱消毒剂,用如图所示装置(夹持装置已省略)制备、吸收、释放 ,并探究其性质。(已知
,并探究其性质。(已知 ,实验室可用稳定剂吸收
,实验室可用稳定剂吸收 ,生成
,生成 ,使用时加酸只释放出
,使用时加酸只释放出 一种气体)。
一种气体)。
已知:①
 沸点为9.9℃,可溶于水,浓度较高时易发生爆炸;
沸点为9.9℃,可溶于水,浓度较高时易发生爆炸;②
 饱和溶液低于38℃时析出
饱和溶液低于38℃时析出 ,高于38℃时析出
,高于38℃时析出 ,高于60℃时
,高于60℃时 分解为
分解为 和NaCl。回答下列问题:
和NaCl。回答下列问题:(1)仪器a的名称是
(2)按图组装好仪器后,首先应该进行的操作是
(3)打开仪器a的活塞,装置A中发生反应,生成
 、
、 、NaCl等,写出装置A中发生反应的化学方程式:
、NaCl等,写出装置A中发生反应的化学方程式: 在装置C中被稳定剂完全吸收,此时观察到装置D中溶液的颜色不变,其中的原因可能是
在装置C中被稳定剂完全吸收,此时观察到装置D中溶液的颜色不变,其中的原因可能是(4)向装置C中滴加稀盐酸,反应剧烈,若将稀盐酸换成等pH的硫酸,开始反应缓慢,稍后一段时间产生气体速率迅速加快,产生气体速率迅速加快的原因可能是
(5)装置F的目的是制备
 ,装置F中加入NaOH溶液的目的有两个,其一为用作反应物,其二为
,装置F中加入NaOH溶液的目的有两个,其一为用作反应物,其二为 的操作步骤是蒸发浓缩、
的操作步骤是蒸发浓缩、(6)城市饮用水处理新技术用
 替代
替代 ,如果以单位质量的氧化剂所得到的电子数来表示消毒效率(
,如果以单位质量的氧化剂所得到的电子数来表示消毒效率( ),那么消毒杀菌剂消毒效率:
),那么消毒杀菌剂消毒效率:
您最近一年使用:0次
2023-08-31更新
|
142次组卷
|
3卷引用:山西省大同市2023-2024学年高三上学期开学质量检测化学试题
解题方法
4 . 某学习小组以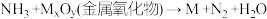 反应为原理设计实验测定金属M的相对原子质量,实验装置如图。
反应为原理设计实验测定金属M的相对原子质量,实验装置如图。
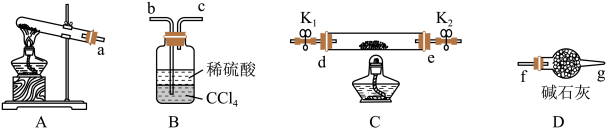
已知,MxOy可为CuO、Fe2O3、MgO;氨气不溶于有机溶剂CCl4.
(1)实验步骤:
①连接实验装置,上述仪器接口顺序为a→_____ (按气流方向从左到右,仪器不重复使用,填标号),检验装置的气密性;
②将m1g纯净的金属氧化物MxOy装入玻璃管C中;
③打开K1和K2,点燃装置A中酒精灯,当装置中充满NH3后再点燃装置C中酒精灯,加热至MxOy反应完全;
④熄灭C中酒精灯,冷却至室温;熄灭A中酒精灯;
⑤冷却至室温后,称量得C中玻璃管剩余固体的质量为m2g。
(2)利用装置A制取氨气的化学方程式为_____ ,列举出一种检验氨气的试剂:_____ 。
(3)仪器D的名称为_____ ;装置B中加入的CCl4的作用是_____ 。
(4)若金属氧化物为CuO,则装置C中发生反应的化学方程式为_____ ,该反应中NH3表现出_____ 性,根据实验记录,算得铜的相对原子质量为_____ (用含m1、m2的式子表示)。
(5)若MxOy未完全反应,则会导致测得的金属M的相对原子质量_____ (填“偏大”、“偏小”或“无影响”)。
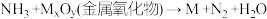 反应为原理设计实验测定金属M的相对原子质量,实验装置如图。
反应为原理设计实验测定金属M的相对原子质量,实验装置如图。
已知,MxOy可为CuO、Fe2O3、MgO;氨气不溶于有机溶剂CCl4.
(1)实验步骤:
①连接实验装置,上述仪器接口顺序为a→
②将m1g纯净的金属氧化物MxOy装入玻璃管C中;
③打开K1和K2,点燃装置A中酒精灯,当装置中充满NH3后再点燃装置C中酒精灯,加热至MxOy反应完全;
④熄灭C中酒精灯,冷却至室温;熄灭A中酒精灯;
⑤冷却至室温后,称量得C中玻璃管剩余固体的质量为m2g。
(2)利用装置A制取氨气的化学方程式为
(3)仪器D的名称为
(4)若金属氧化物为CuO,则装置C中发生反应的化学方程式为
(5)若MxOy未完全反应,则会导致测得的金属M的相对原子质量
您最近一年使用:0次
2023-07-09更新
|
93次组卷
|
2卷引用:山西省忻州市2022-2023学年高一下学期7月期末考试化学试题
5 . 利用工业碱渣( )治理硫酸尾气(SO2),并制取硫代硫酸钠(Na2S2O3)的工艺如图。
)治理硫酸尾气(SO2),并制取硫代硫酸钠(Na2S2O3)的工艺如图。
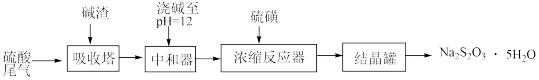
回答下列问题:
(1)吸收塔中可能发生的副反应的化学方程式为___________ 、___________ 。
(2)“浇碱”加入的试剂为___________ ,目的是___________ 。
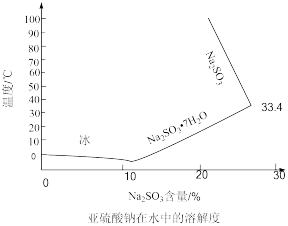
(3)已知Na2S2O3在水中的溶解度曲线如图,则从结晶罐中得到 的操作为
的操作为___________ 。
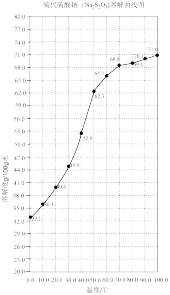
(4)已知在浓缩反应器中可直接获取亚硫酸钠固体,亚硫酸钠在水中的溶解度曲线如图,无水亚硫酸钠易被空气中的氧气氧化,则浓缩时温度应控制在___________ 左右,理由是___________ 。
(5)可用碘水测定产品中 的纯度,发生反应
的纯度,发生反应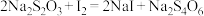 ,测定过程:取产品ag,加蒸馏水溶解后,配制成250mL溶液,取25.00mL于锥形瓶中,滴加几滴淀粉溶液,再逐滴滴加0.005mol/L的碘水,边滴边振荡,直至滴加最后半滴碘水,溶液颜色恰好从无色变为蓝色,且半分钟内不变色,此时消耗碘水VmL。测得产品中
,测定过程:取产品ag,加蒸馏水溶解后,配制成250mL溶液,取25.00mL于锥形瓶中,滴加几滴淀粉溶液,再逐滴滴加0.005mol/L的碘水,边滴边振荡,直至滴加最后半滴碘水,溶液颜色恰好从无色变为蓝色,且半分钟内不变色,此时消耗碘水VmL。测得产品中 的纯度为
的纯度为___________ (用含a、V的式子表示)。
 )治理硫酸尾气(SO2),并制取硫代硫酸钠(Na2S2O3)的工艺如图。
)治理硫酸尾气(SO2),并制取硫代硫酸钠(Na2S2O3)的工艺如图。
回答下列问题:
(1)吸收塔中可能发生的副反应的化学方程式为
(2)“浇碱”加入的试剂为
(3)已知Na2S2O3在水中的溶解度曲线如图,则从结晶罐中得到
 的操作为
的操作为
(4)已知在浓缩反应器中可直接获取亚硫酸钠固体,亚硫酸钠在水中的溶解度曲线如图,无水亚硫酸钠易被空气中的氧气氧化,则浓缩时温度应控制在

(5)可用碘水测定产品中
 的纯度,发生反应
的纯度,发生反应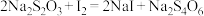 ,测定过程:取产品ag,加蒸馏水溶解后,配制成250mL溶液,取25.00mL于锥形瓶中,滴加几滴淀粉溶液,再逐滴滴加0.005mol/L的碘水,边滴边振荡,直至滴加最后半滴碘水,溶液颜色恰好从无色变为蓝色,且半分钟内不变色,此时消耗碘水VmL。测得产品中
,测定过程:取产品ag,加蒸馏水溶解后,配制成250mL溶液,取25.00mL于锥形瓶中,滴加几滴淀粉溶液,再逐滴滴加0.005mol/L的碘水,边滴边振荡,直至滴加最后半滴碘水,溶液颜色恰好从无色变为蓝色,且半分钟内不变色,此时消耗碘水VmL。测得产品中 的纯度为
的纯度为
您最近一年使用:0次
6 . 某实验小组用如下装置模拟Mg与N2反应制取Mg3N2,已知装置数量可满足需要。Mg3N2为浅黄色粉末,易与水反应;氨气在加热时可还原氧化铜生成铜和氮气,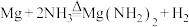 。回答下列问题:
。回答下列问题:
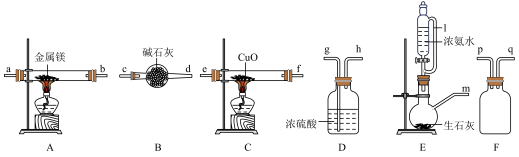
(1)装置“l”名称为___________ 。
(2)各装置接口顺序为m→___________ 。
(3)装置C中发生反应的化学方程式为___________ 。
(4)装置B的作用是___________ 。
(5)实验开始时应先点燃___________ 处酒精灯(填“A”或“C”),理由是___________ 。
(6)有人认为装置D可用B代替,该观点___________ (填“正确”或“错误”),原因是___________ 。
(7)已知Mg3N2与H2O反应无电子转移,试设计实验验证装置A中有Mg3N2生成:___________ 。
 。回答下列问题:
。回答下列问题:
(1)装置“l”名称为
(2)各装置接口顺序为m→
(3)装置C中发生反应的化学方程式为
(4)装置B的作用是
(5)实验开始时应先点燃
(6)有人认为装置D可用B代替,该观点
(7)已知Mg3N2与H2O反应无电子转移,试设计实验验证装置A中有Mg3N2生成:
您最近一年使用:0次
名校
解题方法
7 . 氮化铬(CrN)具有高的硬度和良好的耐磨性。实验室可利用 与
与 反应来制备氮化铬,可选择的装置如下图。下列说法错误的是
反应来制备氮化铬,可选择的装置如下图。下列说法错误的是 为紫色单斜晶体,熔点为383℃,易升华,高温下易被氧气氧化,极易水解,CrN难溶于水,熔点1282℃
为紫色单斜晶体,熔点为383℃,易升华,高温下易被氧气氧化,极易水解,CrN难溶于水,熔点1282℃
 与
与 反应来制备氮化铬,可选择的装置如下图。下列说法错误的是
反应来制备氮化铬,可选择的装置如下图。下列说法错误的是
 为紫色单斜晶体,熔点为383℃,易升华,高温下易被氧气氧化,极易水解,CrN难溶于水,熔点1282℃
为紫色单斜晶体,熔点为383℃,易升华,高温下易被氧气氧化,极易水解,CrN难溶于水,熔点1282℃| A.装置的连接顺序为:A→D→E→B→C→E |
| B.A装置中分液漏斗内盛放的是氯化铵溶液,圆底烧瓶中盛放的是氢氧化钠溶液 |
C.B与C之间采用粗玻璃管的目的是防止升华的 冷凝堵塞导管 冷凝堵塞导管 |
D.制得的CrN中往往含有少量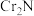 ,生成 ,生成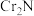 的化学方程式为: 的化学方程式为: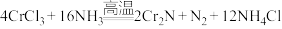 |
您最近一年使用:0次
2023-04-20更新
|
615次组卷
|
5卷引用:山西省大同市第一中学校2022-2023学年高一下学期5月月考化学试题
8 .  常用来配制金属蚀刻剂。某兴趣小组设计如图实验装置制备氯化铁晶体。
常用来配制金属蚀刻剂。某兴趣小组设计如图实验装置制备氯化铁晶体。
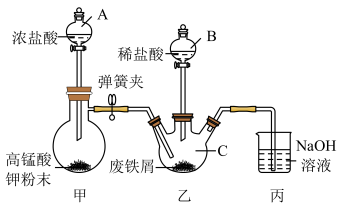
(1)仪器C的名称为_______ 。废铁屑使用前要用热的纯碱溶液浸泡,目的是_______ 。
(2)组装好装置后,如何检验其气密性?_______ 。
(3)实验开始时应先打开_______ (填“A”或“B”)的活塞,再_______ (填“打开”或“关闭”)弹簧夹。
(4)C中生成 的离子方程式为
的离子方程式为_______ 。
(5)待反应完成后,将乙中的溶液在氯化氢气流中蒸发浓缩,然后冷却结晶、过滤、洗涤、干燥即得 晶体。在氯化氢气流中蒸发浓缩的原因是
晶体。在氯化氢气流中蒸发浓缩的原因是_______ 。
(6)气态 分子以双聚形式存在,其结构式为
分子以双聚形式存在,其结构式为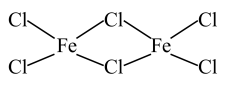 。
。 原子的配位数为
原子的配位数为_______ ,画出其中的配位键_______ 。
 常用来配制金属蚀刻剂。某兴趣小组设计如图实验装置制备氯化铁晶体。
常用来配制金属蚀刻剂。某兴趣小组设计如图实验装置制备氯化铁晶体。
(1)仪器C的名称为
(2)组装好装置后,如何检验其气密性?
(3)实验开始时应先打开
(4)C中生成
 的离子方程式为
的离子方程式为(5)待反应完成后,将乙中的溶液在氯化氢气流中蒸发浓缩,然后冷却结晶、过滤、洗涤、干燥即得
 晶体。在氯化氢气流中蒸发浓缩的原因是
晶体。在氯化氢气流中蒸发浓缩的原因是(6)气态
 分子以双聚形式存在,其结构式为
分子以双聚形式存在,其结构式为 。
。 原子的配位数为
原子的配位数为
您最近一年使用:0次
名校
解题方法
9 . 苯甲酸乙酯是一种有芳香气味,无色液体,沸点为212℃,微溶于水,易溶于乙醚,常用作玫瑰、橙花、香石竹等化妆香精的调配,也用作纤维素脂、纤维素醚、树脂等的溶剂。
I.实验室利用苯甲酸、乙醇、环己烷和浓硫酸混合加热制备苯甲酸乙酯,此反应是个可逆反应,装置如图所示(省略了部分装置),
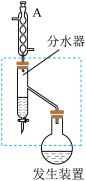
(1)写出实验室制备苯甲酸乙酯的化学方程式_______ 。
(2)加入的环己烷可提高苯甲酸乙酯产率的原因是_______ 。
(3)装置A的名称是_______ ,其作用是_______ 。
(4)及时打开分水器下端旋塞将水层移出反应体系的目的是_______ 。
II.从反应混合物中分离苯甲酸乙酯、苯甲酸和环己烷的流程如图。
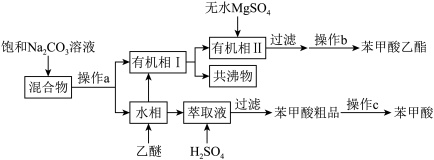
已知:环己烷沸点为80.8℃;乙醚的密度为0.834g/cm3,沸点34.5℃;乙醚-环己烷-水共沸物的沸点为62.1℃。
(5)向混合物中加入饱和Na2CO3溶液的目的是_______ 。
(6)操作b和操作c分别是_______ 、_______ 。
I.实验室利用苯甲酸、乙醇、环己烷和浓硫酸混合加热制备苯甲酸乙酯,此反应是个可逆反应,装置如图所示(省略了部分装置),

(1)写出实验室制备苯甲酸乙酯的化学方程式
(2)加入的环己烷可提高苯甲酸乙酯产率的原因是
(3)装置A的名称是
(4)及时打开分水器下端旋塞将水层移出反应体系的目的是
II.从反应混合物中分离苯甲酸乙酯、苯甲酸和环己烷的流程如图。

已知:环己烷沸点为80.8℃;乙醚的密度为0.834g/cm3,沸点34.5℃;乙醚-环己烷-水共沸物的沸点为62.1℃。
(5)向混合物中加入饱和Na2CO3溶液的目的是
(6)操作b和操作c分别是
您最近一年使用:0次
2022-11-19更新
|
265次组卷
|
2卷引用:山西省运城市2022-2023学年高三上学期期中调研测试化学试题
解题方法
10 . 某课外小组设计如图所示装置(夹持仪器略)进行铁与水的反应并验证气体产物的实验。
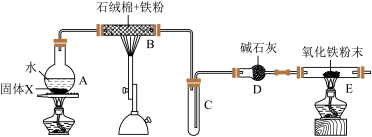
下列有关说法错误的是

下列有关说法错误的是
| A.固体X可以为碎瓷片,目的是防止加热时发生暴沸 |
B.装置B中发生反应 |
| C.应先加热装置A,当装置C中有液滴出现时,再加热装置B |
| D.加热装置E之前须在出口收集气体并检验气体的纯度 |
您最近一年使用:0次



