1 . 完成下列实验,所选装置正确的是
| A | B | C | D | |
| 实验目的 | 检查装置气密性 | 实验室用纯碱和稀硫酸制备二氧化碳 | 用已知浓度的氢氧化钠溶液测定未知浓度盐酸 | 选择合适的试剂,可分别制取少量CO2、NO和O2 |
| 实验 装置 | 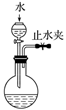 | 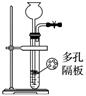 | 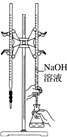 | 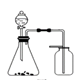 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2018-11-20更新
|
431次组卷
|
5卷引用:天津市河北区2021届高三一模考试化学试题
天津市河北区2021届高三一模考试化学试题【全国百强校】黑龙江省哈尔滨市第六中学2019届高三上学期期中考试化学试题(已下线)押山东卷第05题 实验装置的评价-备战2021年高考化学临考题号押题(山东卷)福建省宁化第一中学2021-2022学年高三上学期第二次阶段考试化学试题(已下线)专题13 装置气密性的检查方法-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)
名校
2 . 以 为原料制备氧钒(Ⅳ)碱式碳酸铵
为原料制备氧钒(Ⅳ)碱式碳酸铵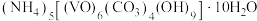 。其过程为:
。其过程为:
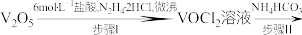 氧钒(Ⅳ)碱式碳酸铵粗产品
氧钒(Ⅳ)碱式碳酸铵粗产品
已知 能被
能被 氧化,回答下列问题:
氧化,回答下列问题:
(1)步骤I的反应装置如图(夹持及加热装置略去)___________ 。
②步骤Ⅰ生成 的同时,还生成一种无色无污染的气体,该反应的化学方程式为
的同时,还生成一种无色无污染的气体,该反应的化学方程式为___________ 。
(2)步骤Ⅱ可在如下图装置中进行。___________ 。
②实验开始时,关闭 ,打开
,打开 ,其目的是
,其目的是___________ 。当___________ 时(写实验现象),再关闭 ,打开
,打开 ,充分反应,静置,得到固体。
,充分反应,静置,得到固体。
(3)测定产品纯度
称取mg氧钒(Ⅳ)碱式碳酸铵粗产品经处理后,钒(Ⅴ)元素均以 的形式存在,然后用
的形式存在,然后用 标准溶液滴定达终点时,消耗体积为
标准溶液滴定达终点时,消耗体积为 。
。
(已知: )
)
①产品中氧钒(Ⅳ)碱式碳酸铵(摩尔质量为 )的质量分数为
)的质量分数为___________ 。
②下列情况会导致产品纯度偏小的是___________ (填标号)。
A.滴定达终点时,俯视刻度线读数
B.用标准液润洗滴定管后,液体从上口倒出
C.滴定达终点时,发现滴定管尖嘴内有气泡生成
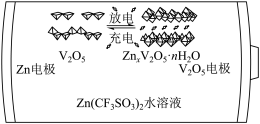
(4)一种以 和Zn为电极、
和Zn为电极、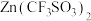 水溶液为电解质的电池,其示意图如下所示。放电时,
水溶液为电解质的电池,其示意图如下所示。放电时, 可插入
可插入 层间形成
层间形成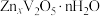 。
。___________ 。
 为原料制备氧钒(Ⅳ)碱式碳酸铵
为原料制备氧钒(Ⅳ)碱式碳酸铵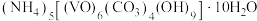 。其过程为:
。其过程为: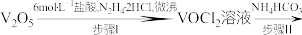 氧钒(Ⅳ)碱式碳酸铵粗产品
氧钒(Ⅳ)碱式碳酸铵粗产品已知
 能被
能被 氧化,回答下列问题:
氧化,回答下列问题:(1)步骤I的反应装置如图(夹持及加热装置略去)
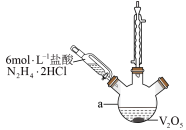
②步骤Ⅰ生成
 的同时,还生成一种无色无污染的气体,该反应的化学方程式为
的同时,还生成一种无色无污染的气体,该反应的化学方程式为(2)步骤Ⅱ可在如下图装置中进行。
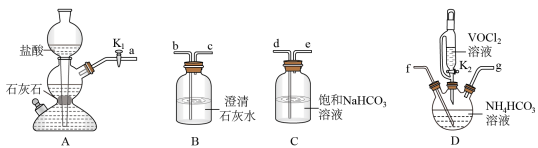
②实验开始时,关闭
 ,打开
,打开 ,其目的是
,其目的是 ,打开
,打开 ,充分反应,静置,得到固体。
,充分反应,静置,得到固体。(3)测定产品纯度
称取mg氧钒(Ⅳ)碱式碳酸铵粗产品经处理后,钒(Ⅴ)元素均以
 的形式存在,然后用
的形式存在,然后用 标准溶液滴定达终点时,消耗体积为
标准溶液滴定达终点时,消耗体积为 。
。(已知:
 )
)①产品中氧钒(Ⅳ)碱式碳酸铵(摩尔质量为
 )的质量分数为
)的质量分数为②下列情况会导致产品纯度偏小的是
A.滴定达终点时,俯视刻度线读数
B.用标准液润洗滴定管后,液体从上口倒出
C.滴定达终点时,发现滴定管尖嘴内有气泡生成
(4)一种以
 和Zn为电极、
和Zn为电极、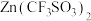 水溶液为电解质的电池,其示意图如下所示。放电时,
水溶液为电解质的电池,其示意图如下所示。放电时, 可插入
可插入 层间形成
层间形成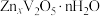 。
。
您最近一年使用:0次
名校
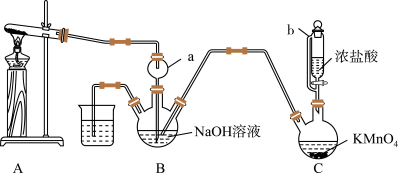
3 . 肼(N2H4)可作火箭发射的燃料。某实验兴趣小组利用氨气与次氯酸钠反应制备N2H4,并探究N2H4的性质,其制备装置如图所示。
(1)N2H4的电子式是_________________________________ 。
(2)仪器b的名称为_________________________ ,仪器a的作用是_________________________________ 。
(3)装置 中发生反应的化学方程式为
中发生反应的化学方程式为_________________________________ 。
(4)采用上述装置制备N2H4时产率较低,可能的原因是_________________________________ 。
(5)写出装置 中生成N2H4的化学方程式
中生成N2H4的化学方程式_________________________________ 。
(6)探究N2H4的性质。将制得的N2H4分离提纯后,进行如下实验。
【提出假设】黑色固体可能是Ag、Ag2O中的一种或两种。
【实验验证】设计如下方案,进行实验。
(7)肼是一种常用的还原剂,可用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1kg肼可除去水中溶解的O2的质量为_________________ kg。
(1)N2H4的电子式是
(2)仪器b的名称为
(3)装置
 中发生反应的化学方程式为
中发生反应的化学方程式为(4)采用上述装置制备N2H4时产率较低,可能的原因是
(5)写出装置
 中生成N2H4的化学方程式
中生成N2H4的化学方程式(6)探究N2H4的性质。将制得的N2H4分离提纯后,进行如下实验。
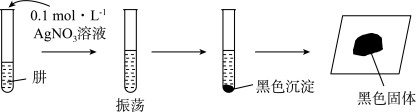
【提出假设】黑色固体可能是Ag、Ag2O中的一种或两种。
【实验验证】设计如下方案,进行实验。
操作 | 现象 | 结论 |
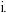 取少量黑色固体于试管中,加入足量 取少量黑色固体于试管中,加入足量 | 黑色固体部分溶解 | 黑色固体中有Ag2O |
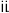 取少量黑色固体于试管中,加入足量稀硝酸,振荡 取少量黑色固体于试管中,加入足量稀硝酸,振荡 | 黑色固体是Ag和Ag2O,则肼具有的性质是碱性和 |
(7)肼是一种常用的还原剂,可用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1kg肼可除去水中溶解的O2的质量为
您最近一年使用:0次
2024-04-20更新
|
465次组卷
|
2卷引用:2024届天津市宁河区芦台第一中学高三下学期第三次模拟化学试题
4 . 硫代硫酸钠是一种重要的化工产品。某兴趣小组制备硫代硫酸钠晶体(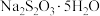 )的实验装置如下图所示(省略夹持装置):
)的实验装置如下图所示(省略夹持装置):

主要实验步骤为:
①检查装置气密性,按图示加入试剂;
②先向A中烧瓶滴加浓 ,再向C中烧瓶加入
,再向C中烧瓶加入 和
和 混合溶液;
混合溶液;
③待 和
和 完全消耗后,结束反应。过滤C中混合物,滤液经
完全消耗后,结束反应。过滤C中混合物,滤液经一系列实验操作 后得到产品。
已知:
i.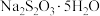 是无色透明晶体,易溶于水,其稀溶液与
是无色透明晶体,易溶于水,其稀溶液与 溶液混合无沉淀生成;
溶液混合无沉淀生成;
ii.向 和
和 混合溶液中通入
混合溶液中通入 可制得
可制得 ,所得产品常含有少量
,所得产品常含有少量 和
和 。
。
回答下列问题:
(1)仪器a的名称是_______ ;B、D装置的作用是_______ 。
(2)上述实验步骤③中的一系列实验操作 主要有_______ 、冷却结晶、过滤、洗涤、干燥;E中的试剂是_______ 。
(3)为检验产品中是否含有 和
和 ,该小组设计了以下实验方案(所需试剂从稀
,该小组设计了以下实验方案(所需试剂从稀 、稀
、稀 、稀HCl、蒸馏水中选择),请将方案补充完整:取适量产品配成稀溶液,滴加足量
、稀HCl、蒸馏水中选择),请将方案补充完整:取适量产品配成稀溶液,滴加足量 溶液,有白色沉淀生成,向沉淀中滴加足量的
溶液,有白色沉淀生成,向沉淀中滴加足量的_______ ,若_______ (填实验现象),则可以确定产品中含有 和
和 。
。
(4)写出制备 的总反应的化学方程式
的总反应的化学方程式_______ 。
(5)称取样品29.10g,配成500mL溶液,取出250mL向其中加入足量稀硫酸,充分反应,静置、过滤、洗涤、干燥、称量得沉淀1.60g,则样品中硫代硫酸钠晶体的百分含量为_______ 。(保留到0.1%)
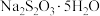 )的实验装置如下图所示(省略夹持装置):
)的实验装置如下图所示(省略夹持装置):
主要实验步骤为:
①检查装置气密性,按图示加入试剂;
②先向A中烧瓶滴加浓
 ,再向C中烧瓶加入
,再向C中烧瓶加入 和
和 混合溶液;
混合溶液;③待
 和
和 完全消耗后,结束反应。过滤C中混合物,滤液经
完全消耗后,结束反应。过滤C中混合物,滤液经已知:
i.
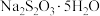 是无色透明晶体,易溶于水,其稀溶液与
是无色透明晶体,易溶于水,其稀溶液与 溶液混合无沉淀生成;
溶液混合无沉淀生成;ii.向
 和
和 混合溶液中通入
混合溶液中通入 可制得
可制得 ,所得产品常含有少量
,所得产品常含有少量 和
和 。
。回答下列问题:
(1)仪器a的名称是
(2)上述实验步骤③中的
(3)为检验产品中是否含有
 和
和 ,该小组设计了以下实验方案(所需试剂从稀
,该小组设计了以下实验方案(所需试剂从稀 、稀
、稀 、稀HCl、蒸馏水中选择),请将方案补充完整:取适量产品配成稀溶液,滴加足量
、稀HCl、蒸馏水中选择),请将方案补充完整:取适量产品配成稀溶液,滴加足量 溶液,有白色沉淀生成,向沉淀中滴加足量的
溶液,有白色沉淀生成,向沉淀中滴加足量的 和
和 。
。(4)写出制备
 的总反应的化学方程式
的总反应的化学方程式(5)称取样品29.10g,配成500mL溶液,取出250mL向其中加入足量稀硫酸,充分反应,静置、过滤、洗涤、干燥、称量得沉淀1.60g,则样品中硫代硫酸钠晶体的百分含量为
您最近一年使用:0次
名校
5 . 五水合硫代硫酸钠( )俗称海波、大苏打,为无色结晶或白色颗粒,在工业生产中有广泛的用途。某化学实验小组制备
)俗称海波、大苏打,为无色结晶或白色颗粒,在工业生产中有广泛的用途。某化学实验小组制备 ,并测定产品纯度,设计如下实验。回答下列问题:
,并测定产品纯度,设计如下实验。回答下列问题:
步骤I.制备
按如图所示装置(加热及夹持装置省略)进行实验,可得到 溶液,再经一系列步骤获得
溶液,再经一系列步骤获得 产品。
产品。
已知:S与Na2SO3在加热条件下可反应生成

(1)仪器a的名称为_______ ,装置A发生反应的化学反应方程式为_______ 。
(2)装置B的作用为_______ 。
(3)补充完成装置C中主要反应的离子方程式:①_______ ,②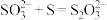 。
。
(4)C中溶液经过_______ 、过滤、洗涤、烘干,得 晶体(填实验操作)。
晶体(填实验操作)。
(5)D中浸有品红溶液的棉花的作用为_______ 。
步骤II. 测定产品纯度
准确称取上述产品12.40g于烧杯中,加入适量水配制成100mL待测液,取25.00mL待测液于锥形瓶中,以淀粉溶液作指示剂,用0.25mol·L-1的I2标准液滴定重复滴定3次;测得消耗I2标准液体积的平均值为20.00mL。(已知: )
)
(6)①滴定达到终点时的现象为_______ ,该产品中 的质量分数为
的质量分数为_______ 。
②以下说法中,能使测量结果偏低的是_______ 。
A.产品中硫代硫酸钠晶体失去部分结晶水
B.滴定前,装I2标准液的滴定管米用标准液润洗
C.滴定过程中,锥形瓶振荡太剧烈,有少量液滴溅出
D.滴定前平视读数,滴定后俯视读数
 )俗称海波、大苏打,为无色结晶或白色颗粒,在工业生产中有广泛的用途。某化学实验小组制备
)俗称海波、大苏打,为无色结晶或白色颗粒,在工业生产中有广泛的用途。某化学实验小组制备 ,并测定产品纯度,设计如下实验。回答下列问题:
,并测定产品纯度,设计如下实验。回答下列问题:步骤I.制备

按如图所示装置(加热及夹持装置省略)进行实验,可得到
 溶液,再经一系列步骤获得
溶液,再经一系列步骤获得 产品。
产品。已知:S与Na2SO3在加热条件下可反应生成


(1)仪器a的名称为
(2)装置B的作用为
(3)补充完成装置C中主要反应的离子方程式:①
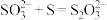 。
。(4)C中溶液经过
 晶体(填实验操作)。
晶体(填实验操作)。(5)D中浸有品红溶液的棉花的作用为
步骤II. 测定产品纯度
准确称取上述产品12.40g于烧杯中,加入适量水配制成100mL待测液,取25.00mL待测液于锥形瓶中,以淀粉溶液作指示剂,用0.25mol·L-1的I2标准液滴定重复滴定3次;测得消耗I2标准液体积的平均值为20.00mL。(已知:
 )
)(6)①滴定达到终点时的现象为
 的质量分数为
的质量分数为②以下说法中,能使测量结果偏低的是
A.产品中硫代硫酸钠晶体失去部分结晶水
B.滴定前,装I2标准液的滴定管米用标准液润洗
C.滴定过程中,锥形瓶振荡太剧烈,有少量液滴溅出
D.滴定前平视读数,滴定后俯视读数
您最近一年使用:0次
2022-09-17更新
|
929次组卷
|
7卷引用:天津市红桥区2023届高三第二次模拟考试化学试题
天津市红桥区2023届高三第二次模拟考试化学试题福建省泉州市2023届高三毕业班8月质量监测(一)化学试题福建省莆田第二中学2022-2023学年高三上学期一调考试化学试题(已下线)2022年辽宁高考真题化学试题变式题(实验综合题)(已下线)考点15 硫及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)福建省福州第七中学2023-2024学年高三上学期10月月考化学试题河南省焦作一中2023-2024学年高三上学期阶段检测化学试题(12月)
名校
6 . 科学家舍勒和戴维对氯气的制取和研究做出了重大贡献。某兴趣小组利用所给仪器在实验室制备纯净干燥的氯气,并模拟工业制漂白粉。请回答下列问题:
I.氯气的制备(装置如图所示)

(1)装置G的名称为_______ ,装置F的作用为_______ 。
(2)从图中选择合适装置制备并收集纯净干燥的氯气(仪器不重复使用),仪器连接顺序为_______ (填写仪器下方字母)。
II.漂白粉的制备( 装置如图所示)
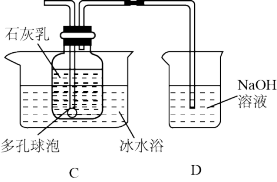
查阅资料可知:①氯气与碱反应放出热量;
②6Cl2+6Ca(OH)2 CaCl2+Ca(ClO3)2+6H2O。
CaCl2+Ca(ClO3)2+6H2O。
(3)装置C中发生反应的化学方程式为_______ 。
(4)多孔球泡的作用是_______ ,使用冰水浴的目的是_______ 。
(5)测定装置C中Ca(ClO)2物质的量浓度的方法如下:取C中溶液10.0mL于锥形瓶中,加入硫酸酸化,加入过量KI溶液,盖紧瓶塞并在暗处充分发生反应ClO-+2I-+2H+=I2+Cl- +H2O。用0.1000 mol·L-1Na2S2O3标准溶液滴定该锥形瓶中的溶液,滴入2~3滴淀粉指示剂,当加入最后一滴 Na2S2O3标准溶液时,其现象为_______ 达到滴定终点,此时消耗Na2S2O3溶液的体积为20.00mL。 (已知: I2+2S2O =2I- +S4O
=2I- +S4O 。该漂白粉溶液中Ca(ClO)2的物质的量浓度为
。该漂白粉溶液中Ca(ClO)2的物质的量浓度为_______ mol/L。(保留4位有效数字)
I.氯气的制备(装置如图所示)

(1)装置G的名称为
(2)从图中选择合适装置制备并收集纯净干燥的氯气(仪器不重复使用),仪器连接顺序为
II.漂白粉的制备( 装置如图所示)

查阅资料可知:①氯气与碱反应放出热量;
②6Cl2+6Ca(OH)2
 CaCl2+Ca(ClO3)2+6H2O。
CaCl2+Ca(ClO3)2+6H2O。(3)装置C中发生反应的化学方程式为
(4)多孔球泡的作用是
(5)测定装置C中Ca(ClO)2物质的量浓度的方法如下:取C中溶液10.0mL于锥形瓶中,加入硫酸酸化,加入过量KI溶液,盖紧瓶塞并在暗处充分发生反应ClO-+2I-+2H+=I2+Cl- +H2O。用0.1000 mol·L-1Na2S2O3标准溶液滴定该锥形瓶中的溶液,滴入2~3滴淀粉指示剂,当加入最后一滴 Na2S2O3标准溶液时,其现象为
 =2I- +S4O
=2I- +S4O 。该漂白粉溶液中Ca(ClO)2的物质的量浓度为
。该漂白粉溶液中Ca(ClO)2的物质的量浓度为
您最近一年使用:0次
2022-09-30更新
|
873次组卷
|
4卷引用:天津市实验中学滨海学校2022-2023学年高三上学期期中质量调查化学试题
7 . 硫氰化钾(KSCN)俗称玫瑰红酸钾,是一种用途广泛的化学药品。实验室模拟工业制备硫氰化钾的实验装置如下图所示:

已知:①CS2不溶于水,密度比水的大;②NH3不溶于CS2;③三颈烧瓶内盛放有CS2、水和催化剂。回答下列问题:
(1)制备NH4SCN溶液:
①实验前,经检验装置的气密性良好。其中装置B中的试剂是_____ 。三颈烧瓶的下层CS2液体必须浸没导气管口,目的是_____ 。
②实验开始时,打开K1,加热装置A、D,使A中产生的气体缓缓通入D中,发生反应
 (该反应比较缓慢),当看到
(该反应比较缓慢),当看到____ 现象时说明该反应接近完全。
(2)制备KSCN溶液:
①熄灭A处的酒精灯,关闭K2,移开水浴,将装置D继续加热至105℃,当NH4SCN完全分解后(NH4SCN ),打开K2,继续保持液温105℃,缓缓滴入适量的KOH溶液,发生反应的化学方程式为
),打开K2,继续保持液温105℃,缓缓滴入适量的KOH溶液,发生反应的化学方程式为_______ 。
②装置E中多孔球泡的作用是______ 。
(3)制备KSCN晶体:先滤去三颈烧瓶中的固体催化剂,_____ 、_____ 、过滤、洗涤、干燥,得到硫氰化钾晶体。
(4)测定晶体中KSCN的含量:称取 样品,配成
样品,配成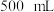 溶液。量取
溶液。量取 溶液于锥形瓶中,加入适量稀硝酸,再加入几滴
溶液于锥形瓶中,加入适量稀硝酸,再加入几滴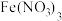 溶液作指示剂,用
溶液作指示剂,用 标准溶液滴定,达到滴定终点时消耗
标准溶液滴定,达到滴定终点时消耗 ,标准溶液
,标准溶液 。
。
①滴定时发生的反应: (白色)。则判断到达滴定终点的方法是
(白色)。则判断到达滴定终点的方法是____ 。
②晶体中KSCN的质量分数为_____ (计算结果精确至0.1%)。

已知:①CS2不溶于水,密度比水的大;②NH3不溶于CS2;③三颈烧瓶内盛放有CS2、水和催化剂。回答下列问题:
(1)制备NH4SCN溶液:
①实验前,经检验装置的气密性良好。其中装置B中的试剂是
②实验开始时,打开K1,加热装置A、D,使A中产生的气体缓缓通入D中,发生反应

 (该反应比较缓慢),当看到
(该反应比较缓慢),当看到(2)制备KSCN溶液:
①熄灭A处的酒精灯,关闭K2,移开水浴,将装置D继续加热至105℃,当NH4SCN完全分解后(NH4SCN
 ),打开K2,继续保持液温105℃,缓缓滴入适量的KOH溶液,发生反应的化学方程式为
),打开K2,继续保持液温105℃,缓缓滴入适量的KOH溶液,发生反应的化学方程式为②装置E中多孔球泡的作用是
(3)制备KSCN晶体:先滤去三颈烧瓶中的固体催化剂,
(4)测定晶体中KSCN的含量:称取
 样品,配成
样品,配成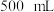 溶液。量取
溶液。量取 溶液于锥形瓶中,加入适量稀硝酸,再加入几滴
溶液于锥形瓶中,加入适量稀硝酸,再加入几滴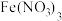 溶液作指示剂,用
溶液作指示剂,用 标准溶液滴定,达到滴定终点时消耗
标准溶液滴定,达到滴定终点时消耗 ,标准溶液
,标准溶液 。
。①滴定时发生的反应:
 (白色)。则判断到达滴定终点的方法是
(白色)。则判断到达滴定终点的方法是②晶体中KSCN的质量分数为
您最近一年使用:0次
8 . 四氯化锡可用作媒染剂。利用如图所示装置可以制备四氯化锡(部分夹持装置已略去);

有关信息如表:
回答下列问题:
(1)甲装置中仪器A的名称为___ 。
(2)用甲装置制氯气,MnO 被还原为Mn2+,该反应的离子方程式为
被还原为Mn2+,该反应的离子方程式为___ 。
(3)将装置如图连接好,__ (填操作),慢慢滴入浓盐酸,待观察到__ (填现象)后,开始加热丁装置,锡熔化后适当增大氯气流量,继续加热丁装置,此时继续加热丁装置的目的是:①促进氯气与锡反应;②___ 。
(4)如果缺少乙装置,可能发生的副反应的化学方程式为__ ;己装置的作用是__ 。
A.除去未反应的氯气,防止污染空气
B.防止空气中CO2气体进入戊装置
C.防止水蒸气进入戊装置的试管中使产物水解
D.防止空气中O2进入戊装置的试管中使产物氧化
(5)某同学认为丁装置中的反应可能产生SnCl2杂质,以下试剂中可用于检测是否产生SnCl2的有__ (填标号)。
A.H2O2溶液 B.FeCl3溶液(滴有KSCN) C.AgNO3溶液 D.溴水
(6)反应中用去锡粒1.19g,反应后在戊装置的试管中收集到2.38gSnCl4,则SnCl4的产率为___ 。(保留3位有效数字)

有关信息如表:
| 化学式 | SnCl2 | SnCl4 |
| 熔点/℃ | 246 | -33 |
| 沸点/℃ | 652 | 144 |
| 其他性质 | 无色晶体,易氧化 | 无色液体,易水解 |
(1)甲装置中仪器A的名称为
(2)用甲装置制氯气,MnO
 被还原为Mn2+,该反应的离子方程式为
被还原为Mn2+,该反应的离子方程式为(3)将装置如图连接好,
(4)如果缺少乙装置,可能发生的副反应的化学方程式为
A.除去未反应的氯气,防止污染空气
B.防止空气中CO2气体进入戊装置
C.防止水蒸气进入戊装置的试管中使产物水解
D.防止空气中O2进入戊装置的试管中使产物氧化
(5)某同学认为丁装置中的反应可能产生SnCl2杂质,以下试剂中可用于检测是否产生SnCl2的有
A.H2O2溶液 B.FeCl3溶液(滴有KSCN) C.AgNO3溶液 D.溴水
(6)反应中用去锡粒1.19g,反应后在戊装置的试管中收集到2.38gSnCl4,则SnCl4的产率为
您最近一年使用:0次
2021-05-28更新
|
276次组卷
|
7卷引用:天津市十二区重点学校2023届高三毕业班下学期第二次联考化学试题
9 . 硫氰化钾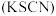 俗称玫瑰红酸钾,是一种用途广泛的化学药品.主要用于合成树脂、杀虫杀菌剂、芥子油、硫脲类和药物等.实验室模拟工业以
俗称玫瑰红酸钾,是一种用途广泛的化学药品.主要用于合成树脂、杀虫杀菌剂、芥子油、硫脲类和药物等.实验室模拟工业以 和
和 为原料制备
为原料制备 的实验装置如图所示:
的实验装置如图所示:
已知:① 不溶于
不溶于 ,
, 密度比水大且难溶于水;
密度比水大且难溶于水;
②三颈烧瓶内盛放 、水和催化剂,发生反应:
、水和催化剂,发生反应: ,该反应比较缓慢,且
,该反应比较缓慢,且 在高于170℃易分解。
在高于170℃易分解。
③ 的溶解度随温度变化较大。
的溶解度随温度变化较大。

(1)A装置中固体混合物是_______ ;仪器a的名称_______
(2)三颈烧瓶内的导气管插入下层  液体中,原因是
液体中,原因是_______ 。
(3)待实验中观察到_______ 现象时,熄灭A处酒精灯,待D中无气泡产生时关闭 .保持三颈烧瓶内液温105℃一段时间,使
.保持三颈烧瓶内液温105℃一段时间,使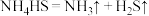 进行完全后,打开
进行完全后,打开 ,继续保持液温105℃,滴入适量的
,继续保持液温105℃,滴入适量的 溶液,写出生成
溶液,写出生成 的化学方程式
的化学方程式_______ 。
(4)装置E的作用为吸收尾气,防止污染环境,写出吸收 的离子方程式
的离子方程式_______ 。
(5)反应结束后将三颈烧瓶中的固体催化剂滤去,再_______ .(填操作),得到硫氰化钾晶体。
(6)晶体中 含量的测定:称取
含量的测定:称取 样品,配成
样品,配成 溶液.量取
溶液.量取 溶液于锥形瓶中,加入适量稀硝酸,再加入几滴a作指示剂,用
溶液于锥形瓶中,加入适量稀硝酸,再加入几滴a作指示剂,用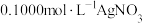 标准溶液滴定,达到滴定终点时消耗
标准溶液滴定,达到滴定终点时消耗 标准溶液
标准溶液 .(已知:滴定时发生的反应为
.(已知:滴定时发生的反应为 (白色))
(白色))
①指示剂a为_______ 。
②晶体中 的质量分数为
的质量分数为_______ %。
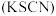 俗称玫瑰红酸钾,是一种用途广泛的化学药品.主要用于合成树脂、杀虫杀菌剂、芥子油、硫脲类和药物等.实验室模拟工业以
俗称玫瑰红酸钾,是一种用途广泛的化学药品.主要用于合成树脂、杀虫杀菌剂、芥子油、硫脲类和药物等.实验室模拟工业以 和
和 为原料制备
为原料制备 的实验装置如图所示:
的实验装置如图所示:已知:①
 不溶于
不溶于 ,
, 密度比水大且难溶于水;
密度比水大且难溶于水;②三颈烧瓶内盛放
 、水和催化剂,发生反应:
、水和催化剂,发生反应: ,该反应比较缓慢,且
,该反应比较缓慢,且 在高于170℃易分解。
在高于170℃易分解。③
 的溶解度随温度变化较大。
的溶解度随温度变化较大。
(1)A装置中固体混合物是
(2)三颈烧瓶内的导气管插入
 液体中,原因是
液体中,原因是(3)待实验中观察到
 .保持三颈烧瓶内液温105℃一段时间,使
.保持三颈烧瓶内液温105℃一段时间,使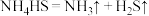 进行完全后,打开
进行完全后,打开 ,继续保持液温105℃,滴入适量的
,继续保持液温105℃,滴入适量的 溶液,写出生成
溶液,写出生成 的化学方程式
的化学方程式(4)装置E的作用为吸收尾气,防止污染环境,写出吸收
 的离子方程式
的离子方程式(5)反应结束后将三颈烧瓶中的固体催化剂滤去,再
(6)晶体中
 含量的测定:称取
含量的测定:称取 样品,配成
样品,配成 溶液.量取
溶液.量取 溶液于锥形瓶中,加入适量稀硝酸,再加入几滴a作指示剂,用
溶液于锥形瓶中,加入适量稀硝酸,再加入几滴a作指示剂,用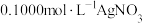 标准溶液滴定,达到滴定终点时消耗
标准溶液滴定,达到滴定终点时消耗 标准溶液
标准溶液 .(已知:滴定时发生的反应为
.(已知:滴定时发生的反应为 (白色))
(白色))①指示剂a为
②晶体中
 的质量分数为
的质量分数为
您最近一年使用:0次
2021-04-13更新
|
559次组卷
|
3卷引用:天津市第一中学2020-2021学年高三下学期第四次月考化学试题
解题方法
10 . 有效的进行科学实验是学习化学的重要方法之一。
I.
(1)下列实验事实不能 作为所得结论合理证据的是_______ 。
II.选择性催化还原是在有催化剂的条件下将NOx转变为N2和H2O,这是目前硝酸厂进行尾气治理普遍采用的一种方法,某小组同学拟验证NO能被氨气还原并测算其转化率。
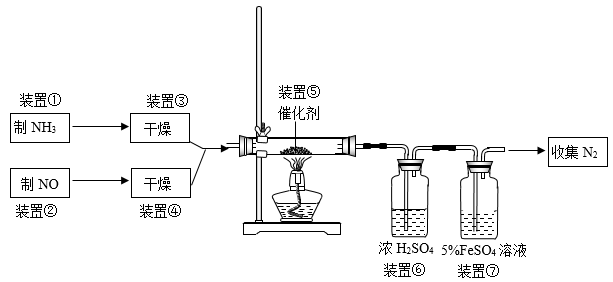
请回答下列问题:
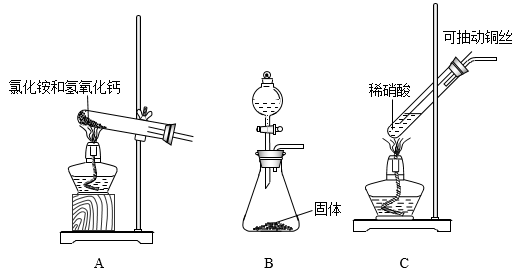
(2)若制取氨气用A装置,则发生反应的化学方程式为_______ ,若用B装置制取氨气,则分液漏斗和锥形瓶中盛放的药品分别是_______ 、_______ ;
(3)用C装置制取NO时,用可抽动的铜丝,其优点是_______ ,其反应的离子方程式为_______ ;
(4)装置⑦的作用可能是_______ ;
(5)若进入装置⑤的NO共4.48L(标准状况下),氨气过量,最后收集到标况下2.24 LN2,则NO的转化率为_______ 。
III.常温常压下,一氧化二氯(Cl2O)为棕黄色气体,沸点为 3.8 ℃,42 ℃以上会分解生成 Cl2和 O2,Cl2O 易溶于水并与水反应生成 HClO。
【制备产品】将氯气和空气(不参与反应)按体积比 1:3 混合通入含水 8%的碳酸钠溶液中制备 Cl2O,并用水吸收 Cl2O(不含 Cl2)制备次氯酸溶液。
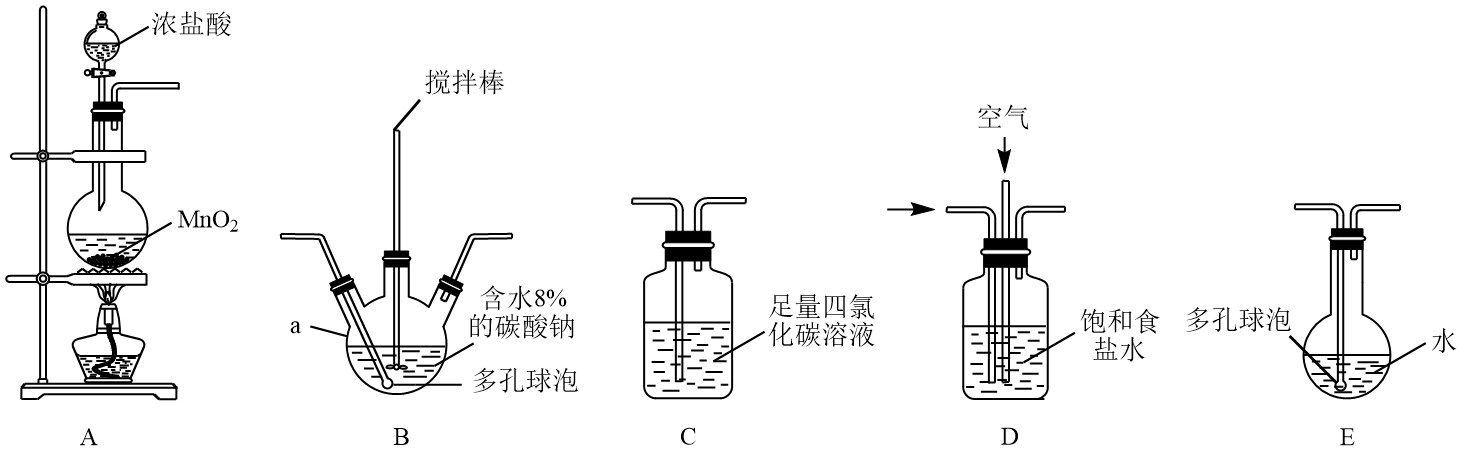
(6)各装置的连接顺序为_______ →_______ →_______ →C→_______ 。
(7)写出A中反应的离子方程式_______ 。
(8)制备Cl2O的化学方程式为_______ 。
(9)反应过程中,装置 B 需放在冷水中,其目的是_______ 。
(10)此方法相对于用氯气直接溶于水制备次氯酸溶液有两个主要优点,分别是_______ 、_______ 。
【测定浓度】
(11)用下列实验方案测定装置 E 所得溶液中次氯酸的物质的量浓度:量取10.00 mL上述次氯酸溶液,并稀释至100.00 mL,再从其中取出10.00 mL于锥形瓶中,并加入10.00 mL 0.8000 mol·L-1的FeSO4溶液(过量),充分反应后用0.05000 mol·L-1的酸性KMnO4溶液滴定剩余的 Fe2+,消耗 KMnO4溶液20.00 mL,则原次氯酸溶液的浓度为_______ 。判断下列情况对HClO含量测定结果的影响(填“偏高”、“偏低”或“无影响”)。若 FeSO4标准溶液部分变质,会使测定结果_______ ;若配制酸性KMnO4溶液时,定容时仰视视刻度线,会使测定结果_______ 。
I.
(1)下列实验事实
| 选项 | A | B | C | D |
| 实验 | 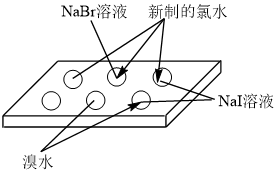 | 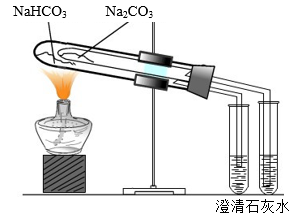 | 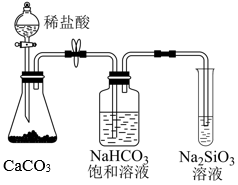 |  钾与水反应 钠与水反应 |
| 现象 | NaBr溶液变为橙色,NaI溶液变为棕黄色 | 左边盛澄清石灰水的试管变浑浊,而右边的不变浑浊 | Na2SiO3溶液中出现白色沉淀 | 钾与水反应比钠与水反应更剧烈 |
| 结论 | 氧化性:Cl2>Br2>I2 | 热稳定性:Na2CO3>NaHCO3 | 非金属性:C>Si | 金属性:K>Na |
II.选择性催化还原是在有催化剂的条件下将NOx转变为N2和H2O,这是目前硝酸厂进行尾气治理普遍采用的一种方法,某小组同学拟验证NO能被氨气还原并测算其转化率。


请回答下列问题:
(2)若制取氨气用A装置,则发生反应的化学方程式为
(3)用C装置制取NO时,用可抽动的铜丝,其优点是
(4)装置⑦的作用可能是
(5)若进入装置⑤的NO共4.48L(标准状况下),氨气过量,最后收集到标况下2.24 LN2,则NO的转化率为
III.常温常压下,一氧化二氯(Cl2O)为棕黄色气体,沸点为 3.8 ℃,42 ℃以上会分解生成 Cl2和 O2,Cl2O 易溶于水并与水反应生成 HClO。
【制备产品】将氯气和空气(不参与反应)按体积比 1:3 混合通入含水 8%的碳酸钠溶液中制备 Cl2O,并用水吸收 Cl2O(不含 Cl2)制备次氯酸溶液。

(6)各装置的连接顺序为
(7)写出A中反应的离子方程式
(8)制备Cl2O的化学方程式为
(9)反应过程中,装置 B 需放在冷水中,其目的是
(10)此方法相对于用氯气直接溶于水制备次氯酸溶液有两个主要优点,分别是
【测定浓度】
(11)用下列实验方案测定装置 E 所得溶液中次氯酸的物质的量浓度:量取10.00 mL上述次氯酸溶液,并稀释至100.00 mL,再从其中取出10.00 mL于锥形瓶中,并加入10.00 mL 0.8000 mol·L-1的FeSO4溶液(过量),充分反应后用0.05000 mol·L-1的酸性KMnO4溶液滴定剩余的 Fe2+,消耗 KMnO4溶液20.00 mL,则原次氯酸溶液的浓度为
您最近一年使用:0次



