名校
解题方法
1 . 某化学兴趣小组在研究“铁及其化合物性质”时,发现向 溶液中滴加2滴
溶液中滴加2滴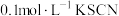 溶液;无明显现象,再滴加
溶液;无明显现象,再滴加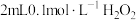 溶液溶液(
溶液溶液( 约为5),溶液先变红,后褪色,并有气泡产生。为了弄清楚产生这种异常现象的原因,他们进行了如下探究:
约为5),溶液先变红,后褪色,并有气泡产生。为了弄清楚产生这种异常现象的原因,他们进行了如下探究:
(1)溶液先变红的原因是____________ 、____________ (用两个离子方程式表示)。
(2)同学们对溶液褪色的原因提出了不同的看法并进行实验:
I.甲同学认为是 被
被 还原。取褪色后溶液,滴加
还原。取褪色后溶液,滴加 溶液,无明显现象,证明甲同学观点不正确。
溶液,无明显现象,证明甲同学观点不正确。
Ⅱ.乙同学认为是 被氧化。取褪色后溶液,滴加
被氧化。取褪色后溶液,滴加 溶液,出现红色。
溶液,出现红色。
根据上述实验现象,同学们认为溶液褪色的原因可能有两种:
乙同学认为 被
被 氧化。
氧化。
丙同学认为____________ 。
为了探究溶液褪色的原因究竟是上述的哪一种,该兴趣小组进行了如下实验。向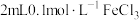 溶液中滴加2滴
溶液中滴加2滴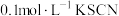 溶液,后通入
溶液,后通入 ,发现溶液
,发现溶液___________ ,证明溶液褪色的原因不是乙同学认为的原因,而是丙同学认为的原因。
(3)该兴趣小组通过查阅资料,发现 可以被氧化成
可以被氧化成 和两种可直接排放到空气中的气体,写出上述实验中
和两种可直接排放到空气中的气体,写出上述实验中 被氧化的离子方程式:
被氧化的离子方程式:_________ 。
(4)根据题目所给信息及实验现象推断物质还原性强弱:
____________  (填“>”或“<”)
(填“>”或“<”)
 溶液中滴加2滴
溶液中滴加2滴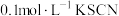 溶液;无明显现象,再滴加
溶液;无明显现象,再滴加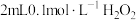 溶液溶液(
溶液溶液( 约为5),溶液先变红,后褪色,并有气泡产生。为了弄清楚产生这种异常现象的原因,他们进行了如下探究:
约为5),溶液先变红,后褪色,并有气泡产生。为了弄清楚产生这种异常现象的原因,他们进行了如下探究:(1)溶液先变红的原因是
(2)同学们对溶液褪色的原因提出了不同的看法并进行实验:
I.甲同学认为是
 被
被 还原。取褪色后溶液,滴加
还原。取褪色后溶液,滴加 溶液,无明显现象,证明甲同学观点不正确。
溶液,无明显现象,证明甲同学观点不正确。Ⅱ.乙同学认为是
 被氧化。取褪色后溶液,滴加
被氧化。取褪色后溶液,滴加 溶液,出现红色。
溶液,出现红色。根据上述实验现象,同学们认为溶液褪色的原因可能有两种:
乙同学认为
 被
被 氧化。
氧化。丙同学认为
为了探究溶液褪色的原因究竟是上述的哪一种,该兴趣小组进行了如下实验。向
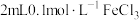 溶液中滴加2滴
溶液中滴加2滴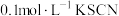 溶液,后通入
溶液,后通入 ,发现溶液
,发现溶液(3)该兴趣小组通过查阅资料,发现
 可以被氧化成
可以被氧化成 和两种可直接排放到空气中的气体,写出上述实验中
和两种可直接排放到空气中的气体,写出上述实验中 被氧化的离子方程式:
被氧化的离子方程式:(4)根据题目所给信息及实验现象推断物质还原性强弱:

 (填“>”或“<”)
(填“>”或“<”)
您最近一年使用:0次
2 . 某化学兴趣小组利用如图所示装置进行SO2的制备与性质探究的一体化实验,下列说法正确的是
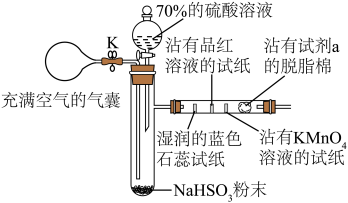
| A.分液漏斗中的硫酸溶液可用98%的浓硫酸代替以加快反应速率 |
| B.打开分液漏斗活塞一段时间后,会观察到湿润的蓝色石蕊试纸先变红后褪色 |
| C.试剂a可选择澄清石灰水以吸收多余的SO2,防止污染环境 |
| D.反应结束后,打开止水夹K并挤压气囊使装置内残留的SO2被充分吸收 |
您最近一年使用:0次
名校
解题方法
3 . 某校研究性学习小组设计实验,验证草酸受热分解的产物。已知:①草酸是一种弱酸,草酸晶体(H2C2O4·2H2O)易溶于水,受热易熔化、气化和分解。②草酸分解产生 和
和 。③草酸钙
。③草酸钙 是白色固体,难溶于水。
是白色固体,难溶于水。
(1)草酸中含有的化学键类型是____________ ,草酸晶体分解的化学方程式是____________ 。
(2)验证草酸分解的产物用到下列仪器,仪器的连接顺序是____________ (仪器可重复使用);A装置的作用是____________ ,该套装置___________ (填“是”或“否”)完善,说明理由____________ 。 的仪器名称是
的仪器名称是___________ 。
(4)证明有 生成的现象是
生成的现象是___________ 。
 和
和 。③草酸钙
。③草酸钙 是白色固体,难溶于水。
是白色固体,难溶于水。(1)草酸中含有的化学键类型是
(2)验证草酸分解的产物用到下列仪器,仪器的连接顺序是
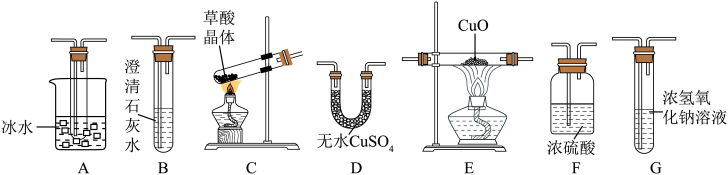
 的仪器名称是
的仪器名称是(4)证明有
 生成的现象是
生成的现象是
您最近一年使用:0次
2024-04-23更新
|
63次组卷
|
2卷引用:河北省张家口市尚义县第一中学等校2023-2024学年高一下学期3月阶段测试化学试题
4 . 某化学兴趣小组用下图装置(部分夹持装置已略去)制取氨气并探究其性质。__________ (填名称)。
(2)气体通过C、D装置时,试纸颜色会发生变化的是__________ (填字母),原因是_______________ 。
(3)当E装置中集满 时,挤压胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是
时,挤压胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是_________________ 。
(4)用下图装置探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物。__________________ ,证明氨气具有__________ (填“氧化性”或“还原性”)。
②若向a中通入标准状况下3.36L的氨气,理论上会得到铜的质量为__________ g。
(5)已知加热条件下,氨气可以与铝发生置换反应生成AlN;AlN加热时可溶于浓碱溶液并产生氨气,发生反应: 。称取AlN样品23.2g(假设杂质只含Al),将其放入足量浓碱溶液中加热,若所产生的气体全部逸出并收集,测得其体积为14.56L(标准状况),则样品中AlN的质量分数为
。称取AlN样品23.2g(假设杂质只含Al),将其放入足量浓碱溶液中加热,若所产生的气体全部逸出并收集,测得其体积为14.56L(标准状况),则样品中AlN的质量分数为__________ %(精确到0.1%)。
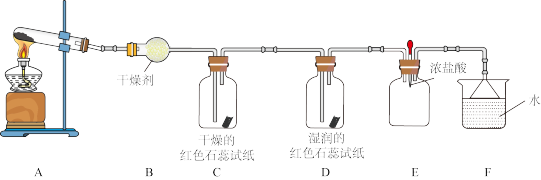
(2)气体通过C、D装置时,试纸颜色会发生变化的是
(3)当E装置中集满
 时,挤压胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是
时,挤压胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是(4)用下图装置探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物。

②若向a中通入标准状况下3.36L的氨气,理论上会得到铜的质量为
(5)已知加热条件下,氨气可以与铝发生置换反应生成AlN;AlN加热时可溶于浓碱溶液并产生氨气,发生反应:
 。称取AlN样品23.2g(假设杂质只含Al),将其放入足量浓碱溶液中加热,若所产生的气体全部逸出并收集,测得其体积为14.56L(标准状况),则样品中AlN的质量分数为
。称取AlN样品23.2g(假设杂质只含Al),将其放入足量浓碱溶液中加热,若所产生的气体全部逸出并收集,测得其体积为14.56L(标准状况),则样品中AlN的质量分数为
您最近一年使用:0次
5 . 某化学兴趣小组同学利用如图所示装置(夹持与加热装置已略去)来进行乙醇的脱水反应实验,下列说法错误的是

A. 在该反应中起催化剂作用 在该反应中起催化剂作用 |
| B.若将盛装水的试剂瓶撤去后进行实验,实验过程中观察到试管中的酸性高锰酸钾溶液褪色,一定是生成的乙烯使其褪色 |
C.实验过程中,可能发生的反应有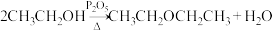 |
| D.该实验过程中所生成的乙烯,其所有原子一定位于同一平面上 |
您最近一年使用:0次
6 . NH3一种重要的化工原料,可用于制氮肥、HNO3、铵盐、纯碱等。某实验小组在实验空中对NH3的性质进行了探究,设计了如下实验装置,回答下列问题:
(1)NH3的制备

①装置 C的仪器名称为_______ 。
②实验室用装置D作为制取氨气的发生装置,该反应的化学方程式为_______ ;若用装置B作为制取氨气的发生装置,分液漏斗中盛装的试剂名称为_______ 。
③欲收集一瓶干燥的气,选择上图中的装置。 其连接顺序为:发生装置
_______ (按气流方向,用小写字母表示)。
(2)NH3性质探究
利用制取的干燥NH3,该实验小组进行如下实验,并填写实验报告,

①完成填空i_______ ,ii_______ 。
②装置 C的作用为_______ 。
③装置A中发生反应的化学方程式为_______ ,体现了NH3的_______ (填“氧化”或“还原”)性。
(1)NH3的制备

①装置 C的仪器名称为
②实验室用装置D作为制取氨气的发生装置,该反应的化学方程式为
③欲收集一瓶干燥的气,选择上图中的装置。 其连接顺序为:发生装置

(2)NH3性质探究
利用制取的干燥NH3,该实验小组进行如下实验,并填写实验报告,

序号 | 实验现象 | 实验结论 |
Ⅰ | _______i_______ | 反应生成了Cu |
Ⅱ | 装置B中无水CuSO4变蓝 | 反应生成了_______ii_______ |
Ⅲ | 装置D中搜集到无色无味气体 | 反应生成了N2 |
②装置 C的作用为
③装置A中发生反应的化学方程式为
您最近一年使用:0次
7 . 某实验小组在验证某些离子的性质时,做了如下实验,并对实验现象进行了相关探究。
实验 | 试剂 | 编号及现象 | |
试管 | 滴管 | ||
| 1.0 | 1.0 | Ⅰ.产生黄色沉淀,溶液无色 |
1.0 | Ⅱ.产生白色沉淀,溶液变黄 | ||
(1)通过所学知识分析,实验Ⅰ中的黄色沉淀可能是
 或
或(2)设计实验检验黄色沉淀是否含
 :取适量的黄色沉淀,
:取适量的黄色沉淀, 。故实验Ⅰ中发生反应的离子方程式为
。故实验Ⅰ中发生反应的离子方程式为(3)将适量实验Ⅱ中得到的黄色溶液加入淀粉溶液中,溶液变蓝,由此推断实验Ⅱ中产生白色沉淀的离子方程式为
(4)某同学分析实验Ⅰ、Ⅱ的现象得出结论:
 氧化性比
氧化性比 强。你认为该结论
强。你认为该结论(5)为检验
 能否氧化
能否氧化 ,设计实验Ⅲ,装置如图所示:
,设计实验Ⅲ,装置如图所示: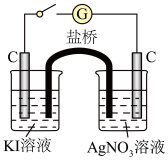
闭合开关,KI溶液变为棕黄色, 溶液中C电极上有银析出,电流计指针偏转。
溶液中C电极上有银析出,电流计指针偏转。
查阅资料:
①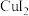 微溶于水,不稳定,在溶液中易发生氧化还原反应生成CuI、
微溶于水,不稳定,在溶液中易发生氧化还原反应生成CuI、 。
。
②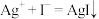
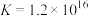 。
。
① 溶液中C电极作
溶液中C电极作
②实验Ⅲ中有Ag单质生成,而实验Ⅰ中没有,其原因可能是
您最近一年使用:0次
8 . 根据实验操作和现象,下列结论中正确的是
选项 | 实验操作和现象 | 结论 |
A | 常温下将铝片分别插入稀硝酸和浓硝酸中,前者产生无色气体,后者无明显现象 | 稀硝酸的氧化性比浓硝酸强 |
B | 向 溶液中通入 溶液中通入 ,无明显现象;再通入X气体,出现沉淀 ,无明显现象;再通入X气体,出现沉淀 | 气体X一定具有强氧化性或溶于水显碱性 |
C | 向两支分别盛有少量等物质的量的白色 固体和黑色 固体和黑色 固体的试管中,同时加入等体积、等浓度的氨水,振荡,白色固体溶解,黑色固体不溶解 固体的试管中,同时加入等体积、等浓度的氨水,振荡,白色固体溶解,黑色固体不溶解 | 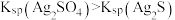 |
D | 向盛有 甲苯的试管中加入几滴酸性高锰酸钾溶液,振荡后溶液褪色 甲苯的试管中加入几滴酸性高锰酸钾溶液,振荡后溶液褪色 | 苯环受甲基影响,可被酸性高锰酸钾溶液氧化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 . 某小组设计了如下图所示的实验装置来探究过氧化钠的强氧化性。
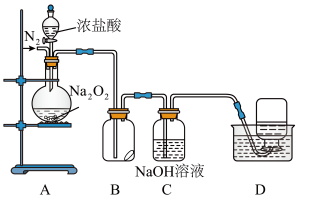
实验步骤及现象如下:
①检查装置气密性后,装入药品并连接装置A、B、C。
②缓慢通入一定量的N2后,将装置D连接好(导管末端未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,A中剧烈反应,有黄绿色气体产生。
③待装置D中导管口产生连续气泡后,将导管末端伸入集气瓶中,收集到无色气体。
④反应一段时间后,停止滴加浓盐酸,再通一段时间N2,直至装置中气体变为无色。
(1)装置D中收集的无色气体X能使带火星的木条复燃,据此推断该气体X为___________ (填化学式)。
(2)装置B中湿润的淀粉碘化钾试纸变蓝。
甲同学根据A中气体的颜色推测试纸变蓝时发生反应的离子方程式为___________ 。乙同学认为使试纸变蓝的原因也可能是___________ (填序号)。
a.挥发的HCl气体使试纸变蓝
b.在此实验过程中生成的X气体也能将I-氧化为I2
c.通入的N2使试纸变蓝
(3)Na2O2与干燥的HCl能发生化学反应生成Cl2、NaCl和H2O,该反应的化学方程式为___________ ,当反应生成标准状况下2.24L Cl2时,转移的电子数___________ mol。

实验步骤及现象如下:
①检查装置气密性后,装入药品并连接装置A、B、C。
②缓慢通入一定量的N2后,将装置D连接好(导管末端未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,A中剧烈反应,有黄绿色气体产生。
③待装置D中导管口产生连续气泡后,将导管末端伸入集气瓶中,收集到无色气体。
④反应一段时间后,停止滴加浓盐酸,再通一段时间N2,直至装置中气体变为无色。
(1)装置D中收集的无色气体X能使带火星的木条复燃,据此推断该气体X为
(2)装置B中湿润的淀粉碘化钾试纸变蓝。
甲同学根据A中气体的颜色推测试纸变蓝时发生反应的离子方程式为
a.挥发的HCl气体使试纸变蓝
b.在此实验过程中生成的X气体也能将I-氧化为I2
c.通入的N2使试纸变蓝
(3)Na2O2与干燥的HCl能发生化学反应生成Cl2、NaCl和H2O,该反应的化学方程式为
您最近一年使用:0次
名校
解题方法
10 . 为探究 的性质,设计了如下实验。
的性质,设计了如下实验。
下列说法错误的是
 的性质,设计了如下实验。
的性质,设计了如下实验。| 实验装置 |
|
| 实验操作及现象 | ①抽去毛玻璃片后,反应瓶内壁有白色固体物质生成,红棕色气体逐渐变浅,直至无色。 ②取白色固体物质溶于水,依次加入稀盐酸、  溶液,溶液中出现白色沉淀。 溶液,溶液中出现白色沉淀。 |
A.白色固体主要成分为 |
B.物质氧化性:浓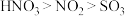 |
C.由实验可知,能用湿润的淀粉 试纸鉴别 试纸鉴别 与 与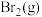 |
D.实验后的剩余气体可用酸性 溶液处理,防止污染空气 溶液处理,防止污染空气 |
您最近一年使用:0次
2024-03-09更新
|
699次组卷
|
5卷引用:河北省廊坊市2023-2024学年高一下学期3月月考化学试题
河北省廊坊市2023-2024学年高一下学期3月月考化学试题江西省赣州市2024届高三下学期3月摸底考试化学试题江西省赣州市2024届高三下学期年3月摸底考试化学试题云南省云南师范大学实验中学2023-2024学年高一下学期三月月考化学试题(已下线)通关练02 重要无机化合物的性质及应用-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)


 KI溶液
KI溶液 溶液
溶液


