解题方法
1 . 某化学小组探究硫酸铁铵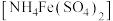 与
与 、
、 的反应。
的反应。
已知: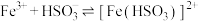 (棕红)
(棕红)
(1)①实验Ⅰ中产生红褐色沉淀与气泡的离子方程式为___________ 。
②由实验Ⅰ可得出与 结合的能力:
结合的能力:
___________  (填“>”、“<”、“=”)。
(填“>”、“<”、“=”)。
(2)资料显示, 可以氧化
可以氧化 。针对实验Ⅱ中的现象,小组同学又设计并实施了如下实验。
。针对实验Ⅱ中的现象,小组同学又设计并实施了如下实验。
①实验Ⅲ中 与
与 反应生成
反应生成 的离子方程式为
的离子方程式为___________ 。
②结合化学反应原理解释实验Ⅱ、Ⅳ中现象存在差异的可能原因___________ 。
(3)针对实验Ⅲ、Ⅳ的现象差异,小组同学提出猜想:pH影响了 的氧化性或
的氧化性或 的还原性,并实施实验。
的还原性,并实施实验。
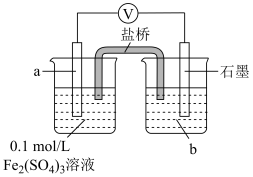
①a、b分别是___________ 。
②结合电极反应解释步骤3中电压表示数减小的原因___________ 。
③补充实验Ⅵ:向实验Ⅱ得到的棕红色液体中加入3滴10%稀硫酸,棕红色迅速变黄,检测到 。结合化学用语解释实验Ⅵ中氧化还原反应明显加快的可能原因
。结合化学用语解释实验Ⅵ中氧化还原反应明显加快的可能原因___________ 。
(4)综合以上实验,盐溶液间反应的多样性与___________ 有关。
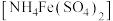 与
与 、
、 的反应。
的反应。| 实验 | 操作 | 现象 |
| Ⅰ | 向2mL 溶液(pH=2.03)中逐滴加入 溶液(pH=2.03)中逐滴加入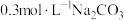 溶液 溶液 | 迅速产生大量红褐色沉淀和大量气泡;继续滴加,当气泡量明显减少时,试管口的湿润红色石蕊试纸开始逐渐变蓝 |
| Ⅱ | 向2mL 溶液(pH=2.03)中逐滴加入 溶液(pH=2.03)中逐滴加入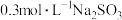 溶液 溶液 | 溶液立即变棕红(无丁达尔现象),继续滴加 溶液至过量,溶液依然为棕红色,放置两天无明显变化 溶液至过量,溶液依然为棕红色,放置两天无明显变化 |
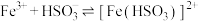 (棕红)
(棕红)(1)①实验Ⅰ中产生红褐色沉淀与气泡的离子方程式为
②由实验Ⅰ可得出与
 结合的能力:
结合的能力:
 (填“>”、“<”、“=”)。
(填“>”、“<”、“=”)。(2)资料显示,
 可以氧化
可以氧化 。针对实验Ⅱ中的现象,小组同学又设计并实施了如下实验。
。针对实验Ⅱ中的现象,小组同学又设计并实施了如下实验。| 实验 | 操作 | 现象 |
| Ⅲ | 向2mL 溶液(pH=1.78)中加入0.5mL 溶液(pH=1.78)中加入0.5mL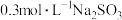 溶液 溶液 | 溶液立即变棕红色,约2小时后,棕红色变为黄色,检测到 |
| Ⅳ | 向2mL 溶液(pH=2.03)中加入0.5mL 溶液(pH=2.03)中加入0.5mL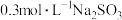 溶液 溶液 | 溶液立即变棕红色,约5小时后,棕红色变为黄色,检测到 |
 与
与 反应生成
反应生成 的离子方程式为
的离子方程式为②结合化学反应原理解释实验Ⅱ、Ⅳ中现象存在差异的可能原因
(3)针对实验Ⅲ、Ⅳ的现象差异,小组同学提出猜想:pH影响了
 的氧化性或
的氧化性或 的还原性,并实施实验。
的还原性,并实施实验。| 实验 | 实验装置 | 实验步骤及现象 |
| Ⅴ |
| 1.按如图搭好装置,接通电路,电压表读数为0.6V; 2.向a电极附近滴加3滴10%稀硫酸,电压表读数不变; 3.向石墨电极附近滴加3滴10%稀硫酸,电压表读数变为0.5V。 |
②结合电极反应解释步骤3中电压表示数减小的原因
③补充实验Ⅵ:向实验Ⅱ得到的棕红色液体中加入3滴10%稀硫酸,棕红色迅速变黄,检测到
 。结合化学用语解释实验Ⅵ中氧化还原反应明显加快的可能原因
。结合化学用语解释实验Ⅵ中氧化还原反应明显加快的可能原因(4)综合以上实验,盐溶液间反应的多样性与
您最近一年使用:0次
2 . 某小组为探究 与
与 之间的反应,进行了如下实验。
之间的反应,进行了如下实验。
已知: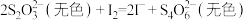 ;
; 为白色沉淀,可吸附
为白色沉淀,可吸附 ;
;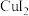 在溶液中不存在;
在溶液中不存在;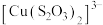 呈无色,
呈无色,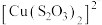 呈黄色。
呈黄色。
下列结论或推断不合理 的是
 与
与 之间的反应,进行了如下实验。
之间的反应,进行了如下实验。实验 |
|
|
现象 | ①产生土黄色沉淀,溶液为棕黄色 ②变为白色悬浊液,最后得到无色澄清溶液 | ①产生土黄色沉淀,溶液为蓝绿色 ②开始变为浅蓝色悬浊液,逐渐变为黄绿色悬浊液,然后变为黄色溶液,最后得到无色溶液 |
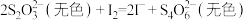 ;
; 为白色沉淀,可吸附
为白色沉淀,可吸附 ;
;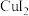 在溶液中不存在;
在溶液中不存在;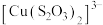 呈无色,
呈无色,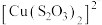 呈黄色。
呈黄色。下列结论或推断
A. 与 与 能发生反应: 能发生反应: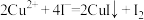 |
B. 与 与 反应的速率快于 反应的速率快于 与 与 反应的速率 反应的速率 |
C.黄绿色悬浊液变为黄色溶液时,有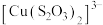 、 、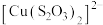 生成 生成 |
D.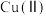 与 与 生成配合物反应的限度小于二者发生氧化还原反应的限度 生成配合物反应的限度小于二者发生氧化还原反应的限度 |
您最近一年使用:0次
3 . 在探究铜与硝酸反应时,发现在室温下,溶液A与铜片立即产生气泡,而相同条件下,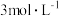 稀硝酸(溶液B)遇铜片短时间内无明显变化,一段时间后才产生气泡。针对这一现象,同学们展开了一系列研究。
稀硝酸(溶液B)遇铜片短时间内无明显变化,一段时间后才产生气泡。针对这一现象,同学们展开了一系列研究。 与浓
与浓 反应的化学方程式为
反应的化学方程式为___________ 。
(2)己知 与浓
与浓 反应后溶液呈绿色的原因是溶液中溶解了生成的气体所致,用化学方程式表示加水稀释过程中溶液变为蓝色的原因
反应后溶液呈绿色的原因是溶液中溶解了生成的气体所致,用化学方程式表示加水稀释过程中溶液变为蓝色的原因___________ 。
(3)查阅资料:
①二氧化氮溶于水的过程产生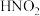 。
。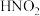 中氮元素的化合价为
中氮元素的化合价为___________ 。
②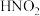 (亚硝酸):无色,易溶于水:不稳定:弱酸,可由亚硝酸盐与强酸反应制得。
(亚硝酸):无色,易溶于水:不稳定:弱酸,可由亚硝酸盐与强酸反应制得。
(4)分析溶液A与铜片立即产生气泡,而相同条件下,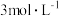 稀硝酸(溶液B)遇铜片短时间内无明显变化的原因,提出假设:
稀硝酸(溶液B)遇铜片短时间内无明显变化的原因,提出假设: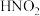 对该反应有催化作用。通过进一步实验确认了这种假设,其实验操作和现象是:向放有铜片的B溶液中
对该反应有催化作用。通过进一步实验确认了这种假设,其实验操作和现象是:向放有铜片的B溶液中___________ 。
(5)催化剂能够加快化学反应速率的原因是:改变反应历程,先参加反应,后又生成,所以反应前后催化剂的量和性质不发生改变。由此同学们推测 与稀硝酸反应中
与稀硝酸反应中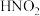 起催化作用的过程如下:
起催化作用的过程如下:
i.___________ (用离子方程式表示)
ii.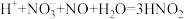
(6)同学们进一步查阅文献资料显示,工业生产硝酸时,会生成亚硝酸等物质。亚硝酸能分解为 (易分解为
(易分解为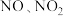 )等物质。要充分考虑到这些变化而采取必要的措施,可提高硝酸的产率,该措施是
)等物质。要充分考虑到这些变化而采取必要的措施,可提高硝酸的产率,该措施是___________ 。
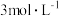 稀硝酸(溶液B)遇铜片短时间内无明显变化,一段时间后才产生气泡。针对这一现象,同学们展开了一系列研究。
稀硝酸(溶液B)遇铜片短时间内无明显变化,一段时间后才产生气泡。针对这一现象,同学们展开了一系列研究。
 与浓
与浓 反应的化学方程式为
反应的化学方程式为(2)己知
 与浓
与浓 反应后溶液呈绿色的原因是溶液中溶解了生成的气体所致,用化学方程式表示加水稀释过程中溶液变为蓝色的原因
反应后溶液呈绿色的原因是溶液中溶解了生成的气体所致,用化学方程式表示加水稀释过程中溶液变为蓝色的原因(3)查阅资料:
①二氧化氮溶于水的过程产生
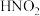 。
。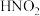 中氮元素的化合价为
中氮元素的化合价为②
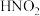 (亚硝酸):无色,易溶于水:不稳定:弱酸,可由亚硝酸盐与强酸反应制得。
(亚硝酸):无色,易溶于水:不稳定:弱酸,可由亚硝酸盐与强酸反应制得。(4)分析溶液A与铜片立即产生气泡,而相同条件下,
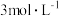 稀硝酸(溶液B)遇铜片短时间内无明显变化的原因,提出假设:
稀硝酸(溶液B)遇铜片短时间内无明显变化的原因,提出假设: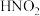 对该反应有催化作用。通过进一步实验确认了这种假设,其实验操作和现象是:向放有铜片的B溶液中
对该反应有催化作用。通过进一步实验确认了这种假设,其实验操作和现象是:向放有铜片的B溶液中(5)催化剂能够加快化学反应速率的原因是:改变反应历程,先参加反应,后又生成,所以反应前后催化剂的量和性质不发生改变。由此同学们推测
 与稀硝酸反应中
与稀硝酸反应中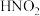 起催化作用的过程如下:
起催化作用的过程如下:i.
ii.
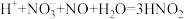
(6)同学们进一步查阅文献资料显示,工业生产硝酸时,会生成亚硝酸等物质。亚硝酸能分解为
 (易分解为
(易分解为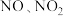 )等物质。要充分考虑到这些变化而采取必要的措施,可提高硝酸的产率,该措施是
)等物质。要充分考虑到这些变化而采取必要的措施,可提高硝酸的产率,该措施是
您最近一年使用:0次
名校
解题方法
4 . 某小组同学探究三种价态(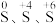 )疏元素间的相互转化。可以选用的试剂有:①
)疏元素间的相互转化。可以选用的试剂有:① 水溶液、②浓硫酸、③稀硫酸、④
水溶液、②浓硫酸、③稀硫酸、④ 溶液、⑤
溶液、⑤ 溶液、⑥氯水(浅黄绿色)、⑦铜片、⑧稀盐酸、⑨
溶液、⑥氯水(浅黄绿色)、⑦铜片、⑧稀盐酸、⑨ 溶液。
溶液。
(1)补全实验表格i ___________ ,ii ___________ ,iii ___________ 。
(2)实验5的化学方程式为___________ 。
(3)为了进一步验证实验1中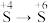 的转化,甲同学设计实验a:向反应后的溶液中先加过量稀盐酸,再加足量
的转化,甲同学设计实验a:向反应后的溶液中先加过量稀盐酸,再加足量 溶液,观察现象。
溶液,观察现象。
①实验a的目的是通过检验___________ ,证明转化得以实现。
②加稀盐酸的作用是___________ 。
乙同学认为还需要补充实验b:取等量的 溶液,向其中先加过量稀盐酸,再加足量
溶液,向其中先加过量稀盐酸,再加足量 溶液,观察现象。
溶液,观察现象。
③补充实验b的原因是___________ 。
④综合实验a和b,实验1中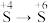 转化得以实现的证据是
转化得以实现的证据是___________ 。
(4)丙同学分析实验3和实验4现象不同的原因,在实验4中又添加了一种试剂___________ (填试剂编号),出现浑浊。发生反应的离子方程式是___________ 。
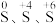 )疏元素间的相互转化。可以选用的试剂有:①
)疏元素间的相互转化。可以选用的试剂有:① 水溶液、②浓硫酸、③稀硫酸、④
水溶液、②浓硫酸、③稀硫酸、④ 溶液、⑤
溶液、⑤ 溶液、⑥氯水(浅黄绿色)、⑦铜片、⑧稀盐酸、⑨
溶液、⑥氯水(浅黄绿色)、⑦铜片、⑧稀盐酸、⑨ 溶液。
溶液。| 实验序号 | 预期的价态转化 | 选择的试剂 (填入试剂编号) | 实验现象 |
| 1 | 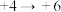 | ④⑥ | |
| 2 | i___________ | ii___________ | |
| 3 |  | ①⑤ | 出现浑浊 |
| 4 | ④⑤ | 无明显现象 | |
| 5 | 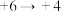 | iii___________ |
(2)实验5的化学方程式为
(3)为了进一步验证实验1中
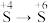 的转化,甲同学设计实验a:向反应后的溶液中先加过量稀盐酸,再加足量
的转化,甲同学设计实验a:向反应后的溶液中先加过量稀盐酸,再加足量 溶液,观察现象。
溶液,观察现象。①实验a的目的是通过检验
②加稀盐酸的作用是
乙同学认为还需要补充实验b:取等量的
 溶液,向其中先加过量稀盐酸,再加足量
溶液,向其中先加过量稀盐酸,再加足量 溶液,观察现象。
溶液,观察现象。③补充实验b的原因是
④综合实验a和b,实验1中
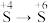 转化得以实现的证据是
转化得以实现的证据是(4)丙同学分析实验3和实验4现象不同的原因,在实验4中又添加了一种试剂
您最近一年使用:0次
解题方法
5 . 探究配制不同金属离子—氨配体溶液的差异性,实验操作及现象如下:
资料:①饱和氨水的浓度约为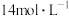
② 为浅青色沉淀
为浅青色沉淀
③ 溶液为红色,在活性炭催化下转化为橙黄色的
溶液为红色,在活性炭催化下转化为橙黄色的 溶液
溶液
(1)实验i-a中生成蓝色沉淀的离子方程式为___________ 。
(2)有研究认为蓝色沉淀中还有 成分,其可以溶于稀酸。检验蓝色沉淀中不止含
成分,其可以溶于稀酸。检验蓝色沉淀中不止含 的实验操作为:将蓝色沉淀过滤,充分洗涤后,
的实验操作为:将蓝色沉淀过滤,充分洗涤后,___________ 。(填后续操作和现象)
(3)对比实验i-a和实验i-b,从平衡移动角度,结合化学用语解释 对
对 生成有一定促进作用的原因
生成有一定促进作用的原因___________ 。
(4)对比实验i-a和实验i-c中再加入过量氨水前的反应,推测 对
对 生成有一定促进作用。设计下图所示实验:在1、2试管内分别完成对实验i-a的重复,再分别加入不同试剂。实验现象证实了预测。
生成有一定促进作用。设计下图所示实验:在1、2试管内分别完成对实验i-a的重复,再分别加入不同试剂。实验现象证实了预测。___________ ,c=___________ 。
②实验现象是___________ 。
(5)从平衡移动角度,结合化学用语,解释 对
对 生成有一定促进作用的原因
生成有一定促进作用的原因___________ 。
(6)针对实验ii未能成功配制 溶液,结合以上分析,提出改进方案:
溶液,结合以上分析,提出改进方案:
①在实验ii-a的基础上继续加入___________ ,即可成功配制。
②验证配制成功的操作及实验现象是:取①的上层红色清液,加入少许活性炭振荡试管,溶液转为橙黄色,反应的离子方程式为:___________ 。
(7)综合以上分析,配制不同金属离子—氨配体溶液的难易程度存在差异性,推测可能与以下因素有关:配位数、___________ 。
| 实验序号 | 操作 | 现象 | |
实验i: 的配制 的配制 | 实验i-a | 在试管内混合 溶液和 溶液和 溶液,再加入过量的 溶液,再加入过量的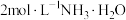 | 产生蓝色沉淀,加入 后沉淀少部分溶解,溶液变浑浊,静置后上层为深蓝色溶液。 后沉淀少部分溶解,溶液变浑浊,静置后上层为深蓝色溶液。 |
| 实验i-b | 在试管内混合 溶液和 溶液和 溶液,再加入过量的 溶液,再加入过量的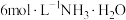 | 产生蓝色沉淀,加入 后沉淀大部分溶解,溶液变浑浊,静置后上层为深蓝色溶液。 后沉淀大部分溶解,溶液变浑浊,静置后上层为深蓝色溶液。 | |
| 实验i-c | 在试管内混合 溶液和 溶液和 溶液,再加入过量的 溶液,再加入过量的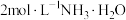 | 产生蓝色沉淀,加入 后沉淀完全溶解,得到澄清的深蓝色溶液。 后沉淀完全溶解,得到澄清的深蓝色溶液。 | |
实验ii: 的配制 的配制 | 实验ii-a | 在试管内混合 溶液和过量 溶液和过量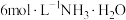 | 得到浅青色沉淀,沉淀未见明显溶解。 |
| 实验ii-b | 在试管内混合 溶液和过量 溶液和过量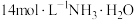 | 得到浅青色沉淀,沉淀未见明显溶解。 | |
实验iii: 的配制 的配制 | 实验iii | 在试管内混合 溶液和 溶液和 溶液,再加入过量的 溶液,再加入过量的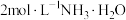 | 产生白色沉淀,加入 后沉淀完全溶解,得到无色溶液。 后沉淀完全溶解,得到无色溶液。 |
②
 为浅青色沉淀
为浅青色沉淀③
 溶液为红色,在活性炭催化下转化为橙黄色的
溶液为红色,在活性炭催化下转化为橙黄色的 溶液
溶液(1)实验i-a中生成蓝色沉淀的离子方程式为
(2)有研究认为蓝色沉淀中还有
 成分,其可以溶于稀酸。检验蓝色沉淀中不止含
成分,其可以溶于稀酸。检验蓝色沉淀中不止含 的实验操作为:将蓝色沉淀过滤,充分洗涤后,
的实验操作为:将蓝色沉淀过滤,充分洗涤后,(3)对比实验i-a和实验i-b,从平衡移动角度,结合化学用语解释
 对
对 生成有一定促进作用的原因
生成有一定促进作用的原因(4)对比实验i-a和实验i-c中再加入过量氨水前的反应,推测
 对
对 生成有一定促进作用。设计下图所示实验:在1、2试管内分别完成对实验i-a的重复,再分别加入不同试剂。实验现象证实了预测。
生成有一定促进作用。设计下图所示实验:在1、2试管内分别完成对实验i-a的重复,再分别加入不同试剂。实验现象证实了预测。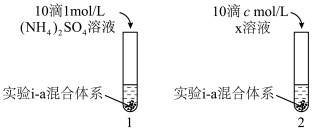
②实验现象是
(5)从平衡移动角度,结合化学用语,解释
 对
对 生成有一定促进作用的原因
生成有一定促进作用的原因(6)针对实验ii未能成功配制
 溶液,结合以上分析,提出改进方案:
溶液,结合以上分析,提出改进方案:①在实验ii-a的基础上继续加入
②验证配制成功的操作及实验现象是:取①的上层红色清液,加入少许活性炭振荡试管,溶液转为橙黄色,反应的离子方程式为:
(7)综合以上分析,配制不同金属离子—氨配体溶液的难易程度存在差异性,推测可能与以下因素有关:配位数、
您最近一年使用:0次
名校
解题方法
6 . 将足量SO2通入AgNO3溶液中,产生沉淀。探究反应原理及沉淀成分,装置如下(加热,夹持等装置略)。
资料:i.Ag2SO4微溶于水;Ag2SO3难溶于水。
ii.Ag2SO4、Ag2SO3均溶于氨水。___________ 。
②B的作用是___________ 。
(2)探究沉淀成分。实验发现,沉淀的颜色与取样时间有关,对比实验记录如下:
推测白色沉淀(t1)可能为Ag2SO4、Ag2SO3或混合物。探究如下:
①试剂a是___________ 。
②产生白色沉淀Y的原因是___________ 。
(3)推测灰黑色沉淀(t2)含Ag。探究如下:
取灰黑色沉淀,加入氨水,部分沉淀溶解,过滤,洗涤。向洗净的沉淀中加入浓HNO3,证实沉淀含Ag。现象是___________ 。
(4)通过检测 探究产生Ag的原因。
探究产生Ag的原因。
①实验:___________ 。(用化学方程式表示)
②t1时,C中产生白色沉淀的离子方程式是___________ 。
综上可知,化学反应的产物与反应速率有关。
资料:i.Ag2SO4微溶于水;Ag2SO3难溶于水。
ii.Ag2SO4、Ag2SO3均溶于氨水。
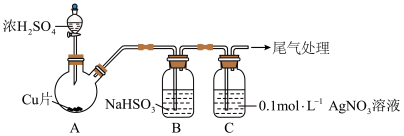
②B的作用是
(2)探究沉淀成分。实验发现,沉淀的颜色与取样时间有关,对比实验记录如下:
| 时间 | 反应开始时(t1) | 一段时间后(t2) | 较长时间后(t3) |
| 颜色 | 白色 | 灰黑色 | 灰黑色加深 |

①试剂a是
②产生白色沉淀Y的原因是
(3)推测灰黑色沉淀(t2)含Ag。探究如下:
取灰黑色沉淀,加入氨水,部分沉淀溶解,过滤,洗涤。向洗净的沉淀中加入浓HNO3,证实沉淀含Ag。现象是
(4)通过检测
 探究产生Ag的原因。
探究产生Ag的原因。①实验:
 (已排除O2的影响)
(已排除O2的影响)
②t1时,C中产生白色沉淀的离子方程式是
综上可知,化学反应的产物与反应速率有关。
您最近一年使用:0次
解题方法
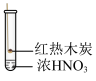
7 . 下述实验中均有红棕色气体产生,对比分析所得结论不正确的是
|
|
|
| ① | ② | ③ |
A.①中发生了反应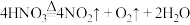 |
| B.由②中产生红棕色气体可推测木炭与浓硝酸发生了反应 |
| C.由③中有红棕色可推测出浓硝酸可能具有挥发性 |
D.③的气体产物中检测出 ,不能得出木炭与浓硝酸发生反应的结论 ,不能得出木炭与浓硝酸发生反应的结论 |
您最近一年使用:0次
8 . 某中学趣味化学实验小组的同学想通过“ 被浓
被浓 氧化”的实验,验证
氧化”的实验,验证 的还原性.
的还原性.
实验一:验证 的还原性
的还原性
(1)红棕色气体是____________ 。(写化学式)
(2)实验现象与预期不符,继续进行实验。
取深棕色溶液于试管中,滴加KSCN溶液,溶液变为红色,该现象说明___________________ 。
实验二:探究溶液变为深棕色的原因
【资料与猜想】
查阅资料后猜想,可能是生成的 或NO与溶液中的
或NO与溶液中的 或
或 反应,而使溶液变为深棕色。
反应,而使溶液变为深棕色。
【实验与探究】
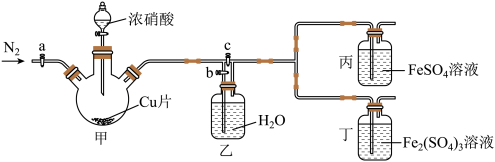
用如图所示装置进行实验(气密性已检验,尾气处理已略去)
ⅱ.向甲中加入适量浓 ,一段时间后丙中溶液变为深棕色,丁中溶液无明显变化;
,一段时间后丙中溶液变为深棕色,丁中溶液无明显变化;
ⅲ.关闭b、打开c,更换丙、丁中的溶液(试剂不变);
ⅳ.继续向甲中加入浓 ,一段时间后观察到了与ⅱ相同的实验现象。
,一段时间后观察到了与ⅱ相同的实验现象。
(3)通入 的目的是
的目的是________________________ 。
(4)铜与浓硝酸反应的离子方程式是__________________________ 。
(5)装置乙的作用是_____________________ 。
(6)实验结论:溶液的深棕色可能是因为 。
【反思与改进】
实验三:验证 的还原性
的还原性
(7)该小组同学依据实验二的结论改进了实验一,观察到了预期现象,其实验操作是向盛有____________ 的试管中滴入几滴____________ ,振荡。
 被浓
被浓 氧化”的实验,验证
氧化”的实验,验证 的还原性.
的还原性.实验一:验证
 的还原性
的还原性实验操作 | 预期现象 | 实验现象 |
向盛有2mL  溶液的试管中,滴入几滴浓硝酸,振荡。 溶液的试管中,滴入几滴浓硝酸,振荡。 | 试管中产生红棕色气体,溶液变为黄色。 | 试管中产生红棕色气体,溶液变为深棕色。 |
(1)红棕色气体是
(2)实验现象与预期不符,继续进行实验。
取深棕色溶液于试管中,滴加KSCN溶液,溶液变为红色,该现象说明
实验二:探究溶液变为深棕色的原因
【资料与猜想】
查阅资料后猜想,可能是生成的
 或NO与溶液中的
或NO与溶液中的 或
或 反应,而使溶液变为深棕色。
反应,而使溶液变为深棕色。【实验与探究】
用如图所示装置进行实验(气密性已检验,尾气处理已略去)
ⅱ.向甲中加入适量浓
 ,一段时间后丙中溶液变为深棕色,丁中溶液无明显变化;
,一段时间后丙中溶液变为深棕色,丁中溶液无明显变化;ⅲ.关闭b、打开c,更换丙、丁中的溶液(试剂不变);
ⅳ.继续向甲中加入浓
 ,一段时间后观察到了与ⅱ相同的实验现象。
,一段时间后观察到了与ⅱ相同的实验现象。(3)通入
 的目的是
的目的是(4)铜与浓硝酸反应的离子方程式是
(5)装置乙的作用是
(6)实验结论:溶液的深棕色可能是因为 。
A. 与NO发生了反应 与NO发生了反应 | B. 与 与 发生了反应 发生了反应 |
C. 与NO发生了反应 与NO发生了反应 | D. 与 与 发生了反应 发生了反应 |
【反思与改进】
实验三:验证
 的还原性
的还原性(7)该小组同学依据实验二的结论改进了实验一,观察到了预期现象,其实验操作是向盛有
您最近一年使用:0次
名校
解题方法
9 . 将足量SO2通入AgNO3溶液中,产生沉淀。探究反应原理及沉淀成分,装置如下(加热、夹持等装置略)。
资料:ⅰ.Ag2SO4微溶于水;Ag2SO3难溶于水。
ⅱ.Ag2SO4、Ag2SO3均溶于氨水。___________ 。
②用NaOH溶液吸收尾气中的SO2,产物是___________ 。
(2)探究沉淀成分。实验发现,沉淀的颜色与取样时间有关,对比实验记录如下:
推测白色沉淀(t1)可能为Ag2SO4、Ag2SO3或二者混合物。探究如下:
①t1时,C中产生白色沉淀的离子方程式是___________ 。
②试剂a是___________ 。
③产生白色沉淀Y的原因是___________ 。
(3)推测灰黑色沉淀(t2)含Ag。探究如下:
取灰黑色沉淀,加入氨水,部分沉淀溶解,过滤。向滤出的沉淀中加入浓HNO3,证实沉淀含Ag。现象是___________ 。
(4)通过检测SO 探究产生Ag的原因。
探究产生Ag的原因。___________ 。(用化学方程式表示)
综上可知,化学反应的产物与反应速率和限度有关。
资料:ⅰ.Ag2SO4微溶于水;Ag2SO3难溶于水。
ⅱ.Ag2SO4、Ag2SO3均溶于氨水。

②用NaOH溶液吸收尾气中的SO2,产物是
(2)探究沉淀成分。实验发现,沉淀的颜色与取样时间有关,对比实验记录如下:
| 时间 | 反应开始时(t1) | 一段时间后(t2) | 较长时间后(t3) |
| 颜色 | 白色 | 灰黑色 | 灰黑色加深 |

①t1时,C中产生白色沉淀的离子方程式是
②试剂a是
③产生白色沉淀Y的原因是
(3)推测灰黑色沉淀(t2)含Ag。探究如下:
取灰黑色沉淀,加入氨水,部分沉淀溶解,过滤。向滤出的沉淀中加入浓HNO3,证实沉淀含Ag。现象是
(4)通过检测SO
 探究产生Ag的原因。
探究产生Ag的原因。实验: (已排除O2的影响)
(已排除O2的影响)
综上可知,化学反应的产物与反应速率和限度有关。
您最近一年使用:0次
10 . 某小组同学探究硫代硫酸钠(Na2S2O3)溶液与某些常见金属离子的反应。
已知:i.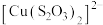 (淡绿色)、
(淡绿色)、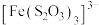 (紫黑色)、
(紫黑色)、 (无色)
(无色)
ii. 在酸性溶液中转化为
在酸性溶液中转化为 、S和SO2。
、S和SO2。
iii.BaS4O6可溶于水、BaS2O3微溶于水。
(1)将S粉加入沸腾的Na2SO3溶液中可制得Na2S2O3,离子方程式是___________ 。
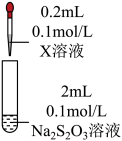
(2)研究 Na2S2O3与某些常见金属离子的反应,进行如下实验。
①取I中的浊液,离心分离,经检验,沉淀是Cu2S和S的混合物,清液中存在 。
。
i.补全I中生成黑色沉淀的总反应的离子方程式:___________
 □___________
□___________ □___________
□___________ □___________
□___________ □___________+
□___________+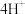
ii.查阅资料可知,常温时,生成黑色沉淀反应的平衡常数很大,但仍需水浴加热至50℃以上才出现沉淀,原因是___________ 。
②Ⅱ中, 被Fe3+氧化的主要产物是
被Fe3+氧化的主要产物是 ,还有很少量的
,还有很少量的 。取Ⅱ中的无色溶液进行如下实验证实了此结论。
。取Ⅱ中的无色溶液进行如下实验证实了此结论。
i.仅由溶液1中加入足量的盐酸后得到沉淀2,不能说明Ⅱ中生成了 ,理由是
,理由是___________ 。
ii.补全实验方案证实上述结论:将沉淀1洗净,___________ 。
③向Ⅲ的无色溶液中继续加入0.5mL 0.1mol·L-1AgNO3溶液,产生白色沉淀Ag2S2O3。静置,得到黑色沉淀Ag2S,同时生成强酸。生成Ag2S的化学方程式是___________ 。
(3)软硬酸碱原理认为,Ⅲ中, Ag+为软酸, 为软碱, S2-是比
为软碱, S2-是比 更软的碱,可解释
更软的碱,可解释 与Ag+反应的最终产物为Ag2S。由此推测,Ⅰ中, Cu+和Cu2+,
与Ag+反应的最终产物为Ag2S。由此推测,Ⅰ中, Cu+和Cu2+,___________ 是更软的酸。
已知:i.
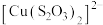 (淡绿色)、
(淡绿色)、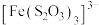 (紫黑色)、
(紫黑色)、 (无色)
(无色)ii.
 在酸性溶液中转化为
在酸性溶液中转化为 、S和SO2。
、S和SO2。iii.BaS4O6可溶于水、BaS2O3微溶于水。
(1)将S粉加入沸腾的Na2SO3溶液中可制得Na2S2O3,离子方程式是
(2)研究 Na2S2O3与某些常见金属离子的反应,进行如下实验。
| 序号 | X溶液 | 现象 |
| I | CuCl2溶液 | 溶液变为淡绿色,水浴加热至50℃以上,逐渐析出黑色沉淀 | |
| Ⅱ | FeCl3溶液 | 溶液变为紫黑色,片刻后溶液变为无色 | |
| Ⅲ | AgNO3溶液 | 逐滴加入AgNO3溶液,生成白色沉淀,振荡后沉淀溶解,得无色溶液 |
 。
。i.补全I中生成黑色沉淀的总反应的离子方程式:
 □___________
□___________ □___________
□___________ □___________
□___________ □___________+
□___________+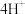
ii.查阅资料可知,常温时,生成黑色沉淀反应的平衡常数很大,但仍需水浴加热至50℃以上才出现沉淀,原因是
②Ⅱ中,
 被Fe3+氧化的主要产物是
被Fe3+氧化的主要产物是 ,还有很少量的
,还有很少量的 。取Ⅱ中的无色溶液进行如下实验证实了此结论。
。取Ⅱ中的无色溶液进行如下实验证实了此结论。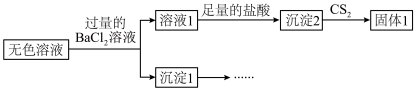
i.仅由溶液1中加入足量的盐酸后得到沉淀2,不能说明Ⅱ中生成了
 ,理由是
,理由是ii.补全实验方案证实上述结论:将沉淀1洗净,
③向Ⅲ的无色溶液中继续加入0.5mL 0.1mol·L-1AgNO3溶液,产生白色沉淀Ag2S2O3。静置,得到黑色沉淀Ag2S,同时生成强酸。生成Ag2S的化学方程式是
(3)软硬酸碱原理认为,Ⅲ中, Ag+为软酸,
 为软碱, S2-是比
为软碱, S2-是比 更软的碱,可解释
更软的碱,可解释 与Ag+反应的最终产物为Ag2S。由此推测,Ⅰ中, Cu+和Cu2+,
与Ag+反应的最终产物为Ag2S。由此推测,Ⅰ中, Cu+和Cu2+,
您最近一年使用:0次