2024·贵州黔西·一模
解题方法
1 . 硫及其化合物是十分重要的化工原料。
(1)某同学设计如图实验测定硫酸浓度(不考虑体积变化,假设锌与稀硫酸反应只产生氢气):__________ (填字母)。
②已知开始时量气管读数为 ,最终读数为
,最终读数为 (均折合成标准状况,且
(均折合成标准状况,且 )。则锌与稀硫酸发生反应的最低硫酸浓度为
)。则锌与稀硫酸发生反应的最低硫酸浓度为__________  。
。
(2)已知 具有还原性,可以还原
具有还原性,可以还原 ,也可以与
,也可以与 发生反应。
发生反应。
①将 通入装有过氧化钠的硬质试管中,将带火星的木条放在试管口处。若木条不复燃,则说明
通入装有过氧化钠的硬质试管中,将带火星的木条放在试管口处。若木条不复燃,则说明 与
与 反应无
反应无 生成,可能发生反应的化学方程式为
生成,可能发生反应的化学方程式为__________ 。
②将 通入装有碘水(含淀粉)的洗气瓶中,若
通入装有碘水(含淀粉)的洗气瓶中,若__________ ,说明还原性: ,写出该反应的离子方程式:
,写出该反应的离子方程式:__________ 。
(3)为探究 在盐酸中与Cu、
在盐酸中与Cu、 的反应,某实验小组设计如图实验。
的反应,某实验小组设计如图实验。
实验Ⅰ: ,实验Ⅰ中得到的黑色固体为
,实验Ⅰ中得到的黑色固体为 。
。
①实验Ⅰ通入 时反应的离子方程式为
时反应的离子方程式为__________ ,实验Ⅱ通入 时反应的离子方程式为
时反应的离子方程式为__________ 。
②实验Ⅱ若消耗__________  ,则生成
,则生成 个
个 。
。
(1)某同学设计如图实验测定硫酸浓度(不考虑体积变化,假设锌与稀硫酸反应只产生氢气):
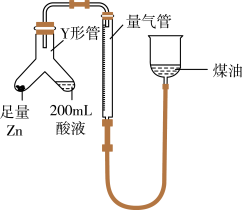
②已知开始时量气管读数为
 ,最终读数为
,最终读数为 (均折合成标准状况,且
(均折合成标准状况,且 )。则锌与稀硫酸发生反应的最低硫酸浓度为
)。则锌与稀硫酸发生反应的最低硫酸浓度为 。
。(2)已知
 具有还原性,可以还原
具有还原性,可以还原 ,也可以与
,也可以与 发生反应。
发生反应。①将
 通入装有过氧化钠的硬质试管中,将带火星的木条放在试管口处。若木条不复燃,则说明
通入装有过氧化钠的硬质试管中,将带火星的木条放在试管口处。若木条不复燃,则说明 与
与 反应无
反应无 生成,可能发生反应的化学方程式为
生成,可能发生反应的化学方程式为②将
 通入装有碘水(含淀粉)的洗气瓶中,若
通入装有碘水(含淀粉)的洗气瓶中,若 ,写出该反应的离子方程式:
,写出该反应的离子方程式:(3)为探究
 在盐酸中与Cu、
在盐酸中与Cu、 的反应,某实验小组设计如图实验。
的反应,某实验小组设计如图实验。实验Ⅰ:
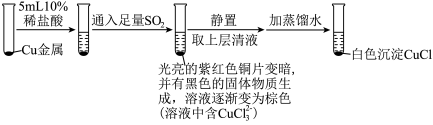
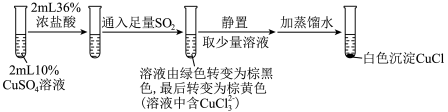
 ,实验Ⅰ中得到的黑色固体为
,实验Ⅰ中得到的黑色固体为 。
。①实验Ⅰ通入
 时反应的离子方程式为
时反应的离子方程式为 时反应的离子方程式为
时反应的离子方程式为②实验Ⅱ若消耗
 ,则生成
,则生成 个
个 。
。
您最近一年使用:0次
2024高三·全国·专题练习
解题方法
2 . 某化学兴趣小组设计如图所示装置探究物质间的氧化性大小。下列说法错误的是
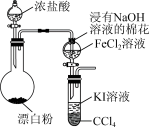
| A.烧瓶中的离子反应式为ClO-+Cl-+2H+=Cl2↑+H2O |
| B.浸有NaOH溶液的棉花起吸收尾气的作用 |
| C.CCl4可用淀粉溶液替换 |
| D.试管下层出现紫红色,可证明氧化性:Cl2>Fe3+>I2 |
您最近一年使用:0次
3 . 化学自主实验小组通过实验探究NH3、NO2的性质。
I.利用如图所示装置探究NO2能否被NH3还原(K1、K2为止水夹,夹持固定装置略去)。___________ 。
(2)甲、乙分别是___________ (填字母)。
a.浓硫酸、碱石灰 b.五氧化二磷、碱石灰
c.碱石灰、无水氯化钙 d.五氧化二磷、五氧化二磷
(3)若NO2能够被NH3还原,预期C装置中能观察到的现象是___________ 。
(4)此实验装置存在一个明显的缺陷是___________ 。
II.探究NO2、O2混合气体的喷泉实验。___________ (填字母)。
a.进气管短,出气管长 b.进气管长,出气管短 c.进气管、出气管等长
(6)G装置有多种作用,请任写出其中两种___________ 。
(7)常温常压下,G装置上的圆底烧瓶集满气体进行喷泉实验,若最终液体充满整个烧瓶,则所得溶液物质的量浓度为___________ mol·L-1(已知常温常压下气体摩尔体积为VL/mol)。
I.利用如图所示装置探究NO2能否被NH3还原(K1、K2为止水夹,夹持固定装置略去)。
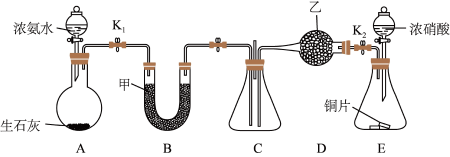
(2)甲、乙分别是
a.浓硫酸、碱石灰 b.五氧化二磷、碱石灰
c.碱石灰、无水氯化钙 d.五氧化二磷、五氧化二磷
(3)若NO2能够被NH3还原,预期C装置中能观察到的现象是
(4)此实验装置存在一个明显的缺陷是
II.探究NO2、O2混合气体的喷泉实验。
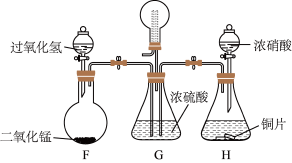
a.进气管短,出气管长 b.进气管长,出气管短 c.进气管、出气管等长
(6)G装置有多种作用,请任写出其中两种
(7)常温常压下,G装置上的圆底烧瓶集满气体进行喷泉实验,若最终液体充满整个烧瓶,则所得溶液物质的量浓度为
您最近一年使用:0次
2024-04-29更新
|
151次组卷
|
2卷引用:福建省福州九县(区、市)一中(高中)2023-2024学年高一下学期4月期中联考化学试题
4 . 兴趣小组查阅文献后,设计实验对苯酚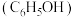 的性质进行探究,回答以下问题。
的性质进行探究,回答以下问题。
已知:ⅰ. 25℃,相关弱酸的电离平衡常数如下:Ka1(H2CO3)=4.2×10−7,Ka2(H2CO3)=5.6×10−11,Ka(C6H5OH)=1.3×10−10。
ⅱ.苯酚与 显色反应的化学方程式为:Fe3++6C6H5OH
显色反应的化学方程式为:Fe3++6C6H5OH [Fe(C6H5O)6]3−(紫色)+6H+。
[Fe(C6H5O)6]3−(紫色)+6H+。
Ⅰ.探究苯酚酸性的强弱
(1)苯酚的电离方程式为___________ 。
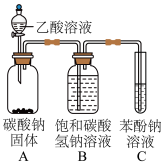
(2)兴趣小组按如图装置进行实验,证明酸性强弱顺序为CH3COOH>H2CO3> C6H5OH,所依据的实验现象为___________ ,C中反应的化学方程式为___________ 。
兴趣小组对以上实验的现象提出猜想。
猜想1: 对铁离子与苯酚的反应有促进作用。
对铁离子与苯酚的反应有促进作用。
猜想2: 对铁离子与苯酚的反应有抑制作用。
对铁离子与苯酚的反应有抑制作用。
(3)向实验1反应后溶液中继续加入 固体,若溶液颜色无变化,则可得出的结论是
固体,若溶液颜色无变化,则可得出的结论是___________ 。
(4)向实验1反应后溶液中加入___________ 固体(填化学式),若溶液颜色变为浅紫色,说明猜想2成立。
(5)兴趣小组同学提出猜想3:溶液的 会影响显色效果,并设计如下实验进行验证。
会影响显色效果,并设计如下实验进行验证。
①实验4中生成的红褐色沉淀是___________ (填化学式)。
②实验5中滴加盐酸至过量,溶液由紫色变为浅黄色,结合平衡移动原理解释原因___________ 。
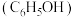 的性质进行探究,回答以下问题。
的性质进行探究,回答以下问题。已知:ⅰ. 25℃,相关弱酸的电离平衡常数如下:Ka1(H2CO3)=4.2×10−7,Ka2(H2CO3)=5.6×10−11,Ka(C6H5OH)=1.3×10−10。
ⅱ.苯酚与
 显色反应的化学方程式为:Fe3++6C6H5OH
显色反应的化学方程式为:Fe3++6C6H5OH [Fe(C6H5O)6]3−(紫色)+6H+。
[Fe(C6H5O)6]3−(紫色)+6H+。Ⅰ.探究苯酚酸性的强弱
(1)苯酚的电离方程式为
(2)兴趣小组按如图装置进行实验,证明酸性强弱顺序为CH3COOH>H2CO3> C6H5OH,所依据的实验现象为
| 实验1 | 实验2 |
|
|
猜想1:
 对铁离子与苯酚的反应有促进作用。
对铁离子与苯酚的反应有促进作用。猜想2:
 对铁离子与苯酚的反应有抑制作用。
对铁离子与苯酚的反应有抑制作用。(3)向实验1反应后溶液中继续加入
 固体,若溶液颜色无变化,则可得出的结论是
固体,若溶液颜色无变化,则可得出的结论是(4)向实验1反应后溶液中加入
(5)兴趣小组同学提出猜想3:溶液的
 会影响显色效果,并设计如下实验进行验证。
会影响显色效果,并设计如下实验进行验证。| 实验 | 操作 | 现象 |
| 3 | 向2mL苯酚溶液(调节 )中滴加0.1mol/LFeCl3溶液 )中滴加0.1mol/LFeCl3溶液 | 溶液显紫色 |
| 4 | 向2mL苯酚溶液(调节 )中滴加0.1mol/LFeCl3溶液 )中滴加0.1mol/LFeCl3溶液 | 生成红褐色沉淀 |
| 5 | 向实验4所得悬浊液中逐滴加入0.1mol/L盐酸至过量 | 沉淀逐渐溶解,溶液变为紫色;继续滴加盐酸,溶液由紫色变为浅黄色 |
②实验5中滴加盐酸至过量,溶液由紫色变为浅黄色,结合平衡移动原理解释原因
您最近一年使用:0次
2024-04-26更新
|
141次组卷
|
2卷引用:北京市北京大学附属中学2023-2024学年高二下学期期中考试化学试题
解题方法
5 . 为探究+1价Ag的氧化性,开展如下活动。
(1)配制溶液:称量→溶解→冷却→操作①→洗涤→注入→混匀→定容→操作②→装瓶贴标签
①下列图示中,操作①为_______ 、操作②为_______ 。_______ g固体。
③实验室AgNO3溶液通常盛放在_______ 试剂瓶中。
(2)通过如下实验,比较Ag+、Fe3+、I2的氧化性。
I中产生黑色沉淀,滴加KSCN溶液,变红
II中溶液呈棕黄色,滴加淀粉溶液,变蓝
III中产生黄色沉淀,滴加淀粉溶液,未变蓝
①II中反应的离子方程式为:_______ 。
②I、II中的现象说明:_______ 。
A.氧化性顺序:Ag+>Fe3+>I2 B.氧化性顺序:Fe3+>I–>Fe2+
C.还原性顺序:I–>Fe2+>Fe3+ D.还原性顺序:Fe2+>Ag>I–
③推测III中未发生Ag+氧化I–的原因_______ 。
(3)利用如下图所示装置,探究Ag+氧化I–的反应。_______ 。
A.KCl B.KNO3 C.Fe2(SO4)3
②闭合K,电流计指针偏转。“石墨2”作_______ 。
A.阴极 B.阳极 C.正极 D.负极
③已知0.1mol·L-1AgNO3溶液的pH=6。上述实验中可能是 氧化了I–,将装置中的
氧化了I–,将装置中的_______ 溶液换成_______ ,闭合K,指针未发生偏转,确认Ag+氧化了I–。
取I中产生的黑色沉淀0.0216g于试管中。进行实验:①向黑色沉淀中滴加稀硝酸使其溶解;②再向试管中滴加氨水,边滴边振荡至沉淀恰好溶解;③再向其中滴加乙醛溶液,加热,产生光亮的银镜。
(4)写出第①步反应的化学方程式。_______ 。
(5)为得到光亮的银镜,实验时应做到:_______ (任写2点)。若黑色沉淀全部转化为银镜,理论上需要乙醛_______ mol。
A.1×10-4 B.2×10-4 C.1×10-3 D.2×10-3
(1)配制溶液:称量→溶解→冷却→操作①→洗涤→注入→混匀→定容→操作②→装瓶贴标签
①下列图示中,操作①为

③实验室AgNO3溶液通常盛放在
(2)通过如下实验,比较Ag+、Fe3+、I2的氧化性。
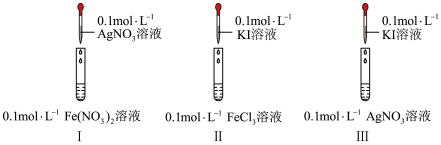
I中产生黑色沉淀,滴加KSCN溶液,变红
II中溶液呈棕黄色,滴加淀粉溶液,变蓝
III中产生黄色沉淀,滴加淀粉溶液,未变蓝
①II中反应的离子方程式为:
②I、II中的现象说明:
A.氧化性顺序:Ag+>Fe3+>I2 B.氧化性顺序:Fe3+>I–>Fe2+
C.还原性顺序:I–>Fe2+>Fe3+ D.还原性顺序:Fe2+>Ag>I–
③推测III中未发生Ag+氧化I–的原因
(3)利用如下图所示装置,探究Ag+氧化I–的反应。

A.KCl B.KNO3 C.Fe2(SO4)3
②闭合K,电流计指针偏转。“石墨2”作
A.阴极 B.阳极 C.正极 D.负极
③已知0.1mol·L-1AgNO3溶液的pH=6。上述实验中可能是
 氧化了I–,将装置中的
氧化了I–,将装置中的取I中产生的黑色沉淀0.0216g于试管中。进行实验:①向黑色沉淀中滴加稀硝酸使其溶解;②再向试管中滴加氨水,边滴边振荡至沉淀恰好溶解;③再向其中滴加乙醛溶液,加热,产生光亮的银镜。
(4)写出第①步反应的化学方程式。
(5)为得到光亮的银镜,实验时应做到:
A.1×10-4 B.2×10-4 C.1×10-3 D.2×10-3
您最近一年使用:0次
解题方法
6 . 某实验小组在探究 性质时,做了如下实验:
性质时,做了如下实验:
实验Ⅰ:向NaCl溶液中加入 溶液,溶液呈绿色。
溶液,溶液呈绿色。
实验Ⅱ:向 溶液中加入表面打磨掉氧化膜的金属Mg,产生大量气泡同时溶液中产生绿色沉淀。
溶液中加入表面打磨掉氧化膜的金属Mg,产生大量气泡同时溶液中产生绿色沉淀。
实验Ⅲ:向 溶液中加入适量氨水,溶液变为深蓝色。
溶液中加入适量氨水,溶液变为深蓝色。
实验Ⅳ:向实验Ⅲ的深蓝色溶液中加入 溶液,产生蓝色沉淀。
溶液,产生蓝色沉淀。
资料显示: 为黄色,
为黄色, 为绿色不溶物。
为绿色不溶物。
下列说法错误的是
 性质时,做了如下实验:
性质时,做了如下实验:实验Ⅰ:向NaCl溶液中加入
 溶液,溶液呈绿色。
溶液,溶液呈绿色。实验Ⅱ:向
 溶液中加入表面打磨掉氧化膜的金属Mg,产生大量气泡同时溶液中产生绿色沉淀。
溶液中加入表面打磨掉氧化膜的金属Mg,产生大量气泡同时溶液中产生绿色沉淀。实验Ⅲ:向
 溶液中加入适量氨水,溶液变为深蓝色。
溶液中加入适量氨水,溶液变为深蓝色。实验Ⅳ:向实验Ⅲ的深蓝色溶液中加入
 溶液,产生蓝色沉淀。
溶液,产生蓝色沉淀。资料显示:
 为黄色,
为黄色, 为绿色不溶物。
为绿色不溶物。下列说法错误的是
A.实验Ⅰ: 在NaCl溶液中部分转化为 在NaCl溶液中部分转化为 |
B.实验Ⅱ:Mg消耗了溶液中的 从而产生了 从而产生了 |
C.实验Ⅲ:有 生成 生成 |
D.实验Ⅳ:获得的蓝色沉淀为 |
您最近一年使用:0次
2024·重庆·模拟预测
解题方法
7 . 下列探究方案能达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 取少量Fe3O4与足量盐酸反应后的溶液于试管中,滴加几滴K3[Fe(CN)6]溶液,观察现象 | 检验Fe3O4与盐酸反应后的溶液中含有Fe2+ |
| B | 向0.1mol.L-1H2O2溶液中滴加0.1mol.L-1KMnO4溶液,观察溶液颜色变化 | 探究H2O2具有氧化性 |
| C | 向蔗糖溶液中滴加稀硫酸,水浴加热,再加入新制Cu(OH)2悬浊液 | 验证蔗糖发生水解 |
| D | 用pH试纸测定浓度均为0.lmol·L-1的CH3COONa溶液和NaClO溶液的pH,比较溶液pH大小 | 比较酸性:CH3COOH>HClO |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
8 . 某化学兴趣小组探究 溶液与
溶液与 溶液的反应。向
溶液的反应。向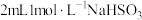 溶液
溶液 中逐滴加入
中逐滴加入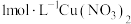 溶液,溶液变为绿色,静置
溶液,溶液变为绿色,静置 后,溶液变蓝,底部产生大量砖红色沉淀。
后,溶液变蓝,底部产生大量砖红色沉淀。
(1)测得 溶液
溶液 ,结合化学原理解释原因
,结合化学原理解释原因________________ 。
(2)甲同学认为 溶液与
溶液与 溶液发生了氧化还原反应。通过检验反应体系中是否含有
溶液发生了氧化还原反应。通过检验反应体系中是否含有 即可证明,检验
即可证明,检验 的方法是
的方法是________________ 。
(3)乙同学认为上述方法不能排除空气中 的干扰,应该进一步分析沉淀的成分。对反应产物中的砖红色沉淀提出以下假设:
的干扰,应该进一步分析沉淀的成分。对反应产物中的砖红色沉淀提出以下假设:
假设1:砖红色沉淀为 ;
;
假设2:砖红色沉淀为 ;
;
假设3:________________ ..
(4)查阅资料1: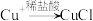 (白色难溶固体)
(白色难溶固体)
将砖红色沉淀过滤洗涤后,滴加 盐酸至过量,
盐酸至过量,________________ (填实验现象),可证明假设1成立,同时溶液变为蓝绿色,并伴有刺激性气味的气体生成。
(5)丙同学做对照实验时,向 中滴加
中滴加 盐酸至过量后,没有观察到溶液变蓝和生成气体的现象。因此,他认为砖红色沉淀中还可能含有其它成分,并设计实验进行证实。
盐酸至过量后,没有观察到溶液变蓝和生成气体的现象。因此,他认为砖红色沉淀中还可能含有其它成分,并设计实验进行证实。
①刺激性气味的气体可能是 或
或 ,在试管口用
,在试管口用蘸有碘水的淀粉试纸 检验,发现蓝色褪去,写出反应的离子方程式________________ 。
②向红色沉淀中加入过量氨水,发现沉淀溶解,溶液立即变蓝。 被空气氧化缓慢变蓝的原理
被空气氧化缓慢变蓝的原理________________ 。
③上述实验现象表明,砖红沉淀中除了含有 外,还含有
外,还含有________ 。(写出离子成分即可)
(6)丁同学通过如图装置证明了此条件下, 也能氧化
也能氧化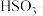 ,图中甲溶液是
,图中甲溶液是________ ,通过对比实验证明了此时空气中的 不是
不是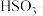 被氧化的主要原因,操作及现象是
被氧化的主要原因,操作及现象是________________ 。
 溶液与
溶液与 溶液的反应。向
溶液的反应。向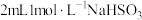 溶液
溶液 中逐滴加入
中逐滴加入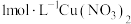 溶液,溶液变为绿色,静置
溶液,溶液变为绿色,静置 后,溶液变蓝,底部产生大量砖红色沉淀。
后,溶液变蓝,底部产生大量砖红色沉淀。(1)测得
 溶液
溶液 ,结合化学原理解释原因
,结合化学原理解释原因(2)甲同学认为
 溶液与
溶液与 溶液发生了氧化还原反应。通过检验反应体系中是否含有
溶液发生了氧化还原反应。通过检验反应体系中是否含有 即可证明,检验
即可证明,检验 的方法是
的方法是(3)乙同学认为上述方法不能排除空气中
 的干扰,应该进一步分析沉淀的成分。对反应产物中的砖红色沉淀提出以下假设:
的干扰,应该进一步分析沉淀的成分。对反应产物中的砖红色沉淀提出以下假设:假设1:砖红色沉淀为
 ;
;假设2:砖红色沉淀为
 ;
;假设3:
(4)查阅资料1:
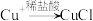 (白色难溶固体)
(白色难溶固体)将砖红色沉淀过滤洗涤后,滴加
 盐酸至过量,
盐酸至过量,(5)丙同学做对照实验时,向
 中滴加
中滴加 盐酸至过量后,没有观察到溶液变蓝和生成气体的现象。因此,他认为砖红色沉淀中还可能含有其它成分,并设计实验进行证实。
盐酸至过量后,没有观察到溶液变蓝和生成气体的现象。因此,他认为砖红色沉淀中还可能含有其它成分,并设计实验进行证实。①刺激性气味的气体可能是
 或
或 ,在试管口用
,在试管口用②向红色沉淀中加入过量氨水,发现沉淀溶解,溶液立即变蓝。
查阅资料2:
 被空气氧化缓慢变蓝的原理
被空气氧化缓慢变蓝的原理③上述实验现象表明,砖红沉淀中除了含有
 外,还含有
外,还含有(6)丁同学通过如图装置证明了此条件下,
 也能氧化
也能氧化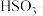 ,图中甲溶液是
,图中甲溶液是 不是
不是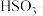 被氧化的主要原因,操作及现象是
被氧化的主要原因,操作及现象是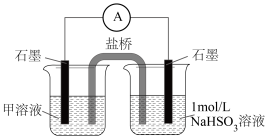
您最近一年使用:0次
9 . 高铁酸钾(K2FeO4,极易溶于水,溶液呈紫红色)是一种绿色净水剂,易溶于水。某小组在实验室条件下制备K2FeO4并探究其性质。回答下列问题:
实验(一)制备K2FeO4。___________ ,装置B的作用是___________ ,盛装的试剂为 ___________ 。
(2)装置C中生成K2FeO4的化学方程式为___________
实验(二)探究K₂FeO4的性质。
(3)R溶液为______ (填“稀硫酸”或“盐酸”),写出装置a中的离子方程式:____________ ,不选择另一种酸的主要原因是____________ .
(4)设计一种方案检验从d口逸出的气体:______ 。
ll.探究K₂FeO4在酸性条件下的氧化性。
(5)向K₂FeO4溶液中滴加少量用稀硫酸酸化后的MnSO4溶液,溶液呈紫红色。______ (填“能”或“不能”)证明氧化性:  >MnSO4,原因是
>MnSO4,原因是____________ (用文字说明)。
实验(一)制备K2FeO4。

(2)装置C中生成K2FeO4的化学方程式为
实验(二)探究K₂FeO4的性质。
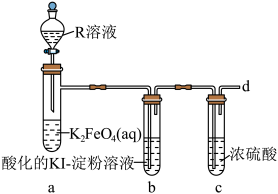
(3)R溶液为
(4)设计一种方案检验从d口逸出的气体:
ll.探究K₂FeO4在酸性条件下的氧化性。
(5)向K₂FeO4溶液中滴加少量用稀硫酸酸化后的MnSO4溶液,溶液呈紫红色。
 >MnSO4,原因是
>MnSO4,原因是
您最近一年使用:0次
23-24高一下·江西宜春·开学考试
名校
解题方法
10 . 某化学兴趣小组在实验室用除去表面氧化物的铁钉(碳素钢)与浓硫酸共热制取SO2并完成相关性质探究(不考虑水蒸气)。(已知:C+2H2SO4(浓) CO2+2SO2↑+2H2O)
CO2+2SO2↑+2H2O)
(1)有同学认为制得的SO2中可能混有杂质,其化学式为___________ 。
(2)为验证气体成分,兴趣小组同学设计了如图所示装置进行了实验探究。___________ ;装置C中品红溶液的作用是___________ 。
②装置H的作用为___________ 。
(3)兴趣小组设计如图装置验证二氧化硫的化学性质。___________ ;
②为验证SO2的还原性,取试管b中充分反应后的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液加入品红溶液,红色褪去;
方案Ⅱ:向第二份溶液加入BaCl2溶液,产生白色沉淀;
方案Ⅲ:向第三份溶液中加入AgNO3溶液,有白色沉淀生成。
上述方案中合理的是___________ (填Ⅰ、Ⅱ或Ⅲ);试管b中发生反应的离子方程式为___________ 。
 CO2+2SO2↑+2H2O)
CO2+2SO2↑+2H2O)(1)有同学认为制得的SO2中可能混有杂质,其化学式为
(2)为验证气体成分,兴趣小组同学设计了如图所示装置进行了实验探究。

②装置H的作用为
(3)兴趣小组设计如图装置验证二氧化硫的化学性质。

②为验证SO2的还原性,取试管b中充分反应后的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液加入品红溶液,红色褪去;
方案Ⅱ:向第二份溶液加入BaCl2溶液,产生白色沉淀;
方案Ⅲ:向第三份溶液中加入AgNO3溶液,有白色沉淀生成。
上述方案中合理的是
您最近一年使用:0次
2024-02-28更新
|
651次组卷
|
7卷引用:专题03 常见气体的实验室制取(考题猜想)(6大题型)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)
(已下线)专题03 常见气体的实验室制取(考题猜想)(6大题型)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)江西省南昌市第十九中学2023-2024学年高一下学期3月月考化学试题河北省石家庄市河北正定中学2023-2024学年高一下学期第一次月考(3月)化学试题辽宁省长海县高级中学2023-2024下学期第一次月考高一化学试卷天津市武清区黄花店中学2023-2024学年高一下学期第一次月考化学试题(理科)江西省丰城中学2023-2024学年高一下学期开学化学试题湖南省常德市第一中学2023-2024学年高一下学期第一次月考化学试题





