名校
解题方法
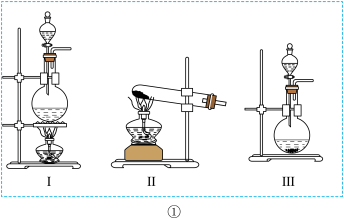
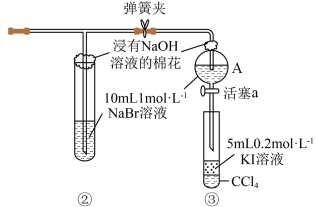
1 . 为验证卤素单质氧化性的相对强弱,某小组用如图所示装置进行实验。(夹持仪器已略去,气密性已检查)
i.打开弹簧夹,滴加浓盐酸,开始制备氯气。
ⅱ.当②中试管内和 处分液漏斗中的溶液都变为黄色时,夹紧弹簧夹。
处分液漏斗中的溶液都变为黄色时,夹紧弹簧夹。
ⅲ.当②中试管内溶液由黄色变为棕红色时,停止滴加浓盐酸。
ⅳ.……
(1)若以二氧化锰和浓盐酸为原料制取氯气,则装置①应选用___________ (填“I”“Ⅱ”或“Ⅲ”),其反应的离子方程式为___________ 。
(2)②中试管内发生反应的离子方程式是___________ 。
(3)为验证溴的氧化性强于碘,可进行的操作Ⅳ和预期的实验现象为___________ 。
(4)操作ⅲ实验的目的是___________ 。
(5)浸有 溶液的棉花可以吸收可能逸出的
溶液的棉花可以吸收可能逸出的 ,相关反应的离子方程式为
,相关反应的离子方程式为___________ 。
(6)解释氯、溴、碘单质的氧化性逐渐减弱的原因:___________ 。
i.打开弹簧夹,滴加浓盐酸,开始制备氯气。
ⅱ.当②中试管内和
 处分液漏斗中的溶液都变为黄色时,夹紧弹簧夹。
处分液漏斗中的溶液都变为黄色时,夹紧弹簧夹。ⅲ.当②中试管内溶液由黄色变为棕红色时,停止滴加浓盐酸。
ⅳ.……
(1)若以二氧化锰和浓盐酸为原料制取氯气,则装置①应选用
(2)②中试管内发生反应的离子方程式是
(3)为验证溴的氧化性强于碘,可进行的操作Ⅳ和预期的实验现象为
(4)操作ⅲ实验的目的是
(5)浸有
 溶液的棉花可以吸收可能逸出的
溶液的棉花可以吸收可能逸出的 ,相关反应的离子方程式为
,相关反应的离子方程式为(6)解释氯、溴、碘单质的氧化性逐渐减弱的原因:
您最近一年使用:0次
昨日更新
|
15次组卷
|
2卷引用:山东省联考2023-2024学年高一下学期5月月考化学试题
2 . 某化学兴趣小组在实验室用除去表面氧化物的铁钉(碳素钢)与浓硫酸共热制取 并完成相关性质探究(不考虑水蒸气)。(已知:
并完成相关性质探究(不考虑水蒸气)。(已知: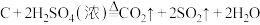 )
)
(1)有同学认为制得的 中可能混有杂质,其化学式为
中可能混有杂质,其化学式为___________ 。
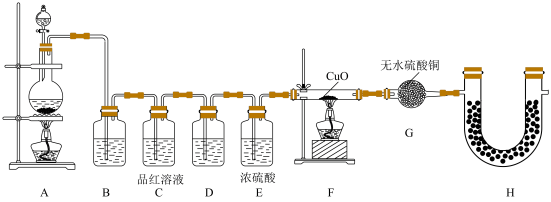
(2)为验证气体成分,兴趣小组同学设计了如图所示装置进行了实验探究。 ,装置B中加入的试剂为
,装置B中加入的试剂为___________ ;装置 中品红溶液的作用是
中品红溶液的作用是___________ 。
(3)兴趣小组设计如图装置验证二氧化硫的化学性质。 具有氧化性的实验现象为
具有氧化性的实验现象为___________ 。
②为验证 的还原性,取试管
的还原性,取试管 中充分反应后的溶液分成三份,分别进行如下实验:
中充分反应后的溶液分成三份,分别进行如下实验:
方案 :向第一份溶液加入品红溶液,红色褪去;
:向第一份溶液加入品红溶液,红色褪去;
方案 :向第二份溶液加入
:向第二份溶液加入 溶液,产生白色沉淀;
溶液,产生白色沉淀;
方案 :向第三份溶液中加入
:向第三份溶液中加入 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。
上述方案中合理的是___________ (填 、
、 或
或 );试管
);试管 中发生反应的离子方程式为
中发生反应的离子方程式为___________ 。
 并完成相关性质探究(不考虑水蒸气)。(已知:
并完成相关性质探究(不考虑水蒸气)。(已知: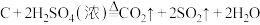 )
)(1)有同学认为制得的
 中可能混有杂质,其化学式为
中可能混有杂质,其化学式为(2)为验证气体成分,兴趣小组同学设计了如图所示装置进行了实验探究。
 ,装置B中加入的试剂为
,装置B中加入的试剂为 中品红溶液的作用是
中品红溶液的作用是(3)兴趣小组设计如图装置验证二氧化硫的化学性质。
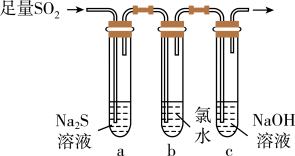
 具有氧化性的实验现象为
具有氧化性的实验现象为②为验证
 的还原性,取试管
的还原性,取试管 中充分反应后的溶液分成三份,分别进行如下实验:
中充分反应后的溶液分成三份,分别进行如下实验:方案
 :向第一份溶液加入品红溶液,红色褪去;
:向第一份溶液加入品红溶液,红色褪去;方案
 :向第二份溶液加入
:向第二份溶液加入 溶液,产生白色沉淀;
溶液,产生白色沉淀;方案
 :向第三份溶液中加入
:向第三份溶液中加入 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。上述方案中合理的是
 、
、 或
或 );试管
);试管 中发生反应的离子方程式为
中发生反应的离子方程式为
您最近一年使用:0次
解题方法
3 . I、回答下列问题
(1)以太阳能为热源,利用纳米级 可获得氢气,过程如图所示,整个过程的催化剂为
可获得氢气,过程如图所示,整个过程的催化剂为___________ (填名称);过程I的化学方程式为___________ ;反应中生成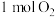 ,则同时生成
,则同时生成
___________ L(标准状况下)。
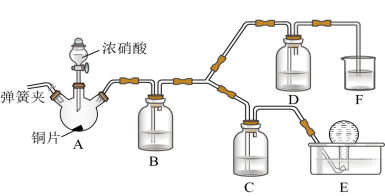
(2)按如图所示装置进行实验(加持装置已略去),实验证明浓硝酸的氧化性强于稀硝酸,依据为浓硝酸能将NO氧化为NO2,而稀硝酸不能。
①浓硝酸应保存在棕色试剂瓶中,用化学方程式解释其原因为___________ 。
②装置A中发生反应的化学方程式为___________ ;装置B的作用为___________ 。
③装置D中的现象为___________ ;C中盛放的试剂为___________ 。
(3)在碱性条件下, 被氧气氧化为
被氧气氧化为 的总反应的离子方程式为
的总反应的离子方程式为___________ 。
(1)以太阳能为热源,利用纳米级
 可获得氢气,过程如图所示,整个过程的催化剂为
可获得氢气,过程如图所示,整个过程的催化剂为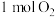 ,则同时生成
,则同时生成

(2)按如图所示装置进行实验(加持装置已略去),实验证明浓硝酸的氧化性强于稀硝酸,依据为浓硝酸能将NO氧化为NO2,而稀硝酸不能。
①浓硝酸应保存在棕色试剂瓶中,用化学方程式解释其原因为
②装置A中发生反应的化学方程式为
③装置D中的现象为
(3)在碱性条件下,
 被氧气氧化为
被氧气氧化为 的总反应的离子方程式为
的总反应的离子方程式为
您最近一年使用:0次
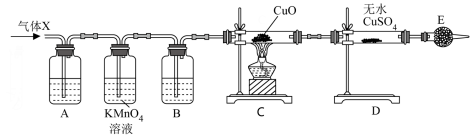
4 . 某课外活动小组的同学在实验室做锌与浓硫酸反应的实验中,甲同学认为产生的气体是二氧化硫,而乙同学认为除二氧化硫气体外,还可能产生氢气。为了验证哪位同学的判断正确,丙同学设计了图中的实验装置(锌与浓硫酸共热时产生的气体为X,且该反应装置略去)。
(1)上述反应中生成二氧化硫的化学方程式为__________________ 。
(2)乙同学认为还可能产生氢气的理由是______________ (写离子方程式)。
(3)丙同学在安装好装置后,必须首先进行的一步操作是________ 。
(4)A中加入的试剂可能是___________ ;
B中加入的试剂作用是_______________ ;
E中加入的试剂作用是______________ 。
(5)可以证明气体X中含有氢气的实验现象是C中:_____________________ ,同时D中:________________ 。
(1)上述反应中生成二氧化硫的化学方程式为
(2)乙同学认为还可能产生氢气的理由是
(3)丙同学在安装好装置后,必须首先进行的一步操作是
(4)A中加入的试剂可能是
B中加入的试剂作用是
E中加入的试剂作用是
(5)可以证明气体X中含有氢气的实验现象是C中:
您最近一年使用:0次
名校
解题方法
5 . 醋酸钴与双水杨醛缩乙二胺形成的配合物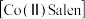 具有可逆载氧能力,能模拟金属蛋白的载氧作用,在催化氧化反应中应用广泛,合成反应如图。回答下列问题:
具有可逆载氧能力,能模拟金属蛋白的载氧作用,在催化氧化反应中应用广泛,合成反应如图。回答下列问题:___________ (填名称,下同),B处应安装的仪器是___________ ;装置C的作用是___________ ,通氮气的目的是___________ 。
(2)回流 ,沉淀转化为暗红色晶体。回流结束后进行如下操作:
,沉淀转化为暗红色晶体。回流结束后进行如下操作:
①停止通氮气 ②停止加热 ③关闭冷凝水
正确的操作顺序为___________ (填标号)。充分冷却后将溶液过滤,洗涤并干燥,得到配合物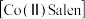 。
。
(3)测定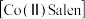 的载氧能力。将
的载氧能力。将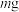 的
的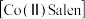 (相对分子质量为
(相对分子质量为 )加入圆底烧瓶中,在恒压漏斗中加入
)加入圆底烧瓶中,在恒压漏斗中加入 (配合物在
(配合物在 中可吸氧),如图搭建装置。
中可吸氧),如图搭建装置。___________ ,然后调节水平仪的水位至与量气管水位产生一定液面差。装置不漏气的现象是___________ 。
②调整水平仪高度,待___________ (填现象)时,记录量气管水位的体积刻度为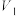 。将
。将 加入圆底烧瓶,待吸氧反应结束并规范操作后,记录量气管水位的体积刻度为
加入圆底烧瓶,待吸氧反应结束并规范操作后,记录量气管水位的体积刻度为 。已知大气压为
。已知大气压为 ,氧气的压强为
,氧气的压强为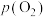 ,温度为
,温度为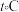 。配合物载氧量的
。配合物载氧量的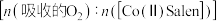 计算式为
计算式为___________ 。
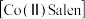 具有可逆载氧能力,能模拟金属蛋白的载氧作用,在催化氧化反应中应用广泛,合成反应如图。回答下列问题:
具有可逆载氧能力,能模拟金属蛋白的载氧作用,在催化氧化反应中应用广泛,合成反应如图。回答下列问题:
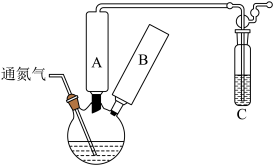
(2)回流
 ,沉淀转化为暗红色晶体。回流结束后进行如下操作:
,沉淀转化为暗红色晶体。回流结束后进行如下操作:①停止通氮气 ②停止加热 ③关闭冷凝水
正确的操作顺序为
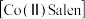 。
。(3)测定
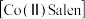 的载氧能力。将
的载氧能力。将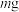 的
的 (相对分子质量为
(相对分子质量为 )加入圆底烧瓶中,在恒压漏斗中加入
)加入圆底烧瓶中,在恒压漏斗中加入 (配合物在
(配合物在 中可吸氧),如图搭建装置。
中可吸氧),如图搭建装置。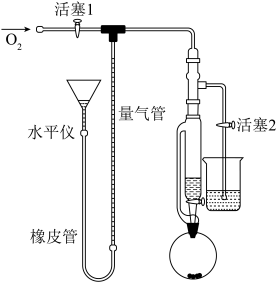
②调整水平仪高度,待
 。将
。将 加入圆底烧瓶,待吸氧反应结束并规范操作后,记录量气管水位的体积刻度为
加入圆底烧瓶,待吸氧反应结束并规范操作后,记录量气管水位的体积刻度为 。已知大气压为
。已知大气压为 ,氧气的压强为
,氧气的压强为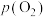 ,温度为
,温度为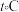 。配合物载氧量的
。配合物载氧量的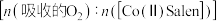 计算式为
计算式为
您最近一年使用:0次
名校
解题方法
6 . 某化学兴趣小组在习题解析中看到:“ 通入
通入 溶液出现白色沉淀,是因为在酸性环境中,
溶液出现白色沉淀,是因为在酸性环境中, 将
将 氧化成
氧化成 而产生沉淀”,有同学对这个解析提出了质疑,“因没有隔绝空气,也许只是
而产生沉淀”,有同学对这个解析提出了质疑,“因没有隔绝空气,也许只是 氧化了
氧化了 ,与
,与 无关”,于是做了“
无关”,于是做了“ 通入
通入 溶液”的探究实验,用pH传感器检测反应的进行,实验装置如图:
溶液”的探究实验,用pH传感器检测反应的进行,实验装置如图:_______________________ 。
(2)为探究硫酸钡产生的原因,分别在装置C中进行以下探究实验,则③④号实验,应该选用的试剂为____________ 。
(3)进行①③号实验前通入氮气的目的是________________________ 。
(4)实验现象:①号依然澄清,②③④号均出现浑浊。据此请补充②号实验中装置C中反应生成沉淀的化学方程式__________________________________ 。
(5)图1~4分别为①②③④号实验所测pH随时间变化曲线。_______________________ 。
(6)计算实验②500s时产生硫酸钡的质量为__________ mg。(可忽略 溶于水产生的
溶于水产生的 )
)
 通入
通入 溶液出现白色沉淀,是因为在酸性环境中,
溶液出现白色沉淀,是因为在酸性环境中, 将
将 氧化成
氧化成 而产生沉淀”,有同学对这个解析提出了质疑,“因没有隔绝空气,也许只是
而产生沉淀”,有同学对这个解析提出了质疑,“因没有隔绝空气,也许只是 氧化了
氧化了 ,与
,与 无关”,于是做了“
无关”,于是做了“ 通入
通入 溶液”的探究实验,用pH传感器检测反应的进行,实验装置如图:
溶液”的探究实验,用pH传感器检测反应的进行,实验装置如图:
(2)为探究硫酸钡产生的原因,分别在装置C中进行以下探究实验,则③④号实验,应该选用的试剂为
编号 | ① | ② | ③ | ④ |
试剂 | 煮沸过的0.1mol/L 溶液50mL,再加入食用油25mL 溶液50mL,再加入食用油25mL | 未煮沸过的0.1mol/L 溶液50mL 溶液50mL | 煮沸过的________溶液50mL,再加入食用油25mL | 未煮沸过的__________溶液50mL |
(3)进行①③号实验前通入氮气的目的是
(4)实验现象:①号依然澄清,②③④号均出现浑浊。据此请补充②号实验中装置C中反应生成沉淀的化学方程式
(5)图1~4分别为①②③④号实验所测pH随时间变化曲线。

(6)计算实验②500s时产生硫酸钡的质量为
 溶于水产生的
溶于水产生的 )
)
您最近一年使用:0次
名校
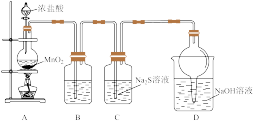
7 . 甲同学设计图1装置探究硫和氯的非金属性相对强弱。_______ 。B装置的作用是除去Cl2中的HCl,则B中的试剂是_______ (填名称),D装置的作用是_______ 。
(2)实验过程中,C中产生浅黄色沉淀,写出C中反应的离子方程式:_______ 。通过实验证明氯的非金属性比硫强,则从原子结构角度的合理解释是_______ 。
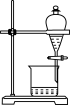
(3)若利用上图装置探究碘和氯的非金属性相对强弱,需要改动的一处是_______ 。用CCl4萃取碘水中的碘,下图的分液漏斗中,下层液体呈_______ 色;打开分液漏斗活塞,却未见液体流下,原因可能是_______ 。
(2)实验过程中,C中产生浅黄色沉淀,写出C中反应的离子方程式:
(3)若利用上图装置探究碘和氯的非金属性相对强弱,需要改动的一处是
您最近一年使用:0次
名校
解题方法
8 . 某研究性学习小组根据元素周期律预测物质性质并实验验证。
I.甲同学设计实验探究碳、硅元素的非金属性的相对强弱,回答下列问题:(已知酸性强弱:亚硫酸 碳酸)
碳酸)
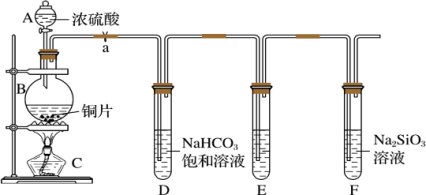
(1)仪器B中反应的化学方程式为______ 。
试管E中盛放的试剂是______ (填试剂名称)。
(2)能说明碳元素的非金属性比硅元素非金属性强的实验现象是______ 。
(3)试管D中产生 能否说明硫元素的非金属性强于碳
能否说明硫元素的非金属性强于碳______ (填“是”或“否”)。
Ⅱ.镓 及其化合物应用广泛,常用于半导体、合金材料等工业。
及其化合物应用广泛,常用于半导体、合金材料等工业。
(4)镓(Ga)在周期表中的位置______ ,GaAs熔融状态不导电,该化合物是______ (填“共价化合物”或“离子化合物”)。
(5) 作为第三代半导体材料,具有耐高温、耐高电压等特性,随着
作为第三代半导体材料,具有耐高温、耐高电压等特性,随着 技术的发展,
技术的发展, 商用进入快车道。某学校化学兴趣小组在实验室利用如图装置模拟制备氮化镓:
商用进入快车道。某学校化学兴趣小组在实验室利用如图装置模拟制备氮化镓:
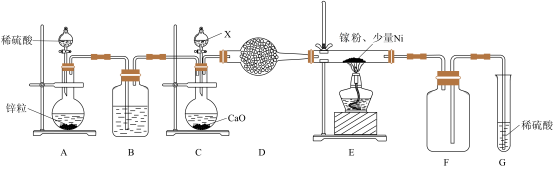
①仪器 中的试剂是
中的试剂是______ 。
②加热前需先打开A中的活塞一段时间,目的是______ 。
 中球形干燥管盛放的试剂是
中球形干燥管盛放的试剂是______ (填字母)。
a.无水 b.
b. c.无水
c.无水 d.碱石灰
d.碱石灰
③ 中生成
中生成 的化学方程式为
的化学方程式为______ 。
④装置 的作用为
的作用为______ 。
I.甲同学设计实验探究碳、硅元素的非金属性的相对强弱,回答下列问题:(已知酸性强弱:亚硫酸
 碳酸)
碳酸)
(1)仪器B中反应的化学方程式为
试管E中盛放的试剂是
(2)能说明碳元素的非金属性比硅元素非金属性强的实验现象是
(3)试管D中产生
 能否说明硫元素的非金属性强于碳
能否说明硫元素的非金属性强于碳Ⅱ.镓
 及其化合物应用广泛,常用于半导体、合金材料等工业。
及其化合物应用广泛,常用于半导体、合金材料等工业。(4)镓(Ga)在周期表中的位置
(5)
 作为第三代半导体材料,具有耐高温、耐高电压等特性,随着
作为第三代半导体材料,具有耐高温、耐高电压等特性,随着 技术的发展,
技术的发展, 商用进入快车道。某学校化学兴趣小组在实验室利用如图装置模拟制备氮化镓:
商用进入快车道。某学校化学兴趣小组在实验室利用如图装置模拟制备氮化镓:
①仪器
 中的试剂是
中的试剂是②加热前需先打开A中的活塞一段时间,目的是
 中球形干燥管盛放的试剂是
中球形干燥管盛放的试剂是a.无水
 b.
b. c.无水
c.无水 d.碱石灰
d.碱石灰③
 中生成
中生成 的化学方程式为
的化学方程式为④装置
 的作用为
的作用为
您最近一年使用:0次
2024-04-08更新
|
114次组卷
|
2卷引用:山东省济南市山东省实验中学2023-2024学年高一下学期3月月考化学试题
名校
解题方法
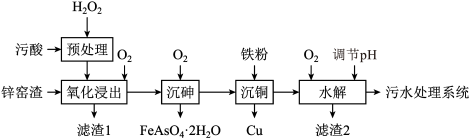
9 . 工业污酸因酸性强,且含有大量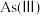 等毒性物质不可直接排放,用锌冶炼窑渣处理含砷废酸可实现砷、酸的高效脱除,同时获得有价金属铜、铁。
等毒性物质不可直接排放,用锌冶炼窑渣处理含砷废酸可实现砷、酸的高效脱除,同时获得有价金属铜、铁。
已知:①锌窑渣主要成分: 等
等
②氧化浸出后上清液主要成分( )
)
(1)为提高污酸中 的消除率,可采取的措施有
的消除率,可采取的措施有___________ 。
a.将锌窑渣粉碎 b.提高液固比 c.延长浸取时间 d.适当升温
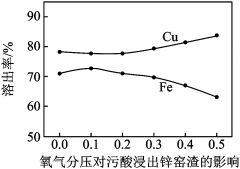
(2)氧化浸出步骤,氧气分压对 溶出率的影响如图所示,试分析氧气分压过大时,铁元素溶出率变化的可能原因:
溶出率的影响如图所示,试分析氧气分压过大时,铁元素溶出率变化的可能原因:___________ ;若该步骤不通入氧气,将影响锌窑渣中___________ (填化学式)成分的溶浸。
(3)滤渣2的主要成分为___________ (填化学式)
(4)基态砷原子价电子轨道表示式为___________ 。
(5)⑤已知: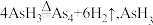 的VSEPR模型为
的VSEPR模型为___________ ,分子空间结构为___________ ,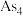 为正四面体结构,则
为正四面体结构,则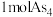 中含
中含___________  键。
键。
(6)《本草纲目》中记载砒霜(As2O3)可入药,已知: 的熔点为312.3℃,沸点为465℃。古代采用“升华法”提纯砒霜,砒霜升华时破坏的作用力为
的熔点为312.3℃,沸点为465℃。古代采用“升华法”提纯砒霜,砒霜升华时破坏的作用力为___________ 。
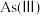 等毒性物质不可直接排放,用锌冶炼窑渣处理含砷废酸可实现砷、酸的高效脱除,同时获得有价金属铜、铁。
等毒性物质不可直接排放,用锌冶炼窑渣处理含砷废酸可实现砷、酸的高效脱除,同时获得有价金属铜、铁。
已知:①锌窑渣主要成分:
 等
等②氧化浸出后上清液主要成分(
 )
) |  |  | Cu2+ |  (主要以 (主要以 形式存在) 形式存在) |
| 18.9 | 17.8 | 6.6 | 1.65 | 8.85 |
(1)为提高污酸中
 的消除率,可采取的措施有
的消除率,可采取的措施有a.将锌窑渣粉碎 b.提高液固比 c.延长浸取时间 d.适当升温
(2)氧化浸出步骤,氧气分压对
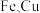 溶出率的影响如图所示,试分析氧气分压过大时,铁元素溶出率变化的可能原因:
溶出率的影响如图所示,试分析氧气分压过大时,铁元素溶出率变化的可能原因:
(3)滤渣2的主要成分为
(4)基态砷原子价电子轨道表示式为
(5)⑤已知:
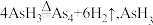 的VSEPR模型为
的VSEPR模型为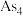 为正四面体结构,则
为正四面体结构,则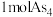 中含
中含 键。
键。(6)《本草纲目》中记载砒霜(As2O3)可入药,已知:
 的熔点为312.3℃,沸点为465℃。古代采用“升华法”提纯砒霜,砒霜升华时破坏的作用力为
的熔点为312.3℃,沸点为465℃。古代采用“升华法”提纯砒霜,砒霜升华时破坏的作用力为
您最近一年使用:0次
10 . 实验安全至关重要。以下两个金属性质探究实验:
实验i:探究金属钠的化学性质
实验ii:探究铁与水蒸气的反应
相关操作符合实验安全要求的是
实验i:探究金属钠的化学性质
实验ii:探究铁与水蒸气的反应
相关操作符合实验安全要求的是
| A.实验i:用镊子将金属钠从试剂瓶中取出,在玻璃片上用小刀切下绿豆粒大小的一块钠,放入盛有水的水槽中,使钠与水反应 |
B.实验 :将一小块钠放入试管中,酒精灯预热后再固定加热,使钠与氧气反应 :将一小块钠放入试管中,酒精灯预热后再固定加热,使钠与氧气反应 |
| C.实验ii:将少量铁粉与水的混合物放置于试管中,管口用带导管的橡胶塞塞紧并略向下倾斜,导管末端插入肥皂液中,用酒精灯预热后再固定加热,使铁与水反应 |
| D.实验ii:在导管口附近用火柴点燃产生的肥皂泡,有爆鸣声,验证有氢气产生 |
您最近一年使用:0次



