1 . 在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应,应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”,请回答该实验中的问题。_______ ,该反应的氧化剂是_______ 。
(2)圆底烧瓶中盛装的水,该装置受热后的主要作用是_______ ;烧瓶底部放置了几片碎瓷片,其作用是_______ 。
(3)酒精灯和酒精喷灯点燃的顺序是先点燃_______ 。
(4)试管中收集气体是_______ ,如果要在A处玻璃管处点燃该气体,则必须对该气体进行_______ 。
(5)若该反应中有16.8gFe参加反应,则生成H2的质量为_______ g。
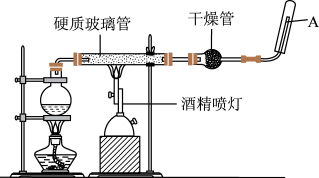
(2)圆底烧瓶中盛装的水,该装置受热后的主要作用是
(3)酒精灯和酒精喷灯点燃的顺序是先点燃
(4)试管中收集气体是
(5)若该反应中有16.8gFe参加反应,则生成H2的质量为
您最近一年使用:0次
2023-03-02更新
|
132次组卷
|
2卷引用:吉林省洮南市第一中学2022-2023学年高一上学期期末考试化学试题
2 . 某小组同学用如图所示装置进行铜与浓硫酸的反应,并探究产物的性质(夹持装置已略去)。
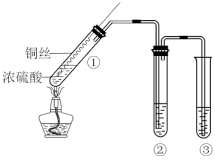
(1)试管①中反应的化学方程式是____ ;浓硫酸表现出了____ 性和____ 性。
(2)若试管②中的试剂为品红溶液,实验中观察到的现象是____ ;若试管②中的试剂为酸性KMnO4溶液,实验时,观察到溶液褪色,则说明生成的气体具有___ 性;若试管②中的试剂为新制氯水则对应的离子方程式为____ 。
(3)试管③中的试剂为NaOH溶液,其作用是___ ,反应的化学方程式是___ 。

(1)试管①中反应的化学方程式是
(2)若试管②中的试剂为品红溶液,实验中观察到的现象是
(3)试管③中的试剂为NaOH溶液,其作用是
您最近一年使用:0次
2022-04-22更新
|
84次组卷
|
2卷引用:吉林省大安市第六中学校2021-2022学年高一下学期期中考试化学试题
3 . 下图是实验室制取、提纯氯气及研究氯气性质的装置图。请回答:
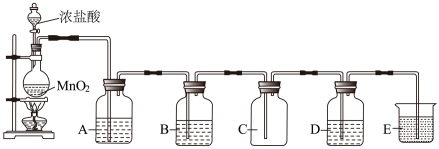
(1)装有浓盐酸的仪器的名称___________ ;A中一般应盛有___________ (填写试剂名称)。
(2)烧瓶中发生反应的化学方程式为___________ 。
(3)若D中盛有紫色石蕊试液,则D中的现象是___________ ,用离子方程式解释这种现象___________ 。
(4)若D中是FeCl2溶液,发生的现象是_______ ,反应的离子方程式为________ 。
(5)若D中盛有KI—淀粉的混合溶液,现象是___________ 。
(6)E中一般应盛有___________ ,其作用是___________ 。
(7)若有17.4gMnO2完全反应,则可生成标准状况下Cl2的体积_______ L。

(1)装有浓盐酸的仪器的名称
(2)烧瓶中发生反应的化学方程式为
(3)若D中盛有紫色石蕊试液,则D中的现象是
(4)若D中是FeCl2溶液,发生的现象是
(5)若D中盛有KI—淀粉的混合溶液,现象是
(6)E中一般应盛有
(7)若有17.4gMnO2完全反应,则可生成标准状况下Cl2的体积
您最近一年使用:0次
解题方法
4 . I.在碘化钾和硫酸的混合溶液中加入过氧化氢水溶液,迅速发生反应放出大量气体,反应过程可表示如下:
①H2O2+2KI+H2SO4=I2+K2SO4+2H2O;
②H2O2+I2=2HIO;
③H2O2+2HIO=I2+O2↑+2H2O
(1)H2O2在反应③中的作用是______ (填正确选项的标号)
A.氧化剂 B.还原剂 C.既是氧化剂又是还原剂 D.既不是氧化剂也不是还原剂
(2)有人认为上述反应说明了碘单质是过氧化氢分解的催化剂,你认为______ (填“对”或“不对”),其理由是______ 。
(3)上述反应说明H2O2、I2、HIO氧化性从强到弱的顺序是______ >______ >______ 。
II.硫酸亚铁(FeSO4·7H2O)是一种重要的食品和饲料添加剂。实验室通过如下实验由废铁屑制备FeSO4·7H2O晶体:
①将5%Na2CO3溶液加入到盛有一定量废铁屑的烧杯中,加热数分钟,用倾析法除去Na2CO3溶液,然后将废铁屑用水洗涤2~3遍;
②向洗涤过的废铁屑中加入过量的稀硫酸,控制温度在50~80℃之间至铁屑耗尽;
③趁热过滤,将滤液转入到密闭容器中,静置、冷却结晶;
④待结晶完毕后,滤出晶体,用少量冰水洗涤2~3次,再用滤纸将晶体吸干;
⑤将制得的FeSO4·7H2O晶体放在一个小广口瓶中,密闭保存。请回答下列问题:
(1)Fe(OH)3在碱性介质中与NaClO反应生成Na2FeO4和NaCl,写出Fe(OH)3与NaClO在碱性介质中反应的离子方程式是______ 。
(2)硫酸亚铁制备中实验步骤①的目的是______ 。
(3)实验步骤②明显不合理,理由是______ 。
(4)实验步骤④中用少量冰水洗涤晶体,其目的是______ 。
①H2O2+2KI+H2SO4=I2+K2SO4+2H2O;
②H2O2+I2=2HIO;
③H2O2+2HIO=I2+O2↑+2H2O
(1)H2O2在反应③中的作用是
A.氧化剂 B.还原剂 C.既是氧化剂又是还原剂 D.既不是氧化剂也不是还原剂
(2)有人认为上述反应说明了碘单质是过氧化氢分解的催化剂,你认为
(3)上述反应说明H2O2、I2、HIO氧化性从强到弱的顺序是
II.硫酸亚铁(FeSO4·7H2O)是一种重要的食品和饲料添加剂。实验室通过如下实验由废铁屑制备FeSO4·7H2O晶体:
①将5%Na2CO3溶液加入到盛有一定量废铁屑的烧杯中,加热数分钟,用倾析法除去Na2CO3溶液,然后将废铁屑用水洗涤2~3遍;
②向洗涤过的废铁屑中加入过量的稀硫酸,控制温度在50~80℃之间至铁屑耗尽;
③趁热过滤,将滤液转入到密闭容器中,静置、冷却结晶;
④待结晶完毕后,滤出晶体,用少量冰水洗涤2~3次,再用滤纸将晶体吸干;
⑤将制得的FeSO4·7H2O晶体放在一个小广口瓶中,密闭保存。请回答下列问题:
(1)Fe(OH)3在碱性介质中与NaClO反应生成Na2FeO4和NaCl,写出Fe(OH)3与NaClO在碱性介质中反应的离子方程式是
(2)硫酸亚铁制备中实验步骤①的目的是
(3)实验步骤②明显不合理,理由是
(4)实验步骤④中用少量冰水洗涤晶体,其目的是
您最近一年使用:0次
5 . 某化学兴趣小组为研究生铁(含碳)与浓硫酸的反应情况及产物性质,设计如下实验。请回答下列问题:
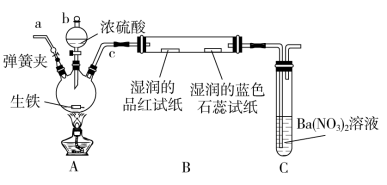
(1)按上图所示装置进行实验(夹持装置及尾气处理装置未画出)。仪器b的名称为__ 装置C中有白色沉淀生成,该沉淀是___ (填化学式)。
(2)装置A中还会产生CO2气体,请写出产生CO2的化学方程式:_____ 。
(3)为了验证装置A中产生的气体中含有CO2,应先从下列①~④中选出必要的装置连接A装置中c处管口,从左到右的顺序为__ (填序号);然后再进行的操作是从a处多次鼓入N2,其目的是___ 。
(4)某同学通过验证实验后期装置A中产生的气体中还含有H2,理由是___ (用离子方程式表示)。

(1)按上图所示装置进行实验(夹持装置及尾气处理装置未画出)。仪器b的名称为
(2)装置A中还会产生CO2气体,请写出产生CO2的化学方程式:
(3)为了验证装置A中产生的气体中含有CO2,应先从下列①~④中选出必要的装置连接A装置中c处管口,从左到右的顺序为

(4)某同学通过验证实验后期装置A中产生的气体中还含有H2,理由是
您最近一年使用:0次
2021-07-09更新
|
121次组卷
|
2卷引用:吉林省白城市第一中学2020-2021学年高一下学期期中考试化学试题
6 . 为探究硫酸亚铁晶体(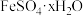 )在加热条件下的分解产物,设计如图实验。
)在加热条件下的分解产物,设计如图实验。
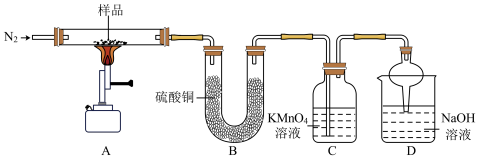
(1)实验过程中需缓慢持续通入氮气,其目的是排除装置中的空气和___________ 。
(2)装置B中可观察到的现象是___________ 。装置C中的现象是酸性高锰酸钾溶液褪色,检测表明溶液中含有Mn2+,则C中发生反应的离子方程式为___________ 。
(3)实验结束后发现装置A中有红棕色固体,经分析硫酸亚铁分解产物之一为SO3,则FeSO4分解的化学方程式为___________ 。
(4)装置D球形干燥管的作用___________
 )在加热条件下的分解产物,设计如图实验。
)在加热条件下的分解产物,设计如图实验。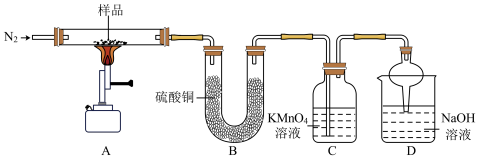
(1)实验过程中需缓慢持续通入氮气,其目的是排除装置中的空气和
(2)装置B中可观察到的现象是
(3)实验结束后发现装置A中有红棕色固体,经分析硫酸亚铁分解产物之一为SO3,则FeSO4分解的化学方程式为
(4)装置D球形干燥管的作用
您最近一年使用:0次
名校
7 . 某研究小组设计如图所示实验装置(夹持装置已略去)分别探究NO与铜粉、Na2O2的反应。
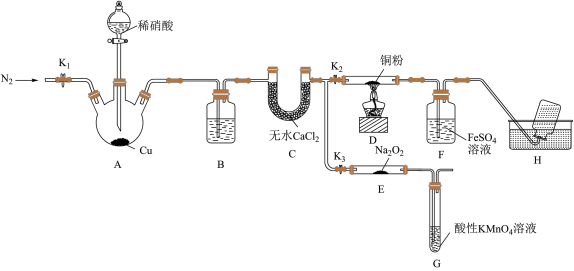
已知:①NO与Na2O2可发生反应2NO+Na2O2 =2NaNO2。
②NO、NO 能被酸性高锰酸钾溶液氧化为
能被酸性高锰酸钾溶液氧化为
③在溶液中存在平衡FeSO4+NO Fe(NO)SO4(棕色)
Fe(NO)SO4(棕色)
I.关闭K3,打开K2,探究NO与铜粉的反应并检验NO。
(1)反应开始前,打开K1,通入一段时间N2,其目的是________ 。
(2)装置B中盛放的试剂为水,其作用是________ 。
(3)装置F中的实验现象为______ 。装置H中收集的气体为N2和_______ (填化学式)。
Ⅱ.关闭K2,打开K3,探究NO与Na2O2的反应并制备NaNO2。
(4)装置G的作用是________ 。
(5)若省略装置C,则进入装置G中的气体除N2、NO外,可能还有NO2和_____ (填化学式)。
(6)测定反应后装置E中NaNO2的含量。已知;在酸性条件下,NO 可将MnO
可将MnO 还原为Mn2+,为测定样品中亚硝酸钠的含量,该小组同学称取ag样品溶于水配制成250mL溶液,取25.00mL所得溶液于锥形瓶中,用0.100mol·L-1的酸性KMnO4溶液滴定至终点时,消耗bmL酸性KMnO4溶液。
还原为Mn2+,为测定样品中亚硝酸钠的含量,该小组同学称取ag样品溶于水配制成250mL溶液,取25.00mL所得溶液于锥形瓶中,用0.100mol·L-1的酸性KMnO4溶液滴定至终点时,消耗bmL酸性KMnO4溶液。
①判断滴定终点的方法________ 。
②样品中NaNO2的质量分数为___________ (用含有a、b的代数式表示)。
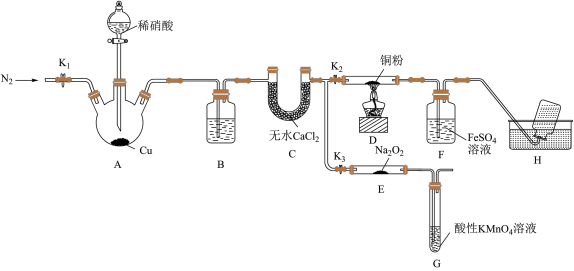
已知:①NO与Na2O2可发生反应2NO+Na2O2 =2NaNO2。
②NO、NO
 能被酸性高锰酸钾溶液氧化为
能被酸性高锰酸钾溶液氧化为
③在溶液中存在平衡FeSO4+NO
 Fe(NO)SO4(棕色)
Fe(NO)SO4(棕色)I.关闭K3,打开K2,探究NO与铜粉的反应并检验NO。
(1)反应开始前,打开K1,通入一段时间N2,其目的是
(2)装置B中盛放的试剂为水,其作用是
(3)装置F中的实验现象为
Ⅱ.关闭K2,打开K3,探究NO与Na2O2的反应并制备NaNO2。
(4)装置G的作用是
(5)若省略装置C,则进入装置G中的气体除N2、NO外,可能还有NO2和
(6)测定反应后装置E中NaNO2的含量。已知;在酸性条件下,NO
 可将MnO
可将MnO 还原为Mn2+,为测定样品中亚硝酸钠的含量,该小组同学称取ag样品溶于水配制成250mL溶液,取25.00mL所得溶液于锥形瓶中,用0.100mol·L-1的酸性KMnO4溶液滴定至终点时,消耗bmL酸性KMnO4溶液。
还原为Mn2+,为测定样品中亚硝酸钠的含量,该小组同学称取ag样品溶于水配制成250mL溶液,取25.00mL所得溶液于锥形瓶中,用0.100mol·L-1的酸性KMnO4溶液滴定至终点时,消耗bmL酸性KMnO4溶液。①判断滴定终点的方法
②样品中NaNO2的质量分数为
您最近一年使用:0次
2020-11-04更新
|
690次组卷
|
5卷引用:吉林省白城市洮南一中2021届高三上学期第三次月考化学试题
名校
解题方法
8 . 如图在A处通入 Cl2,当关闭B阀时,C处湿润的红色布条没有明显变化,当打开B阀时,C处湿润的红色布条逐渐褪色,则D瓶中所装的液体是
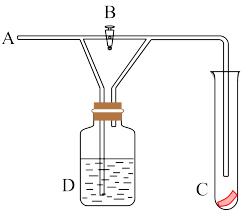

| A.水 | B.浓硫酸 |
| C.NaOH溶液 | D.饱和NaCl溶液 |
您最近一年使用:0次
2020-11-03更新
|
563次组卷
|
40卷引用:吉林省白城市洮南一中2020-2021学年高一上学期期中考试化学试题
吉林省白城市洮南一中2020-2021学年高一上学期期中考试化学试题吉林省洮南市第一中学2021-2022学年高一上学期第三次月考化学试题(已下线)2011届山东省实验中学高三上学期第一次诊断性测试化学卷(已下线)2010年上海市吴淞中学高一上学期期中考试化学试卷(已下线)2010年浙江省绍兴一中高一上学期期中考试化学试题(已下线)2010-2011学年山西省临汾一中高一上学期期末考试化学试卷(已下线)2011-2012学年浙江省瑞安中学高一上学期期中考试化学试卷(已下线)2012-2013学年广东省汕头四中高一上学期期末考试化学试卷(已下线)2013-2014学年浙江省湖州市属九校高一12月联考化学试卷2015-2016学年广东省仲元中学高一上学期期末化学试卷浙江省慈溪实验高级中学2017-2018学年高一上学期第一次月考化学试题黑龙江省牡丹江市第一高级中学2017-2018学年高二上学期期中考试化学(文)试题山东省济南市历城第二中学2017-2018学年高一上学期第三次调研化学试题江西省鹰潭市2017-2018学年高一上学期期末质量检测化学试题安徽省定远重点中学2018-2019学年高二上学期开学考试化学试题江西省遂川中学、吉安县中2017-2018学年高一上学期联考化学试题河南省登封实验高中2019-2020学年高一年级上学期第二次月考化学试题上海市华东师范大学附属天山中学2018-2019学年高一第一学期期中考试化学试题山东省济南外国语学校三箭分校2019-2020学年高一上学期期中考试化学试题山东省济南外国语学校2019-2020学年高一上学期期中考试化学试题步步为赢 高一化学寒假作业:作业十三 富集在海水中的元素——氯湖南省长沙市南雅中学2019-2020学年高一下学期入学考试化学试题(已下线)【新东方】2020-30上海市普通高中三校联考2019-2020学年高一上学期期中化学试卷(已下线)江西省宜丰中学2018_2019学年高一化学上学期期末考试试卷安徽省蚌埠市第二中学2020-2021学年高一10月月考化学(文)试题安徽省蚌埠市第二中学2020-2021学年高一10月月考化学(理)试题安徽省滁州市定远县重点中学2020-2021学年高一10月月考化学试题黑龙江省绥化市第一中学2020-2021学年高一上学期第二次月考化学试题(已下线)第15单元 实验设计与评价(A卷 基础过关检测)-2021年高考化学一轮复习单元滚动双测卷广东实验中学2020-2021学年高一上学期期中考试化学试题(已下线)【浙江新东方】【2021.4.27】【宁波】【高一上】【高中化学】【00139】贵州省凯里市第一中学2021-2022学年高一上学期期中考试化学试题广东省梅州市大埔县虎山中学2021-2022学年高一上学期第一次段考(11月)化学试题黑龙江省鸡东县第二中学2021-2022学年高一上学期期中考试(B班)化学试题黑龙江省鸡东县第二中学2021-2022学年高一上学期期中考试(实验班)化学试题云南衡水实验中学2021-2022学年高一上学期期末考试化学试题上海市南汇中学2022-2023学年高一上学期期末考试化学试题(已下线)【新东方】高一化学二轮班期中诊断试题卷 B1河北省石家庄市正定县弘文中学2023-2024学年高一上学期期中考试化学试题
名校
解题方法
9 . Y形管是一种特殊的仪器,与其他仪器组合可以进行某些探究实验。利用如图所示装置可以探究SO2与BaCl2反应生成沉淀的条件。下列判断正确的是( )
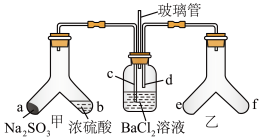

| A.玻璃管的作用是连通大气,使空气中的氧气进入广口瓶,参与反应 |
| B.c、d两根导管都必须插入BaCl2溶液中,保证气体与Ba2+充分接触 |
| C.Y形管乙中产生的是氧化性气体,将BaSO3氧化为BaSO4沉淀 |
| D.e、f两管中的试剂可以分别是浓氨水和NaOH固体 |
您最近一年使用:0次
2020-09-23更新
|
1673次组卷
|
24卷引用:吉林省大安一中2019-2020学年高三上学期第四次月考化学试题
吉林省大安一中2019-2020学年高三上学期第四次月考化学试题【全国校级联考】辽宁省六校协作体2019届高三上学期期初联考化学试题甘肃省师范大学附属中学2019届高三上学期第一次月考化学试题辽宁省葫芦岛协作校2019届高三上学期第一次月考化学试题(已下线)《2018-2019学年同步单元双基双测AB卷》 第四单元 非金属及其化合物单元测试 B卷陕西省西安市长安区第五中学2019届高三上学期期中考试化学试题河北省衡水市衡水中学2019届高三上学期期中考试化学试题辽宁省沈阳市东北育才学校2019届高三上学期第三次模拟化学试题【全国百强校】甘肃省兰州市第一中学2019届高三上学期12月月考化学试题河南省许昌高级中学2020届高三上学期第一次月考化学试题河北省石家庄市行唐县三中2020届高三11月月考化学试题专题5.1 化学实验基础(综合提升卷)——巅峰冲刺2020年高考化学二轮专项提升专题3.2 非金属及其化合物(疑难突破)——巅峰冲刺2020年高考化学二轮专项提升河北省石家庄市第二中学2020届高三下学期3月月考理科综合化学试题陕西省榆林市绥德县绥德中学2020届高三下学期第五次模拟考试化学试题(已下线)第九单元 化学实验基础测试题-2021年高考化学一轮复习名师精讲练高一必修第一册(鲁科2019)第3章 章末综合检测卷(已下线)易错19 实验装置类选择题-备战2021年高考化学一轮复习易错题山东省胶州市实验中学2020-2021学年高一上学期12月月考化学试题(人教版2019)必修第二册 第五章 化工生产中的重要非金属元素 章末综合检测卷湖北省华中师范大学第一附属中学2020-2021学年高一下学期期中检测化学试题广东省东莞市东华高级中学东华松山湖高级中学2022-2023学年高一下学期5月期中考试化学试题广东省潮州市饶平县第二中学2020-2021学年高一下学期第一次月考化学试题黑龙江省哈尔滨市第一中学校2022-2023学年高一下学期期中考试化学试题
名校
解题方法
10 . 为探究Na2O2与H2O的反应,进行了如下实验:有关说法不正确 的是( )


| A.实验ⅰ中发生反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑ |
| B.实验ⅲ中MnO2做H2O2分解反应的催化剂 |
| C.综合实验ⅰ和ⅲ可以说明Na2O2与H2O反应有H2O2生成 |
| D.综合实验表明,实验ⅱ酚酞褪色的原因是溶液碱性变弱 |
您最近一年使用:0次
2020-09-10更新
|
1437次组卷
|
17卷引用:吉林省大安市第一中学校2021届高三上学期第二次月考化学试题
吉林省大安市第一中学校2021届高三上学期第二次月考化学试题北京市延庆区2021届高三上学期统测(9月)考试化学试题山东省德州市齐河县实验中学2021届高三第一次月考化学试题北京市第十二中学2020-2021学年高一上学期期中考试化学试题黑龙江省鸡西市第一中学2020-2021学年高一上学期第一次月考化学试题北京市第二十中学2021-2022学年高一上学期期中考试化学试题北京市东直门中学2021-2022学年高一上学期期中考试化学试题广东省佛山市第一中学2021-2022学年高一上学期期中考试化学试题吉林省长春市十一高中2021-2022学年高一上学期第二学程考试化学试卷江苏省泰州中学2021-2022学年高一上学期期末考试化学试题(已下线)2.1.2 钠的氧化物与焰色试验-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)河北省石家庄市第十五中学2022-2023学年高一上学期期中考试化学试题四川省泸县第四中学2022-2023学年高一上学期第三次月考化学试题广东省深圳市福田区红岭中学2022-2023学年高一上学期第二学段期末考试化学试题(已下线)【知识图鉴】单元讲练测必修第一册第二单元03巩固练江苏省前黄高级中学2022-2023学年高一下学期综合素质测试化学试题(已下线)专题05 金属钠及钠的化合物-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(江苏专用)



