1 . 无水FeCl2是重要的污水处理剂,不溶于C6H5Cl、C6H4Cl2,易溶于乙醇,易吸水和易被氧化。某实验小组利用无水FeCl3和C6H5Cl(氯苯,无色液体,沸点132℃)制备少量无水FeCl2。实验原理:2FeCl3+C6H5Cl 2FeCl2+C6H4Cl2+HCl↑,回答以下问题:
2FeCl2+C6H4Cl2+HCl↑,回答以下问题:
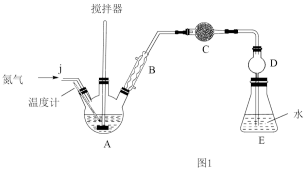
(1)先按图1所示组装好装置,再___________ 后,最后向三颈烧瓶A中加入一定量的无水FeCl3和氯苯(加热装置略去)。
(2)工业氮气中常含有H2O、O2、CO2,需用下图仪器和试剂提纯后才可通入三颈烧瓶A中进行相关反应。
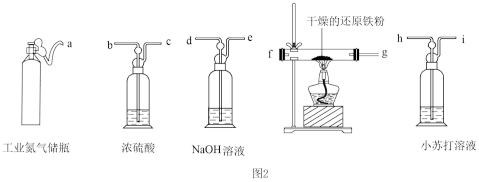
①请从图2中选择必要的装置,按气流方向其合理的连接顺序:a→___________ →j。
②在反应开始之前先通二段时间N2的目的是___________ 。
(3)装置C中的试剂是___________ (填试剂名称),其作用是___________ 。
(4)控制温度在128~139℃条件下对三颈烧瓶A加热2h,混合物颜色逐渐变浅,黏度降低。该步骤中加热温度已经接近或超过C6H5Cl沸点,但氯苯实际损失量却非常小,其原因是___________ 。
(5)下列装置中与D的作用相同的是___________ 。
(6)冷却后,将三颈瓶内物质经过滤、洗涤干燥后,得到粗产品。简述回收滤液中C6H5Cl的实验方案___________ 。
 2FeCl2+C6H4Cl2+HCl↑,回答以下问题:
2FeCl2+C6H4Cl2+HCl↑,回答以下问题:
(1)先按图1所示组装好装置,再
(2)工业氮气中常含有H2O、O2、CO2,需用下图仪器和试剂提纯后才可通入三颈烧瓶A中进行相关反应。

①请从图2中选择必要的装置,按气流方向其合理的连接顺序:a→
②在反应开始之前先通二段时间N2的目的是
(3)装置C中的试剂是
(4)控制温度在128~139℃条件下对三颈烧瓶A加热2h,混合物颜色逐渐变浅,黏度降低。该步骤中加热温度已经接近或超过C6H5Cl沸点,但氯苯实际损失量却非常小,其原因是
(5)下列装置中与D的作用相同的是

(6)冷却后,将三颈瓶内物质经过滤、洗涤干燥后,得到粗产品。简述回收滤液中C6H5Cl的实验方案
您最近一年使用:0次
解题方法
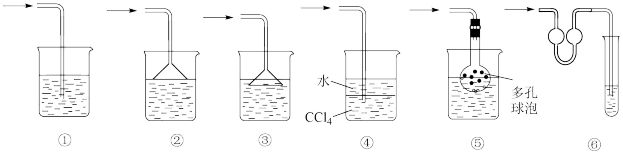
2 . 利用如图所示装置进行下列实验,能得出相应实验结论的是( )
| 选项 | ① | ② | ③ | 实验结论 |  |
| A | 浓盐酸 | MnO2 | NaBr溶液 | 氧化性Cl2>Br2 | |
| B | 浓氨水 | 碱石灰 | AgNO3溶液 | AgOH具有两性 | |
| C | 浓硫酸 | Na2SO3 | FeCl3溶液 | SO2具有还原性 | |
| D | 稀盐酸 | Na2CO3 | Na2SiO3溶液 | 非金属性:Cl>C>Si |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-02-13更新
|
147次组卷
|
4卷引用:2015届陕西省宝鸡中学高三上学期12月月考理综化学试卷(A)
3 . 某化学兴趣小组利用下图装置探究验证黄铜矿(主要成分CuFeS2)在空气中的氧化产物并测定CuFeS2的纯度(杂质为SiO2)。
实验步骤:①组装好仪器,检查装置的气密性良好。②加入药品,打开弹簧夹,从左口不断鼓入空气。③点燃B处的酒精喷灯,高温灼烧石英管中黄铜矿的样品。
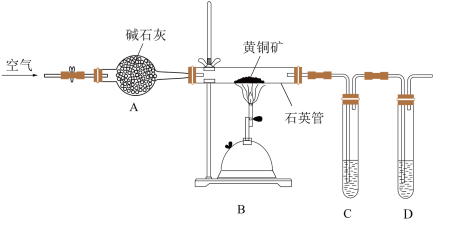
请回答下列问题。
(1)仪器A中的试剂是________ ,其作用为________ 。
(2)为检验灼烧氧化黄铜矿产生的气体,则C、D中的试剂可选择________ (多选)。
a.Na2S溶液、NaOH溶液
b.BaCl2溶液、NaOH溶液
c.品红溶液、NaOH溶液
d.KMnO4溶液、NaOH溶液
(3)查阅资料:
①样品经煅烧后得到的固体可能为泡铜(Cu、Cu2O)和熔渣(Fe2O3、FeO)。
②Cu2O与稀H2SO4的反应为:Cu2O+H2SO4=Cu+CuSO4+H2O
探究Ⅰ:为验证熔渣的成分,取分离出的熔渣少许于试管中,加入适量的稀硫酸溶解,取两份所得液。完成下表中横线上的内容。
探究Ⅱ:设计实验方案验证泡铜中是否含有Cu2O?________ 。
(4)为测定CuFeS2的纯度,称取a g的黄铜矿样品充分燃烧后,甲、乙两组同学设计如下两个不同的实验方案(以下纯度结果均用含相应字母的代数式表示)。
甲方案:若C试管中为足量的H2O2和NaOH的混合溶液,吸收完气体后向C中加入过量的BaCl2溶液振荡且静置,经过滤后处理得到固体为w g,则CuFeS2的纯度为________ 。写出C试管中吸收气体时的总反应的离子方程式________ 。
乙方案:从上述煅烧产物中分离出泡铜,使其完全溶于稀硝酸并配成250mL的溶液,取出25.00mL该溶液用c mol·L-1的标准液EDTA(用H2Y2-表示)滴定至终点(滴定荆不与杂质反应),消耗EDTA标准液V mL,则CuFeS2的纯度为________ 。(滴定时的反应为:Cu2++H2Y2-=CuY2-+2H+)
实验步骤:①组装好仪器,检查装置的气密性良好。②加入药品,打开弹簧夹,从左口不断鼓入空气。③点燃B处的酒精喷灯,高温灼烧石英管中黄铜矿的样品。

请回答下列问题。
(1)仪器A中的试剂是
(2)为检验灼烧氧化黄铜矿产生的气体,则C、D中的试剂可选择
a.Na2S溶液、NaOH溶液
b.BaCl2溶液、NaOH溶液
c.品红溶液、NaOH溶液
d.KMnO4溶液、NaOH溶液
(3)查阅资料:
①样品经煅烧后得到的固体可能为泡铜(Cu、Cu2O)和熔渣(Fe2O3、FeO)。
②Cu2O与稀H2SO4的反应为:Cu2O+H2SO4=Cu+CuSO4+H2O
探究Ⅰ:为验证熔渣的成分,取分离出的熔渣少许于试管中,加入适量的稀硫酸溶解,取两份所得液。完成下表中横线上的内容。
| 试样 | 加入试剂及操作 | 实验现象 | 得出结论 |
| 第一份 | 滴入几滴K3Fe(CN)6]溶液 | 含FeO | |
| 第二份 | 滴入几滴 | 溶液变为血红色 | 含Fe2O3 |
(4)为测定CuFeS2的纯度,称取a g的黄铜矿样品充分燃烧后,甲、乙两组同学设计如下两个不同的实验方案(以下纯度结果均用含相应字母的代数式表示)。
甲方案:若C试管中为足量的H2O2和NaOH的混合溶液,吸收完气体后向C中加入过量的BaCl2溶液振荡且静置,经过滤后处理得到固体为w g,则CuFeS2的纯度为
乙方案:从上述煅烧产物中分离出泡铜,使其完全溶于稀硝酸并配成250mL的溶液,取出25.00mL该溶液用c mol·L-1的标准液EDTA(用H2Y2-表示)滴定至终点(滴定荆不与杂质反应),消耗EDTA标准液V mL,则CuFeS2的纯度为
您最近一年使用:0次
2019-03-20更新
|
642次组卷
|
3卷引用:【市级联考】陕西省宝鸡市2019届高三下学期高考模拟检测(二)理科综合化学试题
【市级联考】陕西省宝鸡市2019届高三下学期高考模拟检测(二)理科综合化学试题【全国百强校】陕西省宝鸡中学2019届高三下学期第二次模拟考试理科综合化学试题(已下线)专题03 化学实验专题-【大题精做】冲刺2023年高考化学大题突破+限时集训(新高考专用)
4 . 绿矾(FeSO4·7H2O)可作还原剂、着色剂、制药等,在不同温度下易分解得到各种铁的氧化物和硫的氧化物。已知SO3是一种无色晶体,熔点16.8℃,沸点44.8℃,氧化性及脱水性强于浓硫酸,能漂白某些有机染料,如品红等。回答下列问题:
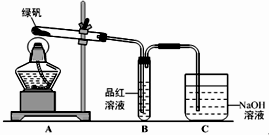
(1)甲组同学按照上图所示的装置,通过实验检验绿矾的分解产物。装置C的作用是_______________ 。装置B中可观察到的现象是__________________________ ,甲组同学由此得出绿矾的分解产物中含有SO2。
(2)乙组同学认为甲组同学的实验结论不严谨,认为需要补做实验。对甲组同学做完实验的B装置的试管加热,发现褪色的品红溶液未恢复红色,则可证明绿矾分解的产物中______ (填字母)。
A.不含SO2 B.可能含SO2 C.一定含有SO3
(3)丙组同学查阅资料发现绿矾受热分解还可能有O2放出,为此,丙组同学选用甲组同学的部分装置和下图部分装置设计出了一套检验绿矾分解所得气态产物的装置:
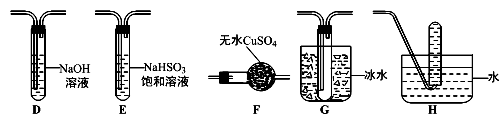
①丙组同学的实验装置中,依次连接的合理顺序为A→_________________ →H。
②能证明绿矾分解产物中有O2的检验方法是________________________ 。
(4)为证明绿矾分解产物中含有三价铁的操作及现象__________________________ 。

(1)甲组同学按照上图所示的装置,通过实验检验绿矾的分解产物。装置C的作用是
(2)乙组同学认为甲组同学的实验结论不严谨,认为需要补做实验。对甲组同学做完实验的B装置的试管加热,发现褪色的品红溶液未恢复红色,则可证明绿矾分解的产物中
A.不含SO2 B.可能含SO2 C.一定含有SO3
(3)丙组同学查阅资料发现绿矾受热分解还可能有O2放出,为此,丙组同学选用甲组同学的部分装置和下图部分装置设计出了一套检验绿矾分解所得气态产物的装置:

①丙组同学的实验装置中,依次连接的合理顺序为A→
②能证明绿矾分解产物中有O2的检验方法是
(4)为证明绿矾分解产物中含有三价铁的操作及现象
您最近一年使用:0次
名校
5 . 烧硫酸铝铵晶体,发生的主要反应为4[NH4Al(SO4)2·12H2O] 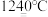 2A12O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O。将产生的气体通过下图所示的装置(假设试剂均过量)。下列说法正确的是
2A12O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O。将产生的气体通过下图所示的装置(假设试剂均过量)。下列说法正确的是
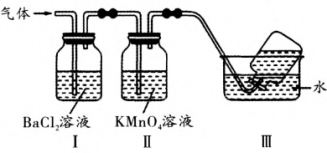
 2A12O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O。将产生的气体通过下图所示的装置(假设试剂均过量)。下列说法正确的是
2A12O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O。将产生的气体通过下图所示的装置(假设试剂均过量)。下列说法正确的是
| A.反应中硫元素既体现氧化性又体现还原性 |
| B.装置Ⅰ中可以观察到出现白色沉淀,其主要成分是BaSO4和BaSO3 |
| C.装置Ⅱ中可以观察到高锰酸钾紫色褪去 |
| D.将装置Ⅰ、Ⅱ顺序交换,仍能观察到相同的现象 |
您最近一年使用:0次
11-12高三上·陕西宝鸡·阶段练习
6 . 某研究小组为了探究“铁与水蒸气”能否发生反应及反应的产物,进行了下列实验:(1)用如图所示实验装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”(石棉绒是耐高温材料,不与水和铁反应)。

①反应一段时间后,有肥皂泡吹起时,用点燃的火柴靠近肥皂泡,当________ 时(填实验现象),说明“铁与水蒸气”能够进行反应。
②写出铁与水蒸气反应的化学方程式_______________ 。
③实验中石棉绒的作用是______________ 。
(2)为了研究一定时间内铁粉的转化率,他们设计了如下实验:准确称量一定质量的铁粉进行反应,收集并测量反应后生成气体的体积,计算出铁粉的转化率。
①收集并测量气体体积应选图中的________ 装置。

②称取0.24 g铁粉与适量石棉绒混合,然后加热至无气体放出。若室温下氢气密度约为0.088 g/L,最好选用______ 规格的量筒(选填字母序号)。

①反应一段时间后,有肥皂泡吹起时,用点燃的火柴靠近肥皂泡,当
②写出铁与水蒸气反应的化学方程式
③实验中石棉绒的作用是
(2)为了研究一定时间内铁粉的转化率,他们设计了如下实验:准确称量一定质量的铁粉进行反应,收集并测量反应后生成气体的体积,计算出铁粉的转化率。
①收集并测量气体体积应选图中的

②称取0.24 g铁粉与适量石棉绒混合,然后加热至无气体放出。若室温下氢气密度约为0.088 g/L,最好选用
| A.100 mL | B.200 mL |
| C.500 mL | D.1 000 mL |
您最近一年使用:0次



